
科目: 来源: 题型:
【题目】A、B、C、D、E、F属于短周期主族元素.A的原子半径是短周期中最大,B元素的原子最外层电子数为m、次外层电子数为n,C元素的原子L层电子数为m+n, M层电子数为m﹣n,D元素与C元素同主族,E元素原子与B元素原子的核外电子数之比为2:1,F的一种原子中,质量数与质子数之差为零.
(1)写出元素的名称C________E________F________.
(2)C在周期表中的位置是________
(3)A2B2的电子式为______.
(4)A、B形成的简单离子的半径由大到小的顺序为________.(用对应的化学符号填空,下同)
(5)A、E形成的是________(填共价或离子)化合物
(6)B、E两种元素形成的气态氢化物中稳定性更强的是______;
(7)由元素C形成的单质Y与由A、B、F三种元素形成的化合物X的水溶液反应的离子方程式为___________________________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关NaClO和NaCl混合溶液的叙述正确的是 ( )
A. 该溶液中,H+、NH![]() 、SO
、SO![]() 、I-可以大量共存
、I-可以大量共存
B. 该溶液中,Ag+、K+、NO![]() 、NH
、NH![]() 可以大量共存
可以大量共存
C. 该溶液中, Fe2+、Fe3+、Cl-、NO![]() 可以大量共存
可以大量共存
D. 向该溶液中加入浓盐酸,每产生1 molCl2,转移电子约为6.02×1023个
查看答案和解析>>
科目: 来源: 题型:
【题目】我们的衣食住行中都蕴含着丰富的化学知识,下列说法中正确的是( )
A.衣料中的蚕丝和涤纶都属于合成有机高分子材料
B.加碘食盐和铁强化酱油都可以补充人体必需的微量元素
C.建筑高楼大厦时用到的钢是纯净物
D.用液化石油气代替汽油作汽车燃料,不会造成空气污染
查看答案和解析>>
科目: 来源: 题型:
【题目】“两型”社会,提倡“低碳”生活,下列有关碳及碳的化合物叙述中正确的是( )
A.二氧化碳是形成酸雨的主要气体
B.金刚石、石墨都是碳单质,两者碳原子的排列方式相同
C.一氧化碳含量增加会导致温室效应
D.大气中二氧化碳的消耗途径主要是绿色植物的光合作用
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ | ||||||
(1)金属性最强的元素是___________(填元素名称);⑥的离子结构示意图是________________ ;
(2)④、⑤、⑥的原子半径由大到小的顺序为_________________。 (填元素符号);
(3)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是________________。
(4)少量元素⑤的单质通常保存在_______________中;
(5)用电子式表示④和⑤形成化合物的过程: ___________________
(6)常温下,将元素⑧的单质通入元素⑤的最高价氧化物对应的水化物中,其反应的离子方程式为___________________。
(7)在⑧与⑩的单质中,化学性质较活泼的是____________________,(填元素符号)
请设计一个实验方案,证明⑧和⑩的非金属性强弱___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图A、B、C、D、E五组仪器(图中a、b、c表示止水夹)可以根据需要组装成不同实验装置.某兴趣小组的同学利用这些实验仪器进行实验,请对其方案进行完善或评价.
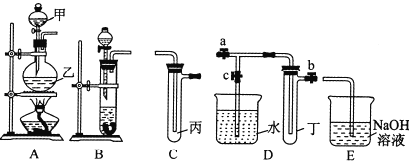
(1)将B、C、E相连,用浓硫酸和浓盐酸可制取氯化氢,装在分液漏斗中的试剂是 ,该实验尾气吸收装置设计有何不妥? ;改正后将B、D、E装置相连,用D装置中的丁试管收集满氯化氢气体,使烧杯中的水进入试管丁的操作是 。
(2)将A、C、E相连,并在丙中加入适量水,即可制得氯水,将所得氯水分为两份,进行ⅠⅡ两个实验,实验操作、现象、结论如下表所示:
序号 | 实验操作 | 现象 | 结论 |
Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物有具有酸性 |
请你评价:实验I推出的相应的结论是否合理? ;若不合理,请说明理由,〔若合理则无需填写) 。实验Ⅱ推出的结论是否合理? ;若不合理,请说明理由,(若合理则无需填写) 。
(3)研究表明,用ClO2气体对自来水消毒效果比用Cl2更好.市售的一种新型消毒剂含两种成分,分别是NaClO3和Na2C2O4.两种成分在溶液中混合便产生ClO2,反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用炭还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl![]() SiHCl3+H2;
SiHCl3+H2;
③SiHCl3与过量H2在1000~1100 ℃反应制得纯硅。
已知:SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学方程式为_____________________。
(2)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
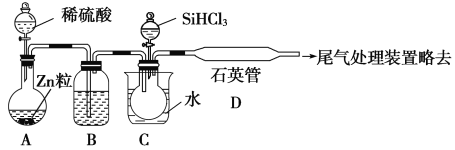
①装置B中的试剂是________。装置C中的烧瓶需要加热,其目的是_________________。
②反应一段时间后,装置D中观察到的现象是________________,装置D中发生反应的化学方程式为__________________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及__________________________。
④SiHCl3的电子式为________,SiHCl3与H2O反应的化学方程式为:_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com