
科目: 来源: 题型:
【题目】在CO2中,Mg燃烧生成MgO和C。下列说法正确的是( )
A. 元素C的单质只存在金刚石和石墨两种同素异形体
B. Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg)
C. 在该反应条件下,Mg的还原性强于C的还原性
D. 该反应中化学能全部转化为热能
查看答案和解析>>
科目: 来源: 题型:
【题目】某烷烃的各种同分异构体中,主链上有4个碳原子的只有两种结构,则含相同碳原子数且主链上也有4个碳原子的单烯烃的同分异构体有
A.2种 B.3种 C.4种 D.5种.
查看答案和解析>>
科目: 来源: 题型:
【题目】I.锰是在地壳中广泛分布的元素之一,其单质和化合物在工农业生产中有着重要的作用。已知Al的燃烧热为ΔH=—ckJ·mol—1,金属锰可用铝热法制得。其余相关热化学方程式为:3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) ΔH1 = akJ·mol—1
3MnO2(s)=Mn3O4(s)+O2(g) ΔH2 = b kJ·mol—1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) ΔH3 =__________kJ·mol—1(用含a、b、c的式子表示)
II.无机和有机氰化物在工农业生产中应用广泛,尤其是冶金工业常用氰化物,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。
(1)电解处理法:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为__________(填“阴极”或“阳极”),阳极产生ClO-的电极反应为__________,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为__________。
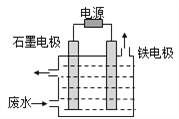
(2)UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH—=4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。
①废水中的CN一经以下反应实现转化:CN—+H2O2+H2O=A+NH3↑,则A是__________(用符号表示)。
②含氰废水在不同pH下的除氰效果如图所示,pH选择的最佳范围应为__________(a.7-10;b.10-11;c.11-13),解释该pH不宜太大的原因__________。
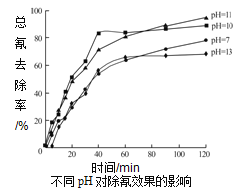
查看答案和解析>>
科目: 来源: 题型:
【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂.
Ⅰ.测定中和热.
(1)写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式 (中和热数值为57.3kJ/mol):
(2)取50mL 0.5mol/L HCl溶液与50mL0.55mol/L NaOH溶液进行测定,但实验数值小于57.3kJ/mol,原因可能是 _(填序号).
A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
B.量取盐酸的体积时仰视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
D.实验装置保温、隔热效果差
Ⅱ.酸碱中和滴定.
(1)某学生用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液,选择酚酞作指示剂.实验中不必用到的是
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
(2)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________.当________时,即停止滴定.
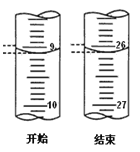
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:已知用c(HCl)=0.10 mol/L的盐酸标定25mL的氢氧化钠溶液,测得c(NaOH)______ ___mol/L
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是___ ___(填序号).
A.锥形瓶用蒸馏水洗净后没有干燥
B.碱式滴定管未用待测液润洗就直接注入待测氢氧化钠溶液
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.将铜丝插入稀硝酸中:Cu+4H++2NO3-![]() Cu2++2NO2↑+H2O
Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe![]() 2Fe2+
2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O![]() Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+![]() H2SiO3↓+2Na+
H2SiO3↓+2Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】青蒿素人工合成的部分反应流程如下:

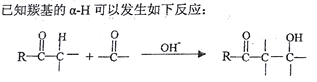
(1)化合物G中含有的官能团名称为:__________、__________,E→F的反应类型为__________。
(2)D→E先后由加成和消去两步反应完成,加成后得到的中间产物的结构简式为__________。
(3)B→C的方程式为__________。(4)写出符合下列要求的H的一种同分异构体的结构简式__________。
①既能与NaHCO3反应放出气体,也能使FeCl3溶液显紫色;
②分子中有四种不同环境的氢原子。
(5)利用题中所给信息,试以苯甲醇( )和乙烯为原料(其他无机试剂任选),合成
)和乙烯为原料(其他无机试剂任选),合成 。__________________________
。__________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A、铁与稀H2SO4反应时,加入少量CuSO4溶液,可使反应速率加快
B、构成原电池的正极和负极必须是两种不同的金属
C、在铁上镀铜时,金属铜作阴极
D、用惰性电极电解CuSO4溶液,溶液的pH不变
查看答案和解析>>
科目: 来源: 题型:
【题目】相同状况下,等质量的O2和CO2相比较,下列叙述正确的是
A.体积比为8︰11 B.密度之比为1︰1
C.物质的量之比为11︰8 D.原子个数之比为12︰11
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )

加入催化剂,减小了反应的热效应
B、加入催化剂,可提高H2O2的平衡转化率
C、H2O2分解的热效应△H<0
D、反应物的总能量高于生成物的总能量
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出)。

已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
(1)甲元素在周期表中的位置为______________。
(2)丙、丁可形成AB2型化合物,其结构式为________。
(3)丙是自然界中形成化合物种类最多的元素,其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是______________________。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,写出这些化合物中任意两种符合以下条件的化学式_______________,________________________。(①原子个数比为1∶2;②分子中价电子总数为偶数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com