
科目: 来源: 题型:
【题目】现有物质的量浓度相等的下列溶液:①醋酸、②盐酸、③苯酚钠、④苯酚、⑤碳酸钠、⑥碳酸氢钠、⑦硫酸、⑧氢氧化钠,按溶液pH由小到大排列正确的是
A.④①②⑦⑥③⑤⑧ B.④①②⑦⑤⑥③⑧
C.⑦①②④⑥③⑤⑧ D.⑦①④②③⑥⑤⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】根据右表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各离子浓度的关系正确的是:
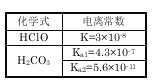
A.c(HCO3-)>c(ClO-)>c(OH-)
B.c(ClO-)>c(HCO3-)>c(H+)
C.c(ClO-)+c(HClO)=c(HCO3-)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】某二元弱酸(简写为H2A)溶液,按下式发生一级或二级电离:
H2A![]() H++HA—;
H++HA—;
HA—![]() H++A2—;
H++A2—;
已知同温同浓度时的电离平衡常数K(H2A)远大于K(HA—),设有下列四种溶液体系:
A. 0.01 mol/L的H2A溶液
B. 0.01 mol/L的NaHA溶液
C. 0.02 mol/L的盐酸与0.04 mol/L的NaHA溶液等体积混合液
D. 0.02 mol/L的氢氧化钠溶液与0.02 mol/L的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1)H+浓度最大的是 ,最小的是 。
(2)H2A浓度最大的是 ,最小的是 。
(3)A2— 浓度最大的是 ,最小的是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是:
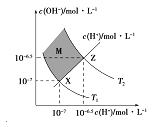
A. 两条曲线间任意点均有c(H+)×c(OH-)=KW
B. M区域内任意点均有c(H+)<c(OH-)
C. 图中T1<T2
D. XZ线上任意点均有pH=7
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,用0.100mol﹒L-1NaOH溶液分别滴定20.00ml0.100mol﹒L-1的盐酸和醋酸,

A.Ⅰ表示的是滴定盐酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C.V(NaOH)=20mL时,两份溶液中c(Cl-)=c(CH3COO-)
D.V(NaOH)=10mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
①Zn为正极,Cu为负极;
②H+向负极移动;
③电子是由Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为0.5mol;
⑥正极的电极反应式为Zn﹣2e﹣═Zn2+.

A.①②③ B.③④⑤ C.④⑤⑥ D.②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,下列说法正确的是

A. 0-t1时,原电池的负极是铜片
B. 0-t1时,正极的电极反应式是2H++2e-=H2↑
C. t1时刻,电流方向发生变化的原因是Al 在浓硝酸中发生钝化,氧化膜阻止了Al进一步反应
D. tl时刻后,电子从铝经过导线流向铜
查看答案和解析>>
科目: 来源: 题型:
【题目】醋酸是一种常见的弱酸,回答下列问题:
(1)醋酸的电离方程式是 ;
在0.1mol·L﹣1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:
(2)向醋酸中加入醋酸钠固体,电离平衡 移动(填向左、向右或不变,下同);c(H+) (填增大、减小或不变,下同),pH (填增大、减小或不变,下同)
(3)向醋酸中加入碳酸钙固体,电离平衡向 移动;c(CH3COOH) .
(4)向醋酸中加入大量的水,c(OH﹣) .导电能力 ,电离平衡常数 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com