
科目: 来源: 题型:
【题目】埋在地下的铸铁输油管道,在下列各种情况下,被腐蚀速率最慢的是( )
A.在潮湿疏松的碱性土壤中
B.在含铁元素较多的酸性土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多,潮湿透气的中性土壤中
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关纯净物、混合物、电解质、非电解质的正确组合为
选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
A | 纯盐酸 | 淀粉溶液 | 硫酸 | 液氨 |
B | 漂粉精 | 水玻璃 | 氧化铝 | 二氧化硫 |
C | 胆矾 | 氢氧化铁胶体 | 碳酸钠 | 乙醇 |
D | 水银 | 澄清石灰水 | 氯化铜 | 铁 |
查看答案和解析>>
科目: 来源: 题型:
【题目】氮及其化合物在生产生活中应用广泛, 其转化关系如下图所示:

(1)NH3的电子式是__________。
(2)ii 中 NH3氧化时发生如下反应:
4NH3(g)+5O2(g) = 4NO(g)+6H2O(g) ΔH1=-907.28 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH2=-1811.63kJ·mol-1
则4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH3=_________kJ·mol-1
(3)iv中反应 2NO(g)+O2(g) ![]() 2NO2(g), 其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、 p2)下随温度变化的曲线如图一所示, 则 p1_____ p2 (填“>”“<”或“=”, 下两空同);
2NO2(g), 其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、 p2)下随温度变化的曲线如图一所示, 则 p1_____ p2 (填“>”“<”或“=”, 下两空同);
该反应的ΔH ______0;A、B 两点的化学反应速率:v(A) ______v(B) 。 已知 400℃时, 投入的NO和O2的起始量分别为x mol 和y mol,此时容器体积为V L,A 点的平衡常数 K=______(用x、y、V表示) 。
(4)利用电化学降解法治理水中的硝酸盐污染(如图二),电解槽中间用质子交换膜隔开,污水放入II区, 通电使NO3-转化为N2,a为电源的______极,Ag-Pt电极上的电极反应式是________。

查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯是重要的有机原料,根据以下合成路线,回答问题。
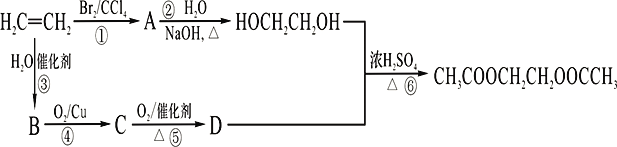
(1)写出乙烯的电子式_____________;A的名称为______________;
(2)B分子中的官能团名称是_________________;
(3)写出指定反应的反应类型:②________________,③______________;
(4)写出指定反应的化学方程式:④________________;⑥_____________。
(5)与B和D反应的生成物互为同分异构体,其中能和氢氧化钠反应的物质的结构简式_____________;
(6)HOCH2CH2OH能被酸性高锰酸钾氧化成E,写出E和HOCH2CH2OH生成高聚物的化学方程式______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++2H+=Ag++2NH![]()
B.向Na2O2中加入足量的水:2Na2O2+2H2O=4Na++4OH-+O2↑
C.向硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓
D.向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO![]() +2OH—=CaCO3↓+CO
+2OH—=CaCO3↓+CO![]() +2H2O
+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料﹣纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
![]() +H2O+H2SO4
+H2O+H2SO4![]()
![]() +NH4HSO4
+NH4HSO4
(苯乙腈)
![]() +Cu(OH)2→(
+Cu(OH)2→(![]() )2Cu+H2O
)2Cu+H2O
制备苯乙酸的装置示意图如图(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇.
回答下列问题:
(1)在250mL三口瓶a中加入70mL 70%硫酸.配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是 .
(2)将a中的溶液加热至100℃,缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应.在装置中,仪器b的作用是 ;仪器c的名称是 ,其作用是 .反应结束后加适量冷水,再分离出苯乙酸粗品.加入冷水的目的是 ,下列仪器中可用于分离苯乙酸粗品的是 (填标号)
A、分液漏斗
B、漏斗
C、烧杯
D、直形冷凝管
E、玻璃棒
(3)提纯苯乙酸的方法是重结晶,最终得到44g纯品,则苯乙酸的产率是 .(百分数)
(4)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列做法或操作中不正确的是
①做实验时可用手直接拿取金属钠
②夜间发生厨房煤气泄漏,应立即开灯检查煤气泄漏的原因,并打开所有门窗通风
③不慎将浓H2SO4沾在皮肤上,立即用NaOH溶液冲洗
④进行SO2性质实验时要在通风橱内进行,多余的SO2一律排到室外
A.①③④ B.①②③
C.②③④ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.常温下,将除去表面氧化膜的Al、Cu片放入U形管作原电池的两极,测得图1所示原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。

(1)0~t1时,原电池的负极是Al片,此时,正极的电极反应式是________。溶液中的H+向________(填“正”或“负”)极移动。
(2)t1时,原电池中电子流动方向发生改变,其原因是________。
Ⅱ.下图所示电化学装置中,a为足量的电解质溶液,X、Y是两块电极板。

请回答:
(3)若X、Y都是石墨电极,a是含有酚酞的饱和NaCl溶液,则在X电极附近观察到的现象是________,检验Y电极上反应产物的化学方法及实验现象是________,电解池总反应的离子方程式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体粉末X中可能含有K2SO4、(NH4)2CO3、K2SO3、NaNO3、Cu2O、FeO、Fe2O3中的若干种。某同学为确定该固体粉末的成分,取X进行如下实验,实验过程及现象如下图所示。该同学得出的结论正确的是
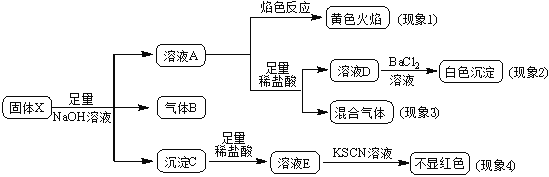
已知:Cu2O+2H+= Cu2++Cu+H2O
A.根据现象1可推出该固体粉末中一定含有NaNO3
B.根据现象2可推出该固体粉末中一定含有K2SO4
C.根据现象3可推出该固体粉末中一定含有K2SO3
D.根据现象4可推出该固体粉末中一定没有Fe2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com