
科目: 来源: 题型:
【题目】在某种强碱性的无色透明溶液中,下列一定能大量共存的离子组是( )
A. K+、AlO2-、Cl-、NO3-
B. MnO4—、SO32-、K+、Cl-
C. Ba2+、CO32-、Cl-、K+
D. HCO3-、K+、SO42—、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式书写正确的
A. 甲烷的燃烧热为-890 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+ 2H2O(g)△H=-890 kJ/mol
B. 在一定条件下将1 molSO2和0.5molO2置于密闭容器中充分反应,放出热量79.2kJ,则反应的热化学方程式为:2SO2(g)+O2(g)![]() 2SO3(g) △H=-158.4kJ·mol-1
2SO3(g) △H=-158.4kJ·mol-1
C. NaOH(s)+1/2H2SO4(浓)=1/2Na2SO4(aq)+H2O(l) △H=-57.3kJ·mol-1
D. 2.00gC2H2气体完全燃烧生成液态水和二氧化碳气体放出99.6kJ的热量,该反应的热化学方程式为:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2589.6kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】2.3g 纯净金属钠一定条件下在干燥空气中被氧化后得到 3.5g 固体,由此判断其产物是 ( )
A.氧化钠 B.过氧化钠 C.氧化钠和过氧化钠 D.无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】下列坐标图均涉及平衡原理,其中相关表述正确的是

A.图①表示室温下,用0.1mol·L-1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示2SO2(g)+O2(g) ![]() 2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
C.图③表示反应2NH3(g) ![]() 3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D.图④表示AgCl(s) ![]() Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。下列说法正确的是 ( )

A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为rX>rY>rZ>rW>rQ
C. 离子Y2-和Z3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物酸性比Q的强
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.碳酸钙与盐酸混合:2H++CO32-=CO2↑+H2O
B.Al投入NaOH溶液中:Al+OH-+H2O=AlO2-+H2↑
C.亚硫酸钠溶液与稀硫酸混合:2H++SO32-=SO2↑+H2O
D.二氧化锰与浓盐酸混合后加热:MnO2+4H++4Cl-=MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】1、根据下面的反应路线及所给信息填空。

(1)A的结构简式是_______,B的结构简式是______________。
(2)反应④所用的试剂和条件是__________。该反应的类型为_________________。
(3)反应⑥的化学方程式是______________。
II.已知烯烃与苯在一定条件下反应生成芳香烃,如:

丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途。
(1)写出丙烯在一定条件下发生聚合反应的化学方程式________________。
(2)丙烯与苯在一定条件下反应可生成M、N等多种芳香烃。红外光谱、核磁共振是研究机物结构的重要方法,根据下列数据,写出M,N的结构简式。
M:元素组成:C89.94%、H 10.06%;1H核磁共振有5个信号。
N:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号。
M:_____,N:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】
反应原理:
反应物与产物的物理性质:
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)实验过程中可能发生的有机副反应的方程式为________________________________。
(2)根据上述资料,装置__________最适宜用来完成本次制备实验。



A B C
(3)制备粗产品
将5 mL________加入试管A中,再加入l0 mL_______,摇匀后放入碎瓷片,缓慢加热至反应完全。
(4)粗产品提纯
①环己烯粗产品中含有环己醇和少量酸性杂质等。粗产品需依次经过水洗,加碳酸钠溶液洗涤以及第二次水洗。在此过程中加入碳酸钠溶液的目的是_____________;分液时,环己烯应从分液漏斗的_____(填“上”或“下”)口取出。
②向水洗后的环己烯中加入少量的无水氯化钙,再将混合物放入右图所示装置的____________(填仪器名称)中,进行蒸馏,收集产品时,温度计显示的温度应为 。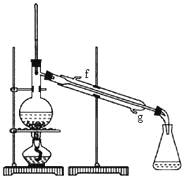
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com