
科目: 来源: 题型:
【题目】分某化学兴趣小组在实脸室模拟侯德榜制碱法制备纯碱。主要步骤如下:
第一步:配制饱和NaCl溶液,倒入烧杯中加热;
第一步:控制温度在30-35 ℃。边搅拌边分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟;
第三步:静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质,然后抽干;
第四步:将第二步所得固体转入蒸发皿中,灼烧2小时,制得纯碱固体,
已知:温度高于35℃时,NH4HCO3会分解。有关盐的溶解度(g/100g水)如下表:
盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —— | —— | —— | —— |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.l | 12.7 | 14.5 | 16.4 | —— |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
回答下列问题:
(1)反应温度控制在30-35℃范围内,应采取的加热方法为 ,反应温度不能高于35℃的理由是 .
(2)第三步静置后析出NaHCO3晶体的原因是 ;用蒸馏水洗涤NaHCO3晶体的目的是除去杂质粒子 (用离子符号表示)。
(3)若向过滤所得母液中加入 (填写试剂名称),并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)纯碱产品不纯,含有NaHCO3、NaCl等杂质。测定纯碱中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加l-2滴酚酞指示剂,用物质的量浓度为cmol/L的盐酸滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点), 所用盐酸体积为V1mL,再加1-2滴甲基橙指示剂,继续用盐酸滴定至溶液由黄变橙,所用盐酸总体积为V2mL。
① 实验室配制一定体积cmol/L盐酸需用的仪器除了容量瓶、烧杯、量筒外还需 ;在容量瓶的使用方法中,下列操作正确的是 (填写标号)
a.使用容量瓶前检验它是否漏水
b.容量瓶用蒸馏水洗净后,再用待配溶液润洗
c.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中.然后加蒸馏水定容
d.用容量瓶把溶液配制完成以后.直接贴上标签,放置备用
e.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次
② 写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)= 。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示(B中冷却装置未画出),将氯气和空气(不参与反应)以体积比约1∶3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O制备次氯酸溶液。
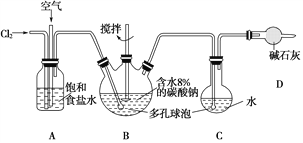
已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。
(1)①实验中控制氯气与空气的体积比的方法是___________________________________。
②使用多孔球泡的作用是_____________________________________。
(2)①装置B中产生Cl2O的化学方程式为____________________________________。
②若B无冷却装置,进入C中的Cl2O会大量减少。其原因是___________________________。
(3)装置C中采用棕色圆底烧瓶是因为________________________________。
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定C中所得次氯酸溶液的物质的量浓度的实验方案:用_________量取20.00 mL次氯酸溶液于烧杯中,_____________________________。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。除常用仪器外须使用的仪器有:电子天平,真空干燥箱)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,由相同种类元素组成的是
A. 胆固醇、脂肪酸、脂肪酶 B. 性激素、生长激素、胰岛素
C. 氨基酸、核苷酸、丙酮酸 D. 淀粉、半乳糖、糖原
查看答案和解析>>
科目: 来源: 题型:
【题目】氢化铝锂(LiAlH4)是有机合成中非常重要的还原剂。纯的氢化铝锂是白色晶状固体,不溶于烃类,溶于乙醚;在120°C以下干燥空气中相对稳定,但遇水即爆炸性分解。某课题组同学查阅资料,设计如下流程合成氢化铝锂:

请回答下列问题:
(1)氢化铝锂遇水发生剧烈反应,写出氢化铝锂与水反应的化学方程式:____________________。
(2)研究小组甲同学拟用图I装置在实验室中制取无水氯化铝。

①若选用A装置制取氯气,可以选用的药品是_________(填编号),反应的离子方程式为_______________________________。
A.浓盐酸+KMnO4 B.浓盐酸+MnO2
C.浓盐酸+KClO3 D.Ca(ClO)2+浓盐酸
②反应开始时,应该先点燃____________处(填“A”或“D”)酒精灯;直至观察到___________________________,再点燃另一处酒精灯。
③图中装置E的作用是________________________________。
(3)研究小组乙同学准确称量a g样品置于烧瓶中,利用图II装置测量样品与水反应生成的气体体积,计算氢化铝锂的纯度;试分析其方案是否合理____________(填“合理”或“不合理”),若不合理请说出理由_______________________________________(若合理,本空不需作答)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有含少量KCl、K2SO4、KgCO3杂质的KNO3溶液,除去杂质,得到纯净KNO3固体的实验流程如图所示。

已知:KNO3固体受热易分解。
(1)沉淀A的主要成分是_______(填化学式)。
(2)过程②中进行的实验操作是__________。
(3)过程③中加入过量K2CO3溶液的目的是_________。
(4)为了除去溶液3中的杂质,可向其中加人适量的_______,而后获得KNO3晶体的操作是_____、______、过滤。
查看答案和解析>>
科目: 来源: 题型:
【题目】在任何条件下,纯水显中性,这是因为 ( )
A、PH=7 B、c(H+)=c(OH-)
C、c(H+)=c(OH-)=10-7mol/L D、c(H+)×c(OH-)=10-14
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值。下列说法不正确的是
A. 2g氢气中所含的分子数为NA
B. 32gSO2中所含的氧原子数为NA
C. 0.5L1mol/LCaCl2溶液中所含的氯离子数目为NA
D. 标准状况下,22.4LH2O中所含的分子数为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】高氯酸铵(NH4ClO4)为白色晶体,具有不稳定性,在400 ℃时开始分解产生多种气体,常用于生产火箭推进剂。某化学兴趣小组同学利用下列装置对NH4ClO4的分解产物进行探究。(假设装置内药品均足量,部分夹持装置已省略。)
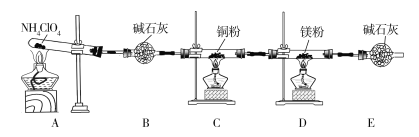
(1)在实验过程中发现C中铜粉由红色变为黑色,说明产物中有____________(填化学式)生成。
(2)实验完毕后,取D中硬质玻璃管中的固体物质于试管中,滴加蒸馏水,产生能使湿润的红色石蕊试纸变蓝色的气体,产生该气体的化学方程式为______________。
(3)通过上述实验现象的分析,某同学认为产物中还应有H2O,可能有Cl2。该同学认为可能有Cl2存在的理由是_________________________________。
(4)为了证明H2O和Cl2的存在,选择上述部分装置和下列提供的装置进行实验:
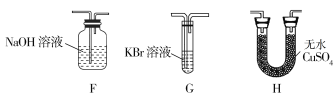
①按气流从左至右,装置的连接顺序为A→________→________→________。
②实验结束后发现G中液体变为橙黄色,用必要的文字和方程式解释出现该现象的原因:________________________。
③F中发生反应的离子方程式为___________________________。
(5)实验结论:NH4ClO4分解时产生了上述几种物质,则高氯酸铵分解的化学方程式为________________________________________________。
(6)在实验过程中仪器E中装有碱石灰的目的是________________;实验结束后,某同学拟通过称量D中镁粉质量的变化,计算高氯酸铵的分解率,会造成计算结果__________(填“偏大”“偏小”或“无法判断”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com