
科目: 来源: 题型:
【题目】如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2 . 回答下列问题: 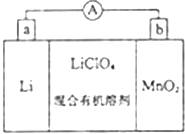
(1)外电路的电流方向是由极流向极.(填字母)
(2)电池正极反应式为 .
(3)是否可用水代替电池中的混合有机溶剂?(填“是”或“否”)原因是 .
查看答案和解析>>
科目: 来源: 题型:
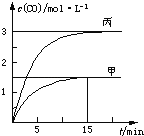
【题目】一定条件下存在反应C(s)+H2O(g)![]() CO(g)+H2(g) ΔH>0,向甲、乙、丙三个恒容容器中加入一定量C 和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
CO(g)+H2(g) ΔH>0,向甲、乙、丙三个恒容容器中加入一定量C 和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1℃ | T2℃ | T1℃ |
起始量 | 2 mol C 1 mol H2O | 1 mol CO 1 mol H2 | 4 mol C 2 mol H2O |
A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L1·min1
B.丙容器的体积V<0.5 L
C.当温度为T1℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2
查看答案和解析>>
科目: 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(1)对于反应:2SO2(g)+O2(g)2SO3(g);如果反应速率υ(SO2)为0.05molL﹣1min﹣1 , 则υ(O2)=;υ(SO3)= .
(2)已知:2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1
2NO(g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1
则反应NO2(g)+SO2(g)SO3(g)+NO(g)的△H=kJmol﹣1 .
(3)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a、体系压强保持不变
b、混合气体颜色保持不变
c、SO3和NO的体积比保持不变
d、每消耗1mol SO3的同时生成1mol NO.
查看答案和解析>>
科目: 来源: 题型:
【题目】【2016沧州模拟】在一定条件下,反应X(g)+3Y(g)2Z(g)△H=﹣92.4kJmol﹣1,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
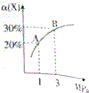
A.图中A、B两点,达到相同的平衡体系
B.上述反应在达到平衡后增大压强,X的转化率提高
C.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
D.将1.0molX,3.0molY,置于1L密闭容器中发生反应,放出的热量为92.4kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是
A.CuCl2 [H2O]B.NaOH [NaOH]C.NaCl [Cl2]D.CuSO4 [CuO]
查看答案和解析>>
科目: 来源: 题型:
【题目】将纯水加热到较高温度时,下列叙述正确的是
A.水的离子积变大、pH变小、呈酸性
B.水的离子积不变、pH变大、呈中性
C.水的离子积变小、pH变小、呈碱性
D.水的离子积变大,pH变小、呈中性
查看答案和解析>>
科目: 来源: 题型:
【题目】在溶液中能大量共存的离子组是
A.Na+、OH-、HCO3-、SO42-
B.Cl-、Ba2+、NO3-、K+
C.Al3+、SO42-、HCO3-、I-
D.OH-、NO3-、NH4+、Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】某可逆反应正向反应过程中能量变化如图所示,下列说法正确的是
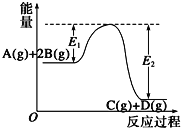
A.该反应为吸热反应
B.当反应达到平衡时,降低温度,A的转化率减小
C.升高温度,平衡常数K增大;压强增大,平衡向正反应方向移动
D.加入催化剂,反应速率增大,E1减小,E2减小,反应热不变
查看答案和解析>>
科目: 来源: 题型:
【题目】500mL 1mol/l稀盐酸与锌粒反应,不会使反应速率加快的是
A.升高温度
B.将500mL 1mol/L的盐酸改为1000mL 1mol/L的盐酸
C.用1mol/L的硫酸代替1mol/L的盐酸
D.用锌粉代替锌粒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com