
科目: 来源: 题型:
【题目】常温时,1 mol/L的HClO2和,1 mol/L的HMnO4两种酸溶液,起始时的体积均为Vo,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是 ( )

A. 稀释前分别用1mol·L-1的NaOH溶液中和,消耗的NaOH溶液体积:HMnO4>HClO2
B. 当稀释至pH均为3时,溶液中c(ClO2-)>c(MnO4-)
C. 在0≤pH≤5时,HMnO4溶液满足,pH= ![]()
D. 常温下,浓度均为0.1mol·L-1的NaClO2和NaMnO4溶液的pH: NaMnO4>NaClO2
查看答案和解析>>
科目: 来源: 题型:
【题目】苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指
A.甲烷B.乙烯C.乙炔D.生长素
查看答案和解析>>
科目: 来源: 题型:
【题目】高温高压下,1L密闭容器中,发生如下反应:2H2+COCH3OH.反应开始时H2的物质的量为5mol,5min时变为0.5mol,则5min内该反应的平均反应速率v(H2)(单位:molL﹣1min﹣1)为( )
A.9.0
B.0.9
C.0.45
D.4.5
查看答案和解析>>
科目: 来源: 题型:
【题目】α-氯乙基苯是一种重要的有机合成中间体,其一种制备反应原理为:

在T℃时,向2.0 L恒容密闭容器中充入0.40mol乙苯(g)和0.40mol Cl2(g)进行反应,反应过程中测定的部分数据见下表:
t/min | 0 | 1 | 2 | 5 | 10 |
n(HCl)/mol | 0 | 0.12 | 0.20 | 0.32 | 0.32 |
下列有关说法正确的是 ( )
A. 反应在0~2 min内的平均速率v(α-氯乙基苯)=0.10mol·L-1·min-1
B. 10 min后,若保持其他条件不变,升高温度,达到新平衡时测得c(α-氯乙基苯)=0.18mol·L-1,则反应的ΔH<0
C. 在T℃时,起始时若向容器中充入1.0 mol乙苯(g)、0.50 mol Cl2(g)和0.50 mol α-氯乙基苯(g)、0.50 mol HCl(g),则反应将向正反应方向进行
D. 在T℃时,起始时若向容器中充入2.0mol α-氯乙基苯(g)和2.2mol HCl(g),达到平衡时,α-氯乙基苯(g)的转化率小于20%
查看答案和解析>>
科目: 来源: 题型:
【题目】图为番茄电池的示意图,下列说法正确的是( ) 
A.电流由锌通过导线流向铜
B.负极反应为Zn﹣2e﹣=Zn2+
C.一段时间后,铜片质量会减少
D.一段时间后,锌片质量会增加
查看答案和解析>>
科目: 来源: 题型:
【题目】反应4A(s)+3B(g)![]() 2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是
2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是
A.用A表示的反应速率是0.8 mol·L-1·s-1
B.分别用B、C、D表示反应的速率,其比值是3∶2∶1
C.在2 min末时的反应速率,用反应物B来表示是0.3 mol·L-1·min-1
D.在这2 min内用B和C表示的反应速率的值都是相同的
查看答案和解析>>
科目: 来源: 题型:
【题目】将9.6g铜单质置于200mL一定浓度的稀硝酸中,两者恰好完全反应.假定溶液体积不变,请回答下列问题:(要求写出计算过程) 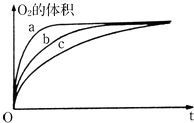
(1)反应生成的气体的体积(标况下);
(2)反应过程中转移电子的物质的量;
(3)参加反应的稀硝酸的物质的量浓度.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列除去杂质的方法中,正确的是
A.除去铜粉中混有的铁:加足量稀硝酸,过滤
B.除去N2中少量的CO2通过足量灼热的CuO粉末
C.除去CO2中的少量的HCl:通过足量的饱和碳酸氢钠溶液
D.除去KCl溶液中的少量CaCl2:加适量Na2CO3溶液,过滤
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示与对应叙述相符的是( )

A. 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图1可确定首先沉淀的是A-
B. 图2表示反应中某反应物的正、逆反应速率随温度变化情况,由图可知该反应的正反应是吸热反应
C. 一定条件下,X和Y反应生成Z,由图3推出该反应的方程式可表示为:X + 3Y![]() Z
Z
D. 图4表示溶液中反应:I2 + I- I3- 平衡c(I3-) 随温度变化,反应速度v(正)M>v(逆)N
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学学习了化学反应速率后,联想到曾用H2O2制备氧气,于是设计了下面的实验方案并进行实验探究.
实验编号 | 反应物 | 催化剂 |
甲 | 试管中加入3mL 2%H2O2溶液和3滴蒸馏水 | 无 |
乙 | 试管中加入3mL 5%H2O2溶液和3滴蒸馏水 | 无 |
丙 | 试管中加入3mL 5%H2O2溶液和3滴蒸馏水 | 1mL 0.1mol/L FeCl3溶液 |
丁 | 试管中加入3mL 5%H2O2溶液和3滴稀盐酸溶液 | 1mL 0.1mol/L FeCl3溶液 |
戊 | 试管中加入3mL 5%H2O2溶液和3滴NaOH溶液 | 1mL 0.1mol/L FeCl3溶液 |
【查阅资料】过氧化氢(H2O2),其水溶液俗称双氧水,常温下是一种无色液体,性质比较稳定.在加热的条件下,它能分解生成氧气.研究表明,将新制的5%的H2O2溶液加热到65℃时就有氧气放出,加热到80℃时就有较多氧气产生.
(1)上述实验发生反应的化学方程式为 .
(2)实验甲和实验乙的实验目的是;实验丙、实验丁和实验戊的实验目的是 .
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的?
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如表.
时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
气体体积/mL | 实验丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
实验丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
实验戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
①对实验戊,0~20s的反应速率v1=mL/s,100~120s的反应速率v2=mL/s.不考虑实验测量误差,二者速率存在差异的主要原因是 .
②如图是根据实验收集到最大体积的气体时所用时间绘制的图象.曲线c表示的是实验(填“丙”、“丁”或“戊”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com