
科目: 来源: 题型:
【题目】已知NO和O2转化为NO2的反应机理如下:
①2NO(g)![]() N2O2(g)(快) △H1<0 平衡常数 K1
N2O2(g)(快) △H1<0 平衡常数 K1
②N2O2(g)+O2(g) ![]() 2NO2化) (慢) △H2<0 平衡常数K2
2NO2化) (慢) △H2<0 平衡常数K2
下列说法正确的是
A. 2NO(g) +O2(g)![]() 2NO2(g)的△H= -(△H1+△H2)
2NO2(g)的△H= -(△H1+△H2)
B. 2NO(g) +O2(g)![]() 2NO2 (g)的平衡常数 K =
2NO2 (g)的平衡常数 K =![]()
C. 反应②的速率大小决定2NO(g)+O2(g) ![]() 2NO2(g)的反应速率
2NO2(g)的反应速率
D. 反应过程中的能量变化可用下图表示

查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 食用植物油混有较多的水分,用蒸发的操作除去水分
B. 食用药酒是利用了萃取分液操作制作而成
C. 海水晒盐是利用了蒸发结晶的原理
D. 石油工业中利用蒸馏的原理在80~150℃收集馏出液获得汽油,汽油是纯净物
查看答案和解析>>
科目: 来源: 题型:
【题目】25 °C时,将1.0 L WmolL-1的CH3COOH溶液与0.1 mol NaOH固体混合,充分反应后向混合液中通(加)入HC1气体或NaOH固体,溶液pH随加入HC1或NaOH的物质的量的变化如图所示。下列叙述正确的是
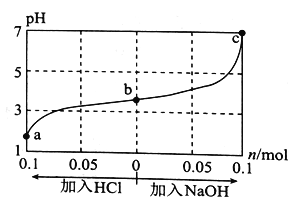
A. a、b、c对应的混合液中,水的电离程度由大到小的顺序是,a>b>c
B. c点混合液中:c(Na+)>c(CH3COO-)
C. 加入NaOH过程中,![]() 的值减小
的值减小
D. 若忽略体积变化,则25 °C时CH3COOH的电离常数 K=![]() ×10-7 molL-1
×10-7 molL-1
查看答案和解析>>
科目: 来源: 题型:
【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、CO、SO2等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。
Ⅰ.CO可用于合成甲醇
(1)已知CO、H2、CH3OH(g)的燃烧热△H分别为:-283.0kJ/mol、-285.8 kJ/mol、-764.5kJ/mol,则CO(g)+2H2(g)![]() CH3OH(g)的△H=________。
CH3OH(g)的△H=________。
(2)将lmolCO和2molH2充入密闭容器中发生上述反应。其他条件相同时.CO的平衡转化率与压强(P)和温度(T)的关系如图所示。
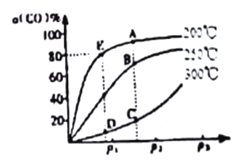
① A、B两点CH3OH的质量分数ω(A)_____ω(B )(填“>”、“<”或“=”)。
② C、D两点的逆反应速率:v(C)_____v(D)(同上)。
③ 200℃ 时,测得E点的容器容积为10L。该温度下,反应的平街常数K=_______;保持温度和容积不变,再向容器中充入lmolCO、lmolH2和xmolCH3OH时,若使v正>v逆,则x的取值范围为________。
Ⅱ. CO2的综合利用
(3)CO2转化为甲醇有广泛应用前景。T℃时,在容积为lL的恒容密闭容器中,充入lmolCO2和3molH2,发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0,达到平衡状态,其它条件不变,下列措施中能使
CH3OH(g)+H2O(g) △H<0,达到平衡状态,其它条件不变,下列措施中能使![]() 增大的是______(填选项字母)。
增大的是______(填选项字母)。
A.升高温度 B.再充入1molCH3OH(g)和1molH2O(g)
C.加入催化剂 D.再充入一定量H2O
Ⅲ.(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_____,阴极的电极反应式是_____________。
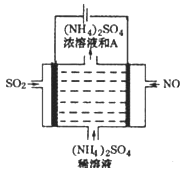
查看答案和解析>>
科目: 来源: 题型:
【题目】铝是一种重要金属,从铝土矿(主要成分为Al2O3 , Fe2O3、SiO2等)中冶炼Al的工业生产流程如下图: 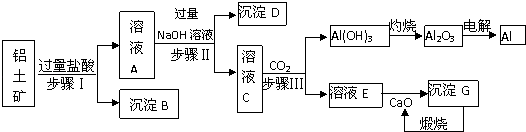
(1)溶液A中含的阳离子主要有 .
(2)写出步骤II生成溶液C 的离子方程式 ,
步骤I、II、III都要用到的分离方法是 .
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有(填化学式).
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:
.
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)(用含a、b的最简式表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,下列溶液的微粒浓度关系正确的是
A. pH = 5的H2C2O4溶液中: c(H+) = c(HC2O4-) = 1×10-5mol·L-1
B. 氨水稀释10倍后,其c(OH-)大于原来的![]()
C. pH之和为14的 H2S与NaOH 溶液混合:c(Na+)+c(H+) = c(OH-)+c(HS-)
D. (NH4)2SO4溶液和NaOH溶液混合所得的中性溶液中:c(Na+)< c(NH3 H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】—定温度下,将2 mol SO2和1mol O2充入10 L恒容密闭容器中,发生反应2SO2(g) +O2(g)![]() 2SO3(g) △H =-196 kJ mol-1。5 min时达到平衡,测得反应放热166. 6 kJ。下列说法错误的是
2SO3(g) △H =-196 kJ mol-1。5 min时达到平衡,测得反应放热166. 6 kJ。下列说法错误的是
A. 0~5 min内,用O2表示的平均反应速率V(O2)=0.017 mol·L-1·min-1
B. ![]() 的值不变时,该反应达到平衡状态
的值不变时,该反应达到平衡状态
C. 若增大O2的浓度,SO2的转化率增大
D. 条件不变,若起始时充入4 mol SO2和2 mol O2,平衡时放出的热量小于333.2 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】I.高铁酸钾(K2FeO4)具有很强的氧化性,在生产,生活中有广泛应用。
(1)K2FeO4常用做高效水处理剂,其两种作用分别是_____。
(2)制备K2FeO4可以采用湿式氧化法,流程如图:
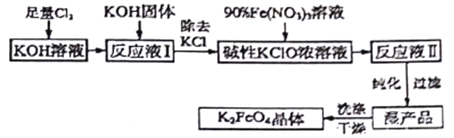
己知:① 温度较低时,Cl2通入KOH溶液生成次氯酸盐;温度较高时,Cl2通入KOH溶液生成氯酸盐;② Fe(NO3)3溶液与KClO溶液在强碱性环境中生成K2FeO4。请回答下列问题:
① 该生产工艺应在_____(填“温度较高”或“温度较低”)的情况下进行。
② 写出产生K2FeO4的离子方程式_________。
(3)实验室模拟工业电解法制取K2FeO4,装置如图.

①此装置中电源的负极是______(填“a”或“b”).
②阳极的电极反应式为______.
II.常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因_____________(用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+)_____(填“>”、“<”或“=”)0.1mol/LNaOH溶液中由水电离出的c(H+)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com