
科目: 来源: 题型:
【题目】下列说法错误的是( )
A.含有共价键的化合物是共价化合物
B.含有极性键的分子可能是非极性分子
C.有电子转移的反应是氧化还原反应
D.水溶液中能完全电离的电解质是强电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
I.拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为________(填字母序号)。
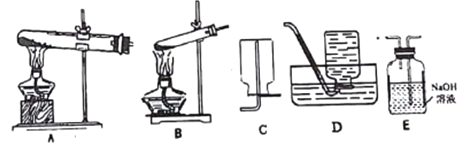
Ⅱ.设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH>7;
C. 室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL
Ⅲ.医学上常用酸性KMnO4溶液和草酸(H2C2O4)溶液反应来测血液中血钙的含量。测定方法是:取2mL血液用蒸馏水稀释后.向其中加入足量的(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解沉淀时______(填“能”或“不能”)用稀盐酸,原因是_________。
②滴定时,用______(填“酸”或“碱”)式滴定管装KMnO4溶液,滴定达到终点的现象是______。
③ 滴定过程中发生的离子反应方程式______________。
④ 若上述滴定中消耗了1.0×10-4mol/LKMnO4的溶液20mL,则200mL该血液中含钙_____g。
⑤ 下列操作会引起测定结果偏高的是__________(填序号)
A.滴定管在盛装KMnO4溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液冲洗
查看答案和解析>>
科目: 来源: 题型:
【题目】S2Cl2和SCl2均为重要的化工原料。
已知:I.S2(l) + Cl2(g)![]() S2Cl2(g) ΔH1;
S2Cl2(g) ΔH1;
II. S2Cl2 (g) +Cl2 (g)![]() 2SCl2 (g) ΔH2;
2SCl2 (g) ΔH2;
III.相关化学键的键能如下表所示:
化学键 | S—S | S—Cl | Cl—Cl |
键能/kJ mol-1 | a | b | c |
请回答下列问题:
(1) SCl2的结构式为______________________。
(2)若反应II正反应的活化能E=dkJ·mol-1,则逆反应的活化能E2=_______kJ·mol-1(用含a、b、c、d的代数式表示)。
(3)—定压强下,向10 L密闭容器中充入1molS2Cl2和1mol Cl2,发生反应II。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图所示:
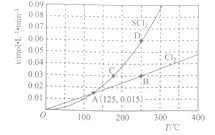
①A、B、C、D四点对应状态下,达到平衡状态的有 ____________(填字母),理由为__________。
②ΔH2_______________0(填“>” “<” 或“=”)。
(4)已知:ΔH1<0。向恒容绝热的容器中加入一定量的S2(l)和Cl2(g),发生反应I,5 min时达到平衡。则3 min时容器内气体压强__________(填“>” “<” 或“=”)5 min时的压强。
(5)—定温度下,在恒容密闭容器中发生反应I和反应II,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率_________(填“增大”“减小”或“不变”),理由为_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、氮、钛、钻、钙等多种化学物质。
请回答下列问题:
(1) 区分晶体硼和无定形硼最可靠的科学方法为___________。第二周期元素的电负性按由小到大的顺序排列,B元素排在第__________位,其基态原子价层电子的电子云轮廊图为 _______________。
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为____________,Si原子的杂化类型为__________________。
(3) N元素位于元素周期表_____________区;基态N原子中,核外电子占据最高能级的电子云有______伸展方向。

(4)[Co(NH3)6]3+的几何构型为正八面体形,Co在中心。
①[Co(NH3)6]3+中,1个Co提供_______________个空轨道。
②若将[Co(NH3)6]3+中的两个NH3分子换成两个Cl-,可以形成_____________种不同的结构形式。
(5)—种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。
①与Ti紧邻的Ca有___________________个。
②若Ca与O之间的最短距离为α pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=______g· cm-3(用含α、NA的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 蒸馏操作中若实验中途发现未添加碎瓷片,应立即补加
B. 点燃可燃气体前必须验纯
C. 不慎将浓碱溶液沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液
D. 蒸发皿在加热时应均匀加热再集中加热
查看答案和解析>>
科目: 来源: 题型:
【题目】用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是 ( ) 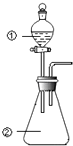
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀硫酸 | 硝酸亚铁溶液 | 无明显现象 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生大量白色沉淀 |
D | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关晶体的叙述正确的是
A.金属晶体含有金属阳离子和自由电子
B.原子晶体一定是单质
C.分子晶体一定是化合物
D.金属晶体的硬度>原子晶体的硬度>分子晶体的硬度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com