
科目: 来源: 题型:
【题目】“绿色化学”对化学反应提出了“原子经济性”(原子节约)的概念及要求。理想的原子经济性反应中原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合“绿色化学”的是( )
A. 以苯和乙醇为原料,在一定条件下生产乙苯
B. 利用乙烷与氯气反应,制备氯乙烷
C. 乙烯与氧气在银的催化作用下生成环氧乙烷(结构简式如图)
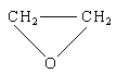
D. 乙醇与浓硫酸共热制备乙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且可以再生。下列最有希望的新能源是
①天然气 ②煤 ③石油 ④太阳能 ⑤氢能 ⑥风能
A.①③⑤B.②③④C.①④⑤⑥D.④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是某种有机物分子的球棍模型图,图中的“棍”代表单键或双键,不同大小的“球”代表不同的短周期元素的原子,对该有机物的叙述不正确的是( ) 
A.该有机物可能的分子式为C2HCl3
B.该有机物可以由乙炔和氯化氢加成反应得到
C.该有机物分子中的所有原子在一个平面上
D.该有机物分子中一定有碳碳双键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质性质的比较中,正确的是
①沸点:H2O>HCl>HF ②密度:四氯化碳>水>汽油
③酸性:H3PO4>H2SO4>HClO4④离子半径:O2->F->Na+
A.①③B.②④C.①④D.②③
查看答案和解析>>
科目: 来源: 题型:
【题目】Cl2是一种常用的自来水消毒剂,高铁酸钾(K2FeO4)是一种新型,高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.
Ⅰ:下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)装置B中饱和食盐水的作用是____________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象__________________________。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入__________。
a | b | c | d | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
II | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
II:制备高铁酸钾的方法有干法和湿法。
(3)干法制备高铁酸钾的主要反应为:
2FeSO4+ 6Na2O2= 2Na2FeO4+ 2Na2O + 2Na2SO4+ O2↑
①该反应中的还原剂是_______,每生成lmolNa2FeO4转移____个电子。
②简要说明K2FeO4作为水处理剂时所起的作用________________________________,
(4)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】控制适合的条件,KI溶液过量,将反应2Fe3++2I-![]() 2Fe2++I2设计成如下图所示的原电池。下列判断正确的是( )
2Fe2++I2设计成如下图所示的原电池。下列判断正确的是( )
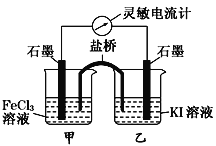
A. 反应开始时,甲中石墨电极为负极,发生氧化反应
B. 反应开始时,乙中石墨电极的反应式:I2+2e- = 2I-
C. 电流计读数为零时,在甲中加入KSCN溶液,出现血红色
D. 电流计读数为零时,反应处在停止状态
查看答案和解析>>
科目: 来源: 题型:
【题目】(13分)卤水中含有丰富的镁离子,可制取多种含镁产品。
(1)向卤水中加入Ca(OH)2制取Mg(OH)2,其离子方程式是 。
(2)Mg(OH)2可制取MgO,进而制得金属镁。
①灼烧Mg(OH)2得到MgO的化学方程式是______。
②1200℃,真空条件下用硅铁(含硅单质95~99%)将MgO还原为镁蒸汽(铁不参与反应),其原理可用化学方程式表示为______。
(3)Mg(OH)2可用来制取MgCl2,进而制取金属镁。
①从MgCl2溶液得到MgCl26H2O的操作是______、过滤。
②MgCl26H2O与SOCl2混合后加热,可获得无水MgCl2(已知SOCl2与水接触时迅速形成白雾,生成SO2)。得到无水MgCl2的化学方程式是______。
(4)Mg(OH)2还可用来制取三硅酸镁(xMgO3SiO2)。三硅酸镁是医疗上某抗酸药的主要成分。已知硅酸盐的化学式通常用氧化物形式表示,如石棉CaMg3Si4O12表示为3MgOCaO4SiO2。
①三硅酸镁中和胃酸的离子方程式是:xMgO3SiO2+□H+=□Mg2++□SiO2+□___
②为确定xMgO3SiO2中x值。取三硅酸镁样品0.52 g,加入0.5000 mol/LH2SO4标准液15.00 mL,充分反应后,用0.5000 mol/L的NaOH标准液滴定过量的H2SO4,消耗NaOH标准液14.00 mL。则x=______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com