
科目: 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.向硫酸铜蓝色溶液中加入BaCl2溶液:Ba2++SO42﹣═BaSO4↓
B.碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑
C.锌与盐酸的反应:Zn+2H++2Cl﹣═Zn2++2Cl﹣+H2↑
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O ![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目: 来源: 题型:
【题目】已知以下化学键的键能(kJ·mol-1):H—H:436 H—O:463 O=O:496,则热化学方程式2H2O(g)=2H2(g)+O2(g)的反应热ΔH是( )
A.-484 kJ·mol-1
B.484 kJ·mol-1
C.-242 kJ·mol-1
D.242 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于石油的说法正确的是( )
A. 石油属于可再生矿物能源 B. 石油主要含有碳、氢两种元素
C. 石油的裂化是物理变化 D. 石油分馏的各馏分均是纯净物
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于糖类、脂肪和蛋白质的说法不正确的是( )
A. 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体
B. 葡萄糖可以发生氧化反应和银镜反应,说明葡萄糖具有还原性
C. 通过盐析从溶液中析出的蛋白质仍能溶解于水
D. 脂肪能发生皂化反应,生成甘油和高级脂肪酸钠
查看答案和解析>>
科目: 来源: 题型:
【题目】假若某蛋白质分子由n个氨基酸构成,它们含有3条多肽链,则它们具有的肽键数和R 基团数分别是( )
A. n个和n个
B. n-3个和n个
C. n个和n-3个
D. n-3个和n-3个
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关构成细胞的化合物的种类和鉴别方法的叙述中,正确的是
A. 细胞中的糖分为单糖、二糖和多糖,可以用斐林试剂鉴别
B. 细胞中的脂质具有多种功能,如储存能量;脂质能被苏丹Ⅲ染成橘黄色
C. 细胞的遗传物质是DNA或RNA,用甲基绿—吡罗红试剂可以鉴定其存在和分布
D. 细胞内蛋白质种类众多,但都能与双缩脲试剂发生紫色颜色反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
(1)盛装0.2000 mol/L盐酸标准液应该用______式滴定管。(填“酸”或“碱”)
(2)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视________________。直到加入一滴盐酸后,溶液由_______________________________,即到终点。
(3)滴定操作可分解为如下几步:
①检查滴定管是否漏水;②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
④装标准溶液和待测液并调整液面(记录初读数);
⑤用蒸馏水洗涤玻璃仪器;⑥滴定操作
正确的操作顺序为:______________________。
(4)有关数据记录如下:
实验序号 | 待测定液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.60 | 20.70 |
2 | 20.00 | 6.00 | 25.90 |
3 | 20.00 | 1.40 | 23.20 |
则NaOH溶液的物质的量浓度为______mol/L。
(5)若滴定时锥形瓶未干燥,则测定结果________;若滴定前平视读数,滴定终点时仰视读数,则所测碱的浓度值________。(填“无影响”、“偏高”或“偏低”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应: CH3CH2OH (g)+aO2(g) →bX+cH2O(l) ΔH, X为下列何种物质时ΔH最小
A. CH3CHO (l) B. CH3CHO (g) C. CO(g) D. CO2(g)
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
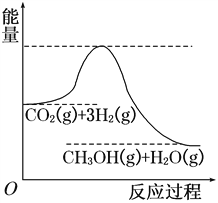
(1)上述反应平衡常数K的表达式为________________,温度降低,平衡常数K________(填“增大”、“不变”或“减小”)。
(2)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。从反应开始到5 min末,用氢气浓度变化表示的平均反应速率v(H2)=________。
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
(3)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是________(填写序号字母)。
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效催化剂
Ⅱ、(1)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,如图所示(T1、T2均大于300℃)
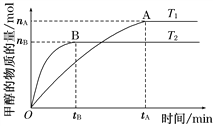
下列说法正确的是________(填序号);
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(2)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com