
科目: 来源: 题型:
【题目】磷化氢气体(PH3)是一种强烈的储粮害虫杀剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒..,请回答:
(1)用碘化磷(PH4I)和烧碱反应制取PH3的化学方程式______。
(2)实验室用硫酸铜溶液吸收PH3时的化学方程式24CuSO4+11PH3+12H2O=8Cu3P↓+3H3PO4+24H2SO4 中氧化剂是______,当吸收2.2molPH3转移电子______mol
(3)氧硫化碳(COS)可替代磷化氢而被用作熏蒸剂.粉末状的KSCN与浓硫酸在一定条件下可得到COS和两种硫酸氢盐,生成物的物质的量之比为1∶1∶1,写出相应的化学方程式______。
(4)氧硫化碳水解及部分应用流程如下(部分产物已略去):
COS![]() H2S
H2S![]() Na2S
Na2S![]() M溶液+H2
M溶液+H2
①组成氧硫化碳和磷化氢的各原子中,原子半径最大的元素在周期表中的位置是_______.
②已知M溶液中硫元素的主要存在形式为S2O32﹣,则反应Ⅲ中生成S2O32﹣的离子方程式为___.
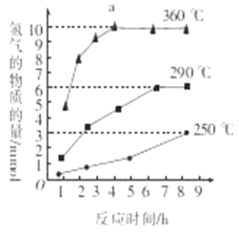
③如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系(Na2S初始含量为3mmol).由图象分析可知,a点时M溶液中除S2O32﹣外,还有____(填含硫微粒的离子符号).
查看答案和解析>>
科目: 来源: 题型:
【题目】如果Fe3+、SO42—、Al3+和M四种离子以物质的量之比为2:4:1:1共同存在于同一种溶液中,那么M可能是
A.Na+B.I-C.CO32—D.Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】把19.2g的Cu放入足量的稀硝酸中,至Cu完全反应.已知:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O求:
(1)参加反应的硝酸的物质的量是多少?
(2)反应结束后溶液加水到500ml,这时硝酸铜的物质的量浓度是多少?
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)常温下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,则溶液的pH= ;可以使0.10 mol·L-1 CH3COOH的电离程度增大的是
a.加入少量0.10 mol·L-1的稀盐酸
b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化钠固体
f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_________V(醋酸)(填“>”、“<”或“=”)。
(3)0.1mol/L的某酸H2A的pH=4,则H2A的电离方程式为 。
(4)25℃时,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸溶液的体积比为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】丙烯酰胺(H2C=CH—CONH2)具有致癌性和遗传毒性。丙烯酰胺主要是由高碳水化合物、低蛋白质的植物性食物在加热(120 ℃以上)过程中形成,特别在烘烤、油炸时更易形成。丙烯酰胺可以进一步形成在工业上有用的聚丙烯酰胺类物质。
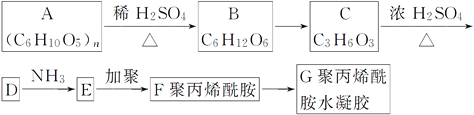
回答下列问题:
(1)D的结构简式为______________;F的结构简式为______________。
(2)指明下列反应类型:A→B____________________,C→D______________________。
(3)丙烯酰胺有多种同分异构体,写出分子中同时含有醛基和碳碳双键的同分异构体:______________________。
(4)写出化学方程式D→E:__________________________________________。2分子C在浓硫酸作用下可形成一个六元酯环,该反应的化学方程式为___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】烷烃CH3CH(CH3)CH(CH3)CH2CH(CH3)CH3是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
A. 8种 B. 6种 C. 2种 D. 1种
查看答案和解析>>
科目: 来源: 题型:
【题目】元素性质呈现周期性变化的根本原因是( )
A.元素原子电子层数增大
B.元素原子最外层电子数呈现周期性变化
C.元素的化合价呈现周期性变化
D.核电荷数依次增大
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求完成下列填空:
(1)已知在标准状况下的四种气体 ①8.96L CH4②3.01×1022个HCl分子③10.2克H2S④0.5molNH3用相应的序号填写下列空白: 体积最大的是;含氢原子数最多的是 .
(2)等物质的量的氧气与臭氧质量之比为 , 分子个数之比为 , 电子个数之比为 .
(3)某金属氯化物MCl3 26.7g,含有0.600mol Cl﹣ . 则金属M的摩尔质量为 .
(4)现有10克H218O中,中子数目为 .
(5)0.4mol NH3中所含氢原子数与g水所含氢原子数相等.
(6)0.5molSO2的质量是g,在标准状况下的体积为L;含有个氧原子.
(7)将标况下22.4L的HCl 溶于水配成200mL的溶液,所溶液的物质的量浓度为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com