
科目: 来源: 题型:
【题目】X、Y、Z、M、N五种常见短周期元素原子半径随原子序数变化如图。已知X的一种原子的质量数为18,中子数为10;Y和Ne原子的核外电子数相差1;M的单质是一种常见的半导体材料;N的原子半径在同周期主族元素中最小;Y、Z、N三种元素的最高氧化物对应水化物两两之间可发生反应。下列说法错误的是
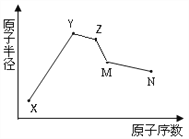
A. N、Z两种元素的离子半径相比前者较小
B. M、N两种元素的气态氢化物的稳定性相比后者较强
C. X与Y两种元素组成的一种化合物中阴、阳离子的个数比为1:1
D. 工业上用电解Y和N形成的化合物的熔融态制取Y的单质
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下:
弱酸 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)CH3COOH、H2CO3、H2SO3三种酸中酸性最弱的是__________(填化学式)。
(2)CH3COOH的电离平衡常数表达式为K=__________。
(3)写出H2CO3的第二步电离方程式:_____________。
(4)写出H2SO3溶液和CH3COONa溶液反应的离子方程式:____________________。
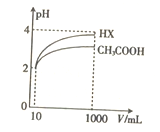
(5)将体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH的变化如图所示,则HX的电离平衡常数____________(填“大于”“ 小于”或“等于”)醋酸的电离平衡常数,理由是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1) 为测定绿矾中结晶水含量,将石英玻璃管(带端开关K1和K2) (设为装置A) 称重,记为m1g。将样品装入石英玻璃管中,再次将装置A 称重,记为m2g。按下图连接好装置进行实验。

①将下列实验操作步骤正确排序________(填标号) ;重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
②根据实验记录,计算绿矾化学式中结晶水数目x=_______(列式表示)。若实验时按a、d 次序操作,则使x_____(填“偏大”“偏小”或“无影响”)。
(2) 为探究硫酸亚铁的分解产物,将(1) 中已恒重的装置A 接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D 中的溶液依次为________(填标号)。C、D中有气泡冒出,并观察到的现象分别是_____。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用纯溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作进行提纯:
①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗,正确的操作顺序是
A. ①②③④② B. ②④②③① C. ④②③①② D. ②④①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车、飞机等交通工具排放的尾气中含有的大量CO、NO 等大气污染物,是造成雾霾天气的主要原因,研究CO、NO 的转化对于环境的改善有重大意义。
(1)有人设想将CO按下列反应除去:2CO(g)=2C(s) +O2(g) △H>0。你认为该设想能否实现并说明理由:__________________________。
(2)用活性炭还原法可以处理汽车尾气中的氮氧化物。某研究小组在2 L的恒容密闭容器中加人0.100 mL NO 和2.030 mol固体活性炭,发生反应:C(s)+2NO(g) ![]() N2(g)+CO2(g)。在不同温度下测得平衡体系中各物质的物质的量如下表:
N2(g)+CO2(g)。在不同温度下测得平衡体系中各物质的物质的量如下表:
T/℃ | n(固体活性炭)/mol | n(NO)/mol | n(N2)/mol | n(CO2)/mol |
200 | 2.000 | 0.040 | 0.030 | 0.030 |
350 | 2.005 | 0.050 | 0.025 | 0.025 |
①该反应的正反应为___________(填“吸热”或“放热”)反应。
②200℃时,反应达到平衡后向恒容容器中再充入0.100 mol NO,再次达到平衡后,混合气中NO的百分含量将__________(填“增大”“减小”或“不变”)。
③上述反应在350℃时的平衡常数K=_______________。
(3)在密闭容器中发生上述反,,达到平衡时,下列措施能提高NO转化率的是___________(填字母)。
A.选用更高效的催化剂 B.增加C(s)的量
C.降低反应体系的温度 D.缩小容器的体积
查看答案和解析>>
科目: 来源: 题型:
【题目】水泥是重要的建筑材料。水泥热料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

已知下列氢氧化物沉淀完全的pH:
Fe(OH)3 3.0 Fe(OH)2 8.35 Al(OH)3 4.7 Mg(OH)2 10.87
回答下列问题:
(1) 在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_______,还可使用______代替硝酸。
(2) 沉淀A 的主要成分是_______,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为__________________。
(3) 加氨水过程中加热的目的是_________.沉淀B 的主要成分为_______(写化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,向体积不变且相同的两个容器中,一个充入NH3,另一个充入N2与H2物质的量之比为1:3的混合气,使两个容器的压强相同。则两个容器内一定相等的是( )
A.原子数B.分子数C.质量D.密度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com