
科目: 来源: 题型:
【题目】(1)将NaHCO3溶液跟Al2(SO4)3溶液混合,相关反应的离子方程式是____________。
(2)有浓度均为0.2 mol·L-1的Na2CO3溶液与NaHCO3溶液,试回答下列问题:
①微粒种类:Na2CO3__________NaHCO3溶液(填“﹥”、“<”或“=”)。
②两溶液分别加入0.1 molNaOH固体,恢复到室温,Na2CO3溶液中的c(CO32-)____________(填“增大”、“减小”或“不变”);NaHCO3溶液中的c(HCO3-)_________(填“增大”、“减小”或“不变”)。
(3)常温下,甲为0.1 mol·L-1的HA溶液,pH﹥1;乙为0.1 mol·L-1的BOH溶液,且溶液中c(OH-):c(H+)=1012。请分别写出甲、乙两溶液中溶质的电离方程式:
甲__________________、乙_________________。
(4)相同条件下,对于浓度均为0.1 mol·L-1的NaCl溶液和CH3COONa溶液,溶液中的离子总数:NaCl溶液__________CH3COONa溶液(填“﹥”、“<”或“=”)。
(5)物质的量浓度相同的 ①氨水 ②氯化铵 ③碳酸氢铵 ④硫酸氢铵 ⑤硫酸铵五种溶液中c(NH4+)由大到小的顺序为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】回答下列问题:
(1)实验室有如下仪器:①试管 ②烧杯 ③量筒 ④蒸发皿 ⑤坩埚 ⑥温度计 ⑦蒸馏烧瓶,其中可以直接加热的玻璃仪器有(填序号)
(2)4.5g水与g磷酸(H3PO4)所含的分子数相等,它们所含的氧原子数之比是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应在生产和生活中使用非常广泛.
I、NaNO2外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:
2NaNO2+4HI═2NO↑+I2+2NaI+2H2O.
(1)上述反应中用单线桥标出电子转移的方向和数目.
(2)某厂废液中,含有2%~5%的NaNO2 , 直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是 .
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(3)II.过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.根据下列反应回答问题:
A.Na2O2+2HCl═2NaCl+H2O2
B.Ag2O+H2O2═2Ag+O2↑+H2O
C.2H2O2═2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
上述反应中,H2O2仅体现氧化性的反应是(填序号)
(4)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是
(5)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO4﹣、H2O、Mn2+、H2O2、H+ . 已知该反应中H2O2只发生了如下过程:H2O2→O2 .
①将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中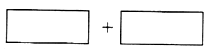
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为 mol.
查看答案和解析>>
科目: 来源: 题型:
【题目】以废旧锌锰电池初步处理分选出的废料(含MnO2、MnOOH、MnO及少量Fe、Pb等)为原料制备MnO2,实现锰的再生利用。其工艺流程如下:

已知:①Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
②金属离子(起始浓度为0.1 mol·L-1)生成氢氧化物沉淀的pH
Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.1 | 6.5 | 1.9 |
完全沉淀时 | 10.1 | 8.5 | 3.2 |
回答下列问题:
(1)酸浸过程中MnO2与浓盐酸反应的离子方程式为_____________________________。
(2)滤液①中铁以Fe3+存在,Fe2+转化为Fe3+过程中,可能发生反应的离子方程式为____________________(写出1种即可)。
(3)除铁的方法是:向滤液①中加MnCO3调节溶液pH,其范围是______________________;过滤得滤液②。
(4)将滤液③转化为MnO2的方法常用氧化法和电解法。
①氧化法的具体做法是向所得溶液中加入酸化的NaC1O3将Mn2+氧化为MnO2,该反应的离子方程式为_____________________________________。
②电解法生成MnO2的电极反应式为_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】玻璃的出现与使用已有四千多年的历史。下列说法正确的是( )
A.玻璃花纹可以用氢氟酸进行雕刻
B.有机玻璃的主要成分为硅酸钠
C.纯碱和硅单质是制取普通玻璃的主要原料
D.玻璃外观规则,属于晶体,有固定的熔点
查看答案和解析>>
科目: 来源: 题型:
【题目】铁元素存在多种硫化物,兴趣小组为测定某铁硫化物(FeaSy)的组成按下列流程进行探究:
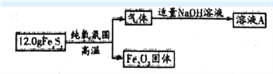
回答下列问题:
(1)测得Fe2O3固体的质量为8.0g,则FeaSy的化学式为______________。请设计实验检验Fe2O3中含有+3价铁:__________________________。
(2)铁硫化物在纯氧中发生反应的化学方程式为______________________________。
(3)兴趣小组同学推测溶液A中除含有Na2SO3外,还可能含有Na2SO4。设计实验方案并探究:
①用0.10 mol·L-1酸性KMnO4溶液应盛装在_______________(填“酸式“或“碱式”)滴定管中,然后进行滴定,反应的离子方程式为_________________________。
②确认A溶液中是否含有Na2SO4

请用化学方程式解释该方案不合理的原因____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某盐的混合物中含有0.1mol Na+、0.6mol Mg2+、0.3mol Cl-,还有SO42-,则SO42-为
A.0.1mol B. 0.5mol C.0.3 mol D.0.7mol
查看答案和解析>>
科目: 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

回答下列问题:
(1)过程I加NaOH溶液的作用是___________________________(用离子方程式表示);鼓入大量空气的目的是____________________________。
(2)已知:水体中以+l价或单质形式存在的氯元素,称为“余氯”。过程Ⅱ中加入适量液氯,控制pH在6-7,将氨氮转化为N2。实验测定氯铵比与余氯、残余NH4+的浓度关系如下图所示。

①为了完全从废水中去除氨氮,根据图像分析,投入的Cl2与NH4+的最佳比值为_________。
②过程Ⅱ分步发生3个反应:
i.Cl2+H2O =H++Cl- +HClO
ii.NH4++HClO==NH2Cl+H++H2O(NH2Cl中Cl元素为+l价)
iii.HClO继续参与反应,其离子方程式为________________________________。
③图中a点余氯浓度较大的原因是________________________________________。
(3)若含余氯废水中折合Cl2的含量是71 mg·L-1,则处理10m3含余氯废水,至少添加Na2SO3_____kg(溶液体积变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com