
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Ζ¥”Π÷–Θ§ τ”ΎΦ”≥…Ζ¥”ΠΒΡ «Θ® Θ©
A.CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
B.CH2=CH2+Br2ΓζCH2BrCH2Br
C.2C2H5OH+2NaΓζ2C2H5ONa+H2Γϋ
D.![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕΧ÷ήΤΎ‘ΣΥΊXΓΔYΓΔZΓΔW‘Ύ÷ήΤΎ±μ÷–ΒΡœύΕ‘ΈΜ÷Ο»γ”“ΆΦΘ§XΒΡ«βΜ·ΈοΡή”κΤδΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·ΈοΖ¥”Π…ζ≥…―ΈΓΘœ¬Ν–≈–Εœ’ΐ»ΖΒΡ «

A. ΉνΦρΒΞΤχΧ§«βΜ·ΈοΒΡΈ»Ε®–‘ΘΚX<Y
B. ΒΞΚΥ“θάκΉ”ΒΡΜΙ‘≠–‘ΘΚW>Z
C. Κ§Z‘ΣΥΊΒΡ―Έ»ή“ΚΩ…Ρήœ‘Υα–‘ΓΔΦν–‘Μρ÷––‘
D. YΓΔZΓΔWΒΡΚ§―θΥαΒΡΥα–‘“ά¥Έ‘ω«Ω
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ±Ϋ““ΥαΆ≠ «Κœ≥…”≈ΝΦ¥ΏΜ·ΦΝΓΔ¥ΪΗ–≤ΡΝœΓΣΓΣΡ…ΟΉ―θΜ·Ά≠ΒΡ÷Ί“Σ«Α«ΐΧε÷°“ΜΓΘœ¬Οφ «ΥϋΒΡ“Μ÷÷ Β―ι “Κœ≥…¬ΖœΏ:
![]() +H2O+H2SO4
+H2O+H2SO4![]()
![]() +NH4HSO4
+NH4HSO4
![]() + Cu(OH)2
+ Cu(OH)2![]()
![]() +H2O
+H2O
÷Τ±Η±Ϋ““ΥαΒΡΉΑ÷Ο Ψ“βΆΦ»γΆΦ(Φ”»»ΚΆΦ–≥÷ΉΑ÷ΟΒ»¬‘)ΓΘ
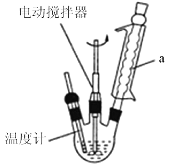
ΦΚ÷Σ: ±Ϋ““ΥαΒΡ»έΒψΈΣ76.5ΓφΘ§Ω……ΐΜΣΘ§“Ή»ή”Ύ»»Υ°Θ§ΈΔ»ή”ΎάδΥ°Θ§»ή”Ύ““¥ΦΓΘ
«κΜΊ¥πœ¬Ν–Έ Χβ:
Θ®1Θ©ΫΪΉΑ÷Ο÷–ΒΡ»ή“ΚΦ”»»÷Ν100ΓφΘ§ΜΚΜΚΒΈΦ”40g ±Ϋ““κφΒΫΝρΥα»ή“Κ÷–Θ§»ΜΚσ…ΐΈ¬÷Ν130ΓφΦΧ–χΖ¥”ΠΘ§‘ΎΉΑ÷Ο Ψ“βΆΦ÷–Θ§“«ΤςaΒΡΟϊ≥Τ «________Θ§ΤδΉς”Ο «_____________ΘΜ
Θ®2Θ©Ζ¥”ΠΫα χΚσΦ” ΝΩάδΥ°Θ§Ω…Ζ÷άκ≥ω±Ϋ““Υα¥÷ΤΖΘ§ΤδΦ”»κάδΥ°ΒΡΡΩΒΡ «____________ΘΜœ¬Ν–“«Τς÷–Ω…”Ο”ΎΖ÷άκ±Ϋ““Υα¥÷ΤΖΒΡ «_______(Χν±ξΚ≈)ΓΘ
A.Ζ÷“Κ¬©ΕΖ B.¬©ΕΖ C.…’±≠ D.÷±–ΈάδΡΐΙή E.≤ΘΝßΑτ
Θ®3Θ©»γΙϊ“ΣΫΪ±Ϋ““Υα¥÷ΤΖΫχ“Μ≤ΫΧα¥ΩΘ§Ρψ―Γ‘ώΒΡ Β―ιΖΫΖ® «___________(ΧνΕΰ÷÷ΖΫΖ®)ΓΘ
Θ®4Θ©”ΟCuCl2ΓΛ2H2OΚΆNaOH »ή“Κ÷Τ±Η ΝΩCu(OH)2≥ΝΒμΘ§≤ΔΕύ¥Έ”Ο’τΝσΥ°œ¥Β”≥ΝΒμΘ§≈–Εœ≥ΝΒμœ¥Η…ΨΜΒΡ Β―ι≤ΌΉςΚΆœ÷œσ «____________ΘΜ
Θ®5Θ©ΫΪ±Ϋ““ΥαΦ”»κΒΫ““¥Φ”κΥ°ΒΡΜλΚœ»ήΦΝ÷–Θ§≥δΖ÷»ήΫβΚσΘ§Φ”»κCu(OH)2ΫΝΑη30minΘ§Ιΐ¬ΥΘ§¬Υ“ΚΨ≤÷Ο“ΜΕΈ ±ΦδΘ§Έω≥ω±Ϋ““ΥαΆ≠ΨßΧεΘ§ΜλΚœ»ήΦΝ÷–““¥ΦΒΡΉς”Ο «____________ΘΜ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A. …ζ≥…ΈοΒΡΉήΡήΝΩ¥σ”ΎΖ¥”ΠΈοΒΡΉήΡήΝΩ ±Θ§ΓςH<0
B. ‘ΎΤδΥϊΧθΦΰ≤Μ±δΒΡ«ιΩωœ¬Θ§ Ι”Ο¥ΏΜ·ΦΝΩ…“‘ΗΡ±δΖ¥”ΠΖΫœρ
C. ΓςH<0ΓΔΓςS>0ΒΡΖ¥”Π‘ΎΒΆΈ¬ ±≤ΜΡήΉ‘ΖΔΫχ––
D. “ΜΗωΜ·―ßΖ¥”ΠΒΡΓςH÷Μ”κΖ¥”ΠΧεœΒΒΡ ΦΧ§ΚΆ÷’Χ§”–ΙΊΘ§Εχ”κΖ¥”ΠΒΡΆΨΨΕΈόΙΊ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ2020Ρξ¥ΚΫΎΤΎΦδΨΌ––ΒΡΓΕ÷–Ιζ Ϊ¥ ¥σΜαΓΖΒΎΈεΦΨΨΪ≤ ΖΉ≥ Θ§Χεœ÷ΝΥ÷–Ιζ Ϊ¥ ≤©¥σΨΪ…νΘ§œ¬Ν– Ϊ¥ Ζ÷Έω¥μΈσΒΡ «
A.ΓΑ≈ΣΖγΝχ–θ“…≥…―©Θ§¬ζΒΊ”ή«°¬ρΒΟ¥ΚΓ±÷–ΒΡΓΑΝχ–θΓ±ΚΆΟόΜ®ΒΡ≥…Ζ÷ΨυΚ§œΥΈ§ΥΊ
B.ΓΑ»’ΡΚΚΚΙ§¥Ϊά·÷ρΘ§«α―Χ…Δ»κΈεΚνΦ“Γ±÷–ΒΡΓΑά·÷ρΓ± «ΗΏΦΕ÷§ΖΨΥαθΞΘ§“≤ «ΗΏΖ÷Ή”Μ·ΚœΈο
C.ΓΑ―Ή―Ή»’’ΐΈγΘ§ΉΤΉΤΜπΨψ»ΦΓ±÷–ΒΡΓΑ―Ή―ΉΓ±Χεœ÷Ή‘»ΜΫγ÷–ΧΪ―τΡή”κ»»ΡήΒΡΉΣΜ·
D.ΓΑ÷σΕΙ≥÷ΉςΗΰΘ§δθΙΡ“‘ΈΣ÷≠Γ±÷–ΒΡΓΑδθΙΡΓ±…φΦΑΒΡΜυ±Ψ≤ΌΉς «Ιΐ¬Υ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷Σœ¬Ν–»»Μ·―ßΖΫ≥Χ ΫΘ§«“bΘΨaΓΘ
Hg(I)+![]() O2(g)===HgO(s) ΓςH=Θ≠akJΓΛmolΘ≠1
O2(g)===HgO(s) ΓςH=Θ≠akJΓΛmolΘ≠1
Zn(s)+![]() O2(g)===ZnO(s) ΓςH=Θ≠bkJΓΛmolΘ≠1
O2(g)===ZnO(s) ΓςH=Θ≠bkJΓΛmolΘ≠1
”…¥ΥΩ…÷ΣΖ¥”ΠZn(s)ΘΪHgO(s) ![]() ZnO(s)ΘΪHg(l)ΒΡλ ±δΈΣ
ZnO(s)ΘΪHg(l)ΒΡλ ±δΈΣ
A. Θ≠(bΘ≠a) kJΓΛmolΘ≠1 B. +(bΘ≠a) kJΓΛmolΘ≠1
C. (bΘ≠a) kJΓΛmolΘ≠1 D. (b+a)kJΓΛmolΘ≠1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®IΘ©Ρ≥Μ·―ß Β―ι–ΓΉιΈΣ»ΖΕ®Ιΐ―θΜ·«βΖ÷ΫβΒΡΉνΦ―¥ΏΜ·ΧθΦΰΘ§”Ο»γΆΦΉΑ÷ΟΫχ–– Β―ιΘ§Ζ¥”ΠΈο”ΟΝΩΚΆΖ¥”ΠΆΘ÷ΙΒΡ ±Φδ ΐΨί»γœ¬±μΘΚ

«κΜΊ¥πœ¬Ν–Έ Χβ:
Θ®1Θ© ΔΉΑΥΪ―θΥ°ΒΡΜ·―ß“«ΤςΟϊ≥Τ «__________ΓΘ
Θ®2Θ©»γΚΈΦλ―ιΗΟΧΉΉΑ÷ΟΒΡΤχΟή–‘__________ΓΘ
Θ®3Θ©œύΆ§≈®Ε»ΒΡΙΐ―θΜ·«βΘ§ΤδΖ÷ΫβΥΌ¬ ΥφΉ≈Εΰ―θΜ·ΟΧ”ΟΝΩΒΡ‘ωΦ”Εχ__________ΓΘ
Θ®4Θ©¥” Β―ι–ßΙϊΚΆΓΑ¬Χ…ΪΜ·―ßΓ±ΒΡΫ«Ε»ΩΦ¬«Θ§ΥΪ―θΥ°ΒΡ≈®Ε»œύΆ§ ±Θ§Φ”»κ______gΒΡΕΰ―θΜ·ΟΧΈΣΫœΦ――Γ‘ώΓΘ
Θ®5Θ©Ρ≥Ά§―ßΖ÷Έω…œ ω ΐΨίΚσ»œΈΣ:ΓΑΒ±”ΟœύΆ§÷ ΝΩΒΡΕΰ―θΜ·ΟΧ ±Θ§ΥΪ―θΥ°ΒΡ≈®Ε»‘Ϋ–ΓΘ§Υυ–η“ΣΒΡ ±ΦδΨΆ‘Ϋ…ΌΘ§“ύΦ¥ΤδΖ¥”ΠΥΌ¬ ‘ΫΩλΓ±ΒΡΫα¬έΘ§Ρψ»œΈΣ «Ζώ’ΐ»Ζ_______Θ§άμ”… «__________ΓΘ(Χα ΨΘΚH2O2ΒΡΟήΕ»Ω…»œΈΣΫϋΥΤœύΒ»)ΓΘ
(II)‘Ύ»γΆΦΥυ ΨΒΡΝΩ»»ΦΤ÷–Θ§ΫΪ100mL0.50mol/LCH3COOH»ή“Κ”κ100mL0.55mol/LNaOH»ή“ΚΜλΚœΓΘΈ¬Ε»¥”25.0Γφ…ΐΗΏΒΫ27.7ΓφΓΘ“―÷ΣΝΩ»»ΦΤΒΡ»»»ί≥Θ ΐ(ΝΩ»»ΦΤΗς≤ΩΦΰΟΩ…ΐΗΏ1ΓφΥυ–ηΒΡ»»ΝΩ) «150.5J/Γφ…ζ≥…»ή“ΚΒΡ±»»»»ίΈΣ4.184JΓΛg-1ΓΛΓφ-1,»ή“ΚΒΡΟήΕ»ΨυΫϋΥΤΈΣ1g/mLΓΘ

Θ®1Θ© ‘«σCH3COOHΒΡ÷–ΚΆ»»ΓςH=__________ΓΘ
Θ®2Θ©CH3COOHΒΡ÷–ΚΆ»»ΒΡΈΡœΉ÷ΒΈΣ56.1kJ/mol,‘ρ«κΡψΖ÷Έω‘Ύ(1)÷–≤βΒΟΒΡ Β―ι÷ΒΤΪ≤νΩ…ΡήΒΡ‘≠“ρ_____________ΓΘ
Θ®3Θ© Β―ι÷–NaOHΙΐΝΩΒΡΡΩΒΡ «_____________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΆ®»κΥ°÷–ΥυΒΟ»ή“Κ≥ Φν–‘ΒΡΤχΧε «Θ® Θ©
A.NH3
B.NO2
C.SO2
D.HCl
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈ“ΙζΙ≈¥ζΨΆ”– ΣΖ®ΝΕΆ≠ΒΡΦ«‘ΊΓΑ‘χ«ύΒΟΧζ‘ρΜ·ΈΣΆ≠Γ±Θ§Ζ¥”ΠΈΣFe+CuSO4®TCu+FeSO4 Θ° ”–ΙΊΗΟΖ¥”ΠΒΡΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.Fe «―θΜ·ΦΝ
B.CuSO4 «ΜΙ‘≠ΦΝ
C.Fe±Μ―θΜ·
D.CuSO4ΖΔ…ζ―θΜ·Ζ¥”Π
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Ά§―ß…ηΦΤ Β―ι÷Τ±Η2-τ«Μυ-4-±ΫΜυΕΓΥα““θΞΘ§Ζ¥”Π‘≠άμΓΔΉΑ÷ΟΚΆ ΐΨί»γœ¬:


œύΕ‘Ζ÷Ή”÷ ΝΩ | ΟήΕ»(g/cm3) | Ζ–Βψ(Γφ) | Υ°»ή–‘ | |
2-τ«Μυ-4-±ΫΜυΕΓΥα | 180 | 1.219 | 357 | ΈΔ»ή |
““¥Φ | 46 | 0.789 | 78.4 | “Ή»ή |
2-τ«Μυ-4-±ΫΜυΕΓΥα““θΞ | 208 | 1.075 | 212 | Ρ―»ή |
Β―ι≤Ϋ÷η:
ΔΌ»γΆΦ1Θ§‘ΎΗ…‘οΒΡ‘≤ΒΉ…’ΤΩ÷–Φ”»κ20mL2-τ«Μυ-4-±ΫΜυΕΓΥαΓΔ20mLΈόΥ°““¥ΦΚΆ ΝΩ≈®ΝρΥαΘ§‘ΌΦ”»κΦΗΝΘΖ– ·ΘΜ
ΔΎΦ”»»÷Ν70ΓφΉσ”“±Θ≥÷ΚψΈ¬Ακ–Γ ±ΘΜ
ΔέΖ÷άκΓΔΧα¥Ω»ΐΨ±ΤΩ÷–ΒΡ¥÷≤ζΤΖΘ§ΒΟΒΫ”–Μζ¥÷≤ζΤΖΘΜ
ΔήΨΪ÷Τ≤ζΤΖΓΘ
«κΜΊ¥πœ¬Ν–Έ Χβ:
Θ®1Θ©”ΆΥ°Ζ÷άκΤςΒΡΉς”ΟΈΣ__________ΓΘ
Θ®2Θ©±Ψ Β―ι≤…”ΟΥ°‘ΓΦ”»»Θ§“ρΈΣΈ¬Ε»ΙΐΗΏΜα Ι≤ζ¬ _________ (ΧνΓΑ‘ω¥σΓ±ΓΔΓΑΦθ–ΓΓ±ΜρΓΑ≤Μ±δΓ±)ΓΘ
Θ®3Θ©»Γ»ΐΨ±…’ΤΩ÷–ΒΡΜλΚœΈοΖ÷±π”ΟΥ°ΓΔ±ΞΚΆΧΦΥα«βΡΤ»ή“ΚΚΆΥ°œ¥Β”ΓΘΒΎΕΰ¥ΈΥ°œ¥ΒΡΡΩΒΡ «_________ΓΘ
Θ®4Θ©‘ΎΨΪ÷Τ≤ζΤΖ ±Θ§Φ”»κΈόΥ°MgSO4ΒΡΉς”ΟΈΣ____ΘΜ»ΜΚσΙΐ¬ΥΘ§‘Όάϊ”Ο»γΆΦ2ΉΑ÷ΟΫχ––’τΝσ¥ΩΜ·Θ§ΆΦ2ΉΑ÷Ο÷–ΒΡ¥μΈσ”–_________ΓΘ
Θ®5Θ©»τΑ¥Ψά’ΐΚσΒΡ≤ΌΉςΫχ––’τΝσ¥ΩΜ·Θ§≤Δ ’Φ·212ΓφΒΡΝσΖ÷Θ§ΒΟ2-τ«Μυ-4-±ΫΜυΕΓΥα““θΞ‘Φ9.0gΓΘ‘ρΗΟ Β―ιΒΡ≤ζ¬ ΈΣ_________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com