
科目: 来源: 题型:
【题目】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题.某研究小组利用软锰矿(主要成分为MnO2 , 另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2 , 又制得电池材料MnO2(反应条件已省略).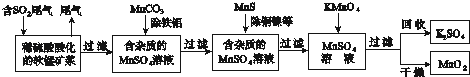
请回答下列问题:
(1)上述流程脱硫实现了(选填下列字母编号).
A.废弃物的综合利用
B.白色污染的减少
C.酸雨的减少
(2)用MnCO3能除去溶液中的Al3+和Fe3+ , 其原因是 .
(3)已知:25℃、101kPa时,Mn(s)+O2(g)═MnO2(s)△H=﹣520kJ/mol
S(s)+O2(g)═SO2(g)△H=﹣297kJ/mol
Mn(s)+S(s)+2O2(g)═MnSO4(s)△H=﹣1065kJ/mol
SO2与MnO2反应生成无水MnSO4的热化方程式是 .
(4)MnO2可作超级电容器材料.用惰性电极电解MnSO4溶液可制得MnO2 , 其阳极的电极反应式是 .
(5)MnO2是碱性锌锰电池的正极材料.碱性锌锰电池放电时,正极的电极反应式是 .
(6)假设脱除的SO2只与软锰矿浆中的MnO2反应.按照图示流程,将a m3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为ckg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2kg.
查看答案和解析>>
科目: 来源: 题型:
【题目】在中学化学实验中使用的玻璃、陶瓷等仪器,在实验操作中不能承受温度的急剧变化,否则会引起安全事故。下列实验操作过程不是基于上述原因的是
A.钠与水反应时,只能取黄豆粒大小的钠投入盛水的烧杯中反应
B.在用二氧化锰和浓盐酸制氯气时,在加入二氧化锰后应首先加入浓盐酸,然后再点燃酒精灯
C.在用固体氯化铵和氢氧化钙制取氨气结束后,将大试管从铁架台上取下置于石棉网上冷却后再洗涤
D.用排水法收集气体后,先移出导气管,后熄灭酒精灯
查看答案和解析>>
科目: 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:【实验一】焦亚硫酸钠的制取
采用如图1装置(实验前已除尽装置内的空气)制取Na2S2O5 . 装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2═Na2S2O5 . 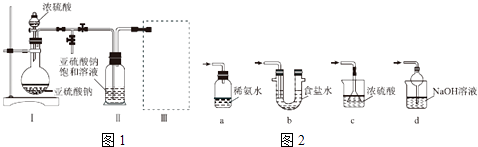
(1)装置Ⅰ中产生气体的化学方程式为 .
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 .
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为(填序号).
(4)【实验二】焦亚硫酸钠的性质:Na2S2O5溶于水即生成NaHSO3 . 证明NaHSO3溶液中HSO ![]() 的电离程度大于水解程度,可采用的实验方法是(填序号).
的电离程度大于水解程度,可采用的实验方法是(填序号).
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
(6)【实验三】葡萄酒中抗氧化剂残留量的测定葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:![]()
(已知:滴定时反应的化学方程式为SO2+I2+2H2O═H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为gL﹣1 .
②在上述实验过程中,若有部分HI被空气氧化,则测定结果(填“偏高”“偏低”或“不变”).
查看答案和解析>>
科目: 来源: 题型:
【题目】通过比较钠与水和钾与水的反应,以及氯、溴、碘之间的置换反应,能得出什么结论?写出本实验中有关反应的化学方程式。___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】有一种星际分子,其分子结构模型如图所示(图中球与球之间的连线代表化学键,如单键、双键、三键等,不同花纹的球表示不同的原子)。

对该物质判断正确的是 ( )
A.①处的化学键是碳碳双键
B.②处的化学键是碳碳三键
C.③处的原子可能是氯原子或氟原子
D.②处的化学键是碳碳单键
查看答案和解析>>
科目: 来源: 题型:
【题目】若在加入铝粉能放出氢气的溶液中,下列各组离子可能共存的是( )
A.NH ![]() 、NO
、NO ![]() 、CO
、CO ![]() 、Na +
、Na +
B.Na+、Ba2+、Mg2+、HCO ![]()
C.NO ![]() 、K+、[Al(OH)4]﹣、OH﹣
、K+、[Al(OH)4]﹣、OH﹣
D.NO ![]() 、Mg2+、K+、Cl﹣
、Mg2+、K+、Cl﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】将下列物质分别注入水中,振荡后静置,能分层且浮于水面的是( )
①溴苯 ②乙酸乙酯 ③乙醇 ④甘油 ⑤油酸甘油酯 ⑥硝基苯
A.全部
B.①②⑤⑥
C.②⑤
D.①⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、I﹣等)中回收碘,其实验过程如图一所示.
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I﹣ , 其离子方程式为;该操作将I2还原为I﹣的目的是 .
(2)操作X的名称为 .
(3)氧化时,在三颈烧瓶中将含I﹣的水溶液用盐酸调至pH约为2,缓慢通入Cl2 , 在40℃左右反应(实验装置如图二所示).实验室控制在较低温度下进行的原因是;锥形瓶里盛放的溶液为 . 
(4)已知:5SO32﹣+2IO3﹣+2H+═I2+5SO42﹣+H2O某含碘废水(pH约为8)中一定存在I2 , 可能存在I﹣、IO3﹣中的一种或两种,请补充完整检验含碘废水中是否含有I﹣、IO3﹣的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com