
【题目】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题.某研究小组利用软锰矿(主要成分为MnO2 , 另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2 , 又制得电池材料MnO2(反应条件已省略).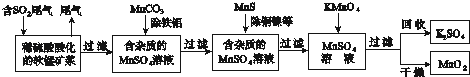
请回答下列问题:
(1)上述流程脱硫实现了(选填下列字母编号).
A.废弃物的综合利用
B.白色污染的减少
C.酸雨的减少
(2)用MnCO3能除去溶液中的Al3+和Fe3+ , 其原因是 .
(3)已知:25℃、101kPa时,Mn(s)+O2(g)═MnO2(s)△H=﹣520kJ/mol
S(s)+O2(g)═SO2(g)△H=﹣297kJ/mol
Mn(s)+S(s)+2O2(g)═MnSO4(s)△H=﹣1065kJ/mol
SO2与MnO2反应生成无水MnSO4的热化方程式是 .
(4)MnO2可作超级电容器材料.用惰性电极电解MnSO4溶液可制得MnO2 , 其阳极的电极反应式是 .
(5)MnO2是碱性锌锰电池的正极材料.碱性锌锰电池放电时,正极的电极反应式是 .
(6)假设脱除的SO2只与软锰矿浆中的MnO2反应.按照图示流程,将a m3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为ckg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2kg.
【答案】
(1)AC
(2)消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀
(3)MnO2(s)+SO2(g)=MnSO4(s)△H=﹣248kJ/mol
(4)Mn2++2H2O﹣2e﹣=MnO2+4H+
(5)MnO2+H2O+e﹣=MnO(OH)+OH﹣
(6)![]()
【解析】解:二氧化硫能与二氧化锰反应生成硫酸锰,用MnCO3能除去溶液中Al3+和Fe3+ , MnS将铜、镍离子还原为单质,高锰酸钾能与硫酸锰反应生成二氧化锰,(1)硫氧化后生成二氧化硫,二氧化硫能形成酸雨,脱硫能减少酸雨和废物在利用,所以答案是:AC;(2)MnCO3消耗溶液中的酸,溶液的酸性减弱,碱性增强,促进Al3+和Fe3+水解生成氢氧化物沉淀,从而达到除去Al3+和Fe3+的目的,所以答案是:消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀;(3)Mn(s)+O2(g)═MnO2(s)△H=﹣520kJmol﹣1S(s)+O2(g)═SO2(g)△H=﹣297kJmol﹣1
Mn(s)+S(s)+2O2(g)═MnSO4(s)△H=﹣1065kJmol﹣1根据盖斯定律,将③﹣②﹣①可得MnO2(s)+SO2(g)=MnSO4(s)△H=﹣248kJ/mol,所以答案是:MnO2(s)+SO2(g)=MnSO4(s)△H=﹣248kJ/mol;(4)锰离子在阳极失电子:Mn2++2H2O﹣2e﹣=MnO2+4H+ ,
所以答案是:Mn2++2H2O﹣2e﹣=MnO2+4H+;(5)二氧化锰得电子生成MnO(OH),MnO2+H2O+e﹣=MnO(OH)+OH﹣ , 所以答案是:MnO2+H2O+e﹣=MnO(OH)+OH﹣;(6)反应的二氧化硫的物质的量为 ![]() ×b%×89.6%=0.4abmol,根据SO2+MnO2=MnSO4可知生成硫酸锰的物质的量为0.4abmol,最终生成的二氧化锰为c kg,设消耗硫酸锰的物质的量为x.
×b%×89.6%=0.4abmol,根据SO2+MnO2=MnSO4可知生成硫酸锰的物质的量为0.4abmol,最终生成的二氧化锰为c kg,设消耗硫酸锰的物质的量为x.
2KMnO4+3MnSO4+2H2O═5MnO2+2H2SO4+K2SO4
3 87×5
x 1000c ![]() ,
,
x= ![]() ,
,
除去铁、铝、铜、镍等杂质时,所引入的锰元素( ![]() ﹣0.4ab)mol,相当于MnO2的质量(
﹣0.4ab)mol,相当于MnO2的质量( ![]() ﹣0.4ab)mol×87g/mol=(600c﹣0.4ab×87)g=
﹣0.4ab)mol×87g/mol=(600c﹣0.4ab×87)g= ![]() kg,所以答案是:
kg,所以答案是: ![]() .
.


科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.已知白磷(P4)为正四面体形,12.4 g白磷中则含有共价键数为0.4 NA
B.3Fe+4H2O(g) ![]() ?Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3 NA电子发生转移
?Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3 NA电子发生转移
C.在0.1 mol/L碳酸钠溶液中Na+总数等于0.2 NA
D.电解精炼铜时,当电路中转移NA个电子时,阴极增重32g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构为 ,已知:
,已知:![]() ,有关核黄素的下列说法中,不正确的是
,有关核黄素的下列说法中,不正确的是
A. 该化合物的分子式为C17H22N4O6
B. 酸性条件下加热水解,有CO2生成
C. 酸性条件下加热水解,所得溶液加碱后有NH3生成
D. 能发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化铜(Ⅱ)甲基咪唑配合物是一种制备有机玻璃的催化剂,其合成方法如下:
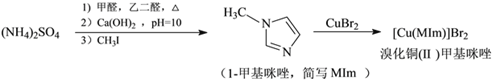
(1)铜元素位于周期表中第___族___区,基态Cu2+的核外电子排布式为______________。
(2)与NH4+互为等电子体的阴离子为__________________。
(3)MIm中碳原子杂化轨道类型为____________;1molMIm中含![]() 键数目为________ mol。
键数目为________ mol。
(4)一种铜的溴化物晶胞结构如图所示。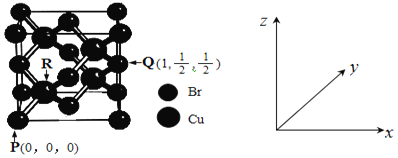
有关说法正确的是____________(填序号)。
a.该化合物的化学式为CuBr2 b.铜的配位数为8
c.与每个Br紧邻的Br有12个
d.由图中P点和Q点的原子坐标参数,可确定R点的原子坐标参数为(![]() ,
,![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法中不正确的是( )
A. 同一横行元素性质基本相同
B. 同一横行元素原子序数从左到右依次递增
C. 同一纵行元素最外层电子数相同
D. 同一纵行元素电子层数自上而下依次递增
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础,研究物质的组成、结构、性质及其变化规律的自然科学。学习科学研究的基本方法,可以加深对科学本质的认识,增进对物质世界的认识。下列有关叙述不正确的是
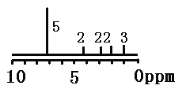
A. 用测定接近水的沸点的水蒸气相对分子质量的方法可知水分子间可以形成氢键
B. 相对分子质量的测定常用质谱仪,在质谱仪内,有机化合物分子在高真空环境下被高能电子束轰击后主要形成带负电的碎片
C. 利用红外光谱、核磁共振氢谱等现代物理方法或化学方法均可测定C2H6O的分子结构
D. 某有机物分子式为C11H14O2,其H—NMR图谱如右图(峰右侧或上面的数字表示H的个数,且知:7.2ppm(5H)为苯基),可推测该有机物可能为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)在水溶液中橙红色的Cr2O72--与黄色的CrO42--有下列平衡关系:Cr2O72--+H 2O![]() 2CrO42--+2H+现将一定量的K2Cr2O7溶于水配成稀溶液,溶液呈橙色。
2CrO42--+2H+现将一定量的K2Cr2O7溶于水配成稀溶液,溶液呈橙色。
(1)向上述溶液中加入浓硫酸溶液,溶液呈__________色,因为_____________________。
(2)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡向__________方向移动(正或逆),溶液颜色将__________(加深或变浅)。
(II)工业上有一种用CO2生产甲醇燃料的方法:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol
某实验中将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图曲线 (甲)所示。请完成下列问题:
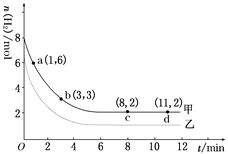
(1)a点正反应速率________逆反应速率(填“>”、“<”或“=”)。
(2)若仅改变某一实验条件再进行一次实验,测得H2的物质的量随时间变化如图中虚线(乙)所示,曲线(乙)对应改变的实验条件可以是________(填序号)。
a.加催化剂 b.增大压强 c.升高温度 d.增大H2浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com