
科目: 来源: 题型:
【题目】取3.38g K2CO3和KHCO3的混合物溶于水配成25mL溶液,往溶液中加入25mL Ba(OH)2溶液恰好使生成白色沉淀的量最多.反应后溶液的c(OH﹣)=0.8mol/L(忽略混合后溶液体积变化).则原混合物中K2CO3和KHCO3 物质的量之比为( )
A.1:2
B.1:1
C.2:1
D.2:3
查看答案和解析>>
科目: 来源: 题型:
【题目】碘是人类发现的第二个生命体必须微量元素,回答下列问题:
(1)碘是氯的同族元素,它们位于元素周期表第族;HI的稳定性比HCl(填“强”或“弱”,下同),HI的还原性比HCl
(2)为了从海带中提取碘,某研究性学习小组设计并进行了如图实验: 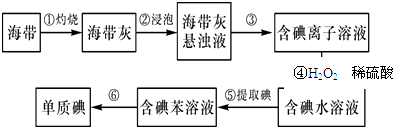
步骤①需要在(填仪器名称)中进行.步骤④反应的离子方程式是 . 步骤⑤中应进行的操作名称是
(3)自然界中的碘有的以NaIO3形态,加入NaHSO4可以制得I2 , 反应为:(未配平)IO3﹣+HSO3﹣→I2+SO42﹣+H++H2O,若制得1mol I2 , 则转移的电子数目为
查看答案和解析>>
科目: 来源: 题型:
【题目】不同元素的原子电负性不同,若用x值来表示,x值越大,其原子的电负性就越大,吸引电子的能力越强,在所形成的分子中成为带负电荷的一方,下面是某些短周期元素的电负性的值:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
第二周期 | Li | Be | B | C | N | O | F |
电负性值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | |
第三周期 | Na | Mg | Al | Si | P | S | Cl |
电负性值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析x值的变化规律,确定N、Mg的x值的范围:<x(Mg)< , <x(N)< .
(2)推测x值与原子半径的关系是 . 根据短周期元素x值变化特点,体现了元素性质的变化规律.
(3)某有机物结构简式如图,其中C﹣N中,你认为共用电子对偏向原子(填原子名称). 
(4)经验规律告诉我们,当成键的两原子的x差值,即△x>1.7时,一般为离子键,当△x<1.7时,一般为共价键.试推断AlBr3中化学键的类型为
(5)预测元素周期表中x值最小的元素是(填元素符号,放射性元素除外).
查看答案和解析>>
科目: 来源: 题型:
【题目】下列递变规律不正确的是( )
A. Na、Mg、Al还原性依次减弱B. I2、Br2、Cl2氧化性依次增强
C. C、N、O原子半径依次增大D. P、S、Cl最高正价依次升高
查看答案和解析>>
科目: 来源: 题型:
【题目】某混合物的水溶液中可能含有以下离子中的若干种:Na+、Al3+、Fe3+、Mg2+、Ba2+、NH ![]() 、Cl﹣、SO
、Cl﹣、SO ![]() ,现分别取100mL的两份溶液进行如下实验. ①第一份加过量NaOH溶液后加热,收集到0.03mol气体,无沉淀生成,同时得到溶液甲.
,现分别取100mL的两份溶液进行如下实验. ①第一份加过量NaOH溶液后加热,收集到0.03mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2 , 生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到23.3g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
A.由①可知原溶液存在离子为NH4+ , 其浓度为0.03mol/L
B.原溶液肯定没有Fe3+、Mg2+ , 一定含有Na+
C.n(NH ![]() ):n(Al3+):n(SO
):n(Al3+):n(SO ![]() )=3:1:10
)=3:1:10
D.原溶液一定存在Cl﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3 , 其流程如下: 
已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
FeS2+14Fe3++8H2O=15Fe2++2SO42﹣+16H+
(1)加入FeS2还原后,检验Fe3+是否反应完全的试剂为 .
(2)所得FeCO3需充分洗涤,检验是否洗净的方法是 . “沉淀”时,pH不宜过高,否则制备的FeCO3中可能混有的杂质是 .
(3)①写出“还原”时反应Ⅱ的离子方程式: .
(4)②“还原”前后溶液中部分离子的浓度见下表(溶液体积变化或略不计):
离子 | 离子浓度(molL﹣1) | |
还原前 | 还原后 | |
Fe2+ | 0.10 | 2.5 |
SO42﹣ | 3.5 | 3.7 |
请计算反应Ⅰ、Ⅱ中被还原的Fe3+的物质的量之比(写出计算过程).
查看答案和解析>>
科目: 来源: 题型:
【题目】在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见图).下列说法错误的是( ) 
A.a、b两处的混合气体成分含量相同,温度不同
B.c、d两处的混合气体成分含量相同,温度不同
C.热交换器的作用是预热待反应的气体,冷却反应后的气体
D.c处气体经热交换后再次催化氧化的目的是提高SO2的转化率
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20.其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1 . B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题:
(1)A是 , B是 , E是 .
(2)写出C元素基态原子的电子排布式 .
(3)用轨道表示式表示D元素原子的价电子构型 .
(4)元素B与D的电负性的大小关系是 , C与E的第一电离能的大小关系是 . (填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com