
科目: 来源: 题型:
【题目】FeCO3与砂糖混用可作补血剂.以黄铁矿烧渣(含CuO、Fe2O3、FeO、SiO2、Al2O3等)为主要原料制备FeCO3的流程如下: 
(1)质量分数为30%(密度是1.176gcm﹣3)的稀硫酸的物质的量浓度为 .
(2)检验滤液A中存在Fe2+的试剂是 .
(3)加入足量铁粉的作用除调节pH使Al3+转化为Al(OH)3沉淀外,还有两个作用,写出其中一个反应的离子方程式:
(4)写出滤液C与NH4HCO3溶液反应的离子方程式: .
(5)FeCO3在空气中灼烧可制得铁系氧化物材料.已知25℃,101kPa时:
4Fe(s)+3O2(g)═2Fe2O3△H=﹣1648kJmol﹣1
C(s)+O2(g)═CO2(g)△H=﹣393kJmol﹣1
2Fe(s)+2C(s)+3O2(g)═2FeCO3(s)△H=﹣1480kJmol﹣1
写出FeCO3在空气中灼烧生成Fe2O3的热化学方程式: .
(6)某兴趣小组为充分利用副产品,欲利用滤渣D为原料制取Al2O3 , 请补充完成实验步骤:向滤渣D中加入适量NaOH溶液,
查看答案和解析>>
科目: 来源: 题型:
【题目】某化工厂用软锰矿(含MnO2及少量Al2O3)和闪锌矿(含ZnS及少量FeS)联合生产Zn、MnO2 , 其部分生产流程如下: 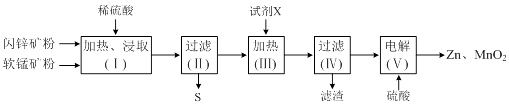
已知:过滤(Ⅱ)所得滤液是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液.相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL﹣1计算)如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 | Mn(OH)2 |
开始沉淀时的pH | 2.7 | 4.0 | 6.4 | 7.7 |
完全沉淀时的pH | 3.7 | 5.2 | 8.0 | 10.4 |
(1)加热、浸取时所加矿石均需粉碎,其目的是 .
(2)写出FeS和MnO2和稀硫酸反应的离子方程式: .
(3)试剂X的作用是调节溶液的pH以生成Fe(OH)3、Al(OH)3 . pH调节的范围是 , 试剂X可以选用(填选项字母).
A.MnCO3 B.Na2CO3 C.Zn2(OH)2CO3 D.NH3H2O
(4)电解(Ⅴ)中阳极的电极反应式为 .
(5)Zn和MnO2是制作电池的原料.某锌﹣锰碱性电池以KOH溶液为电解质溶液,其电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s).该电池的正极的电极反应式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质互为同系物的是 ( )
A. C6H5OH和C6H5CH2OH B. CH3OH和HOCH2CH2OH
C. HCOOH和C17H35COOH D. CH3Cl和CH2Cl2
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应在生产生活中有着重要的应用.请按要求写出相应的方程式.
(1)将含SO2的废气通入含Fe2+(催化剂)的溶液中,常温下可使SO2转化为SO24﹣ , 其总反应为2SO2+O2+2H2O=2H2SO4 . 上述总反应分两步进行,第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,写出第二步反应的离子方程式: .
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6﹣2x]溶液.若溶液的pH偏高,则碱式硫酸铝产率降低且有气泡产生,用化学方程式表示其原因: .
(3)ClO2是一种高效安全的杀菌消毒剂.氯化钠电解法生产ClO2工艺原理示意图如下: 
①写出氯化钠电解槽内发生反应的离子方程式: .
②写出ClO2发生器中的化学方程式,并标出电子转移的方向及数目: .
③ClO2能将电镀废水中的CN﹣离子氧化成两种无毒气体,自身被还原成Cl﹣ . 写出该反应的离子方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸钙可用于生产硫酸、漂白粉等一系列物质(见图).下列说法正确的是( ) 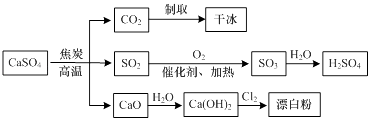
A.CO2制取干冰的过程吸收热量,属于物理变化
B.硫酸钙与焦炭反应时生成的n(CO2):n(SO2)=1:2
C.由SO2制取H2SO4的过程均为氧化还原反应
D.石灰乳与Cl2反应制取漂白粉时,Cl2仅作还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】镁是一种活泼的金属,可以在CO2中燃烧生成MgO和C,海水中镁含量很大,世界上生产的镁60%来自海水.海水提镁,需要在海水中加碱,然后沉淀分离后转化为氯化镁,最后电解得到金属镁.试根据你已有的知识,回答下列问题:
(1)请用流程图式表示工业上用海水提炼镁的主要工序 .
(2)若金属镁的提取都是利用电解氯化镁来进行的.请写出电解氯化镁的化学方程式 , 在电解过程中还原剂是 , 氧化产物是 .
(3)若用电解制得的镁来制镁粉,可将镁加热变成蒸气,然后冷却得到镁粉,这个过程能在空气中进行吗?原因是什么? , 现有气体:二氧化碳、氢气、氩气、氮气、氧气,可以选择用于冷却镁粉的气体有 .
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( ) 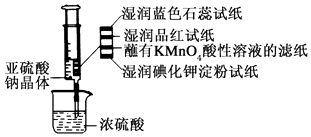
A.湿润的蓝色石蕊试纸只变红不褪色
B.湿润的品红试纸蘸有KMnO4酸性溶液的滤纸均褪色证明了SO2的漂白性
C.湿润的碘化钾淀粉试纸未变蓝说明SO2不能将I﹣还原为I2
D.实验后,可把注射器中的物质推入NaOH溶液,以减少环境污染
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶质 | HCl | NaOH | CH3COOH | HNO3 |
溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
物质的量浓度/mol·L1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是
A.HCl B.NaOH C.CH3COOH D.HNO3
查看答案和解析>>
科目: 来源: 题型:
【题目】实验中需用2.0 mol·L1的Na2CO3溶液950 mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为
A.950 mL;201.4 g B.1 000 mL;212.0 g
C.100 mL;21.2 g D.500 mL;100.7 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com