
科目: 来源: 题型:
【题目】室温下,0.1mol/L的二元酸H2A溶液中,溶液体系可能存在的含A粒子(H2A、HA﹣、A2﹣)所占物质的量分数随pH变化的关系如图所示,下列说法正确的是( ) 
A.H2A的电离方程式为:H2AH++HA﹣
B.pH=5时,在NaHA和Na2A的混合溶液中:c(HA﹣):c(A2﹣)=1:100
C.等物质的量浓度的NaHA和Na2A溶液等体积混合,离子浓度大小关系为c(Na+)>c(HA﹣)>c(A2﹣)
D.Na2A溶液必存在c(OH﹣)=c(H+)+c(HA﹣)+2c(H2A),各粒子浓度均大于0
查看答案和解析>>
科目: 来源: 题型:
【题目】天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl﹣、SO42﹣、Br﹣、CO32﹣、HCO3﹣等离子.火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示: 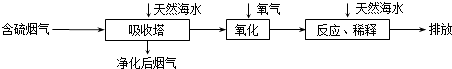 下列说法错误的是( )
下列说法错误的是( )
A.天然海水pH≈8的原因是由于海水中的CO32﹣、HCO3﹣水解
B.“氧化”是利用氧气将H2SO3、HSO3﹣、SO32﹣等氧化生成SO42﹣
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧化后海水中生成的酸
D.“排放”出来的海水中SO42﹣的物质的量浓度与进入吸收塔的天然海水相同
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求回答问题:
(1)向某NaOH溶液中投入一块Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为 .
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为 .
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为 .
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备.某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3 , 则该小组同学实验时发生的总离子反应方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料.以含镍(Ni2+)废液为原料生产NiOOH的一种工艺流程如图1: 
(1)加入Na2CO3溶液时,证明Ni2+已经完全沉淀的实验方法是 . 过滤时需用到的玻璃仪器有烧杯、
(2)写出碳酸镍与稀硫酸反应的离子方理式 .
(3)硫酸镍溶液可用于制备合成氨的催化剂ConNi(1﹣n)Fe2O4 . 在其他条件相同时合成氨的相对初始速率随催化剂中n值变化的曲线如图,由图分析可知Co2+、Ni2+两种离子中催化效果更好的是
(4)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式: .
(5)若加热不充分,则制得的NiOOH中会混有Ni(OH)2 , 其组成可表示为xNiOOHy Ni(OH)2 . 现称取9.21g样品溶于稀硫酸中,冷却后转入容量瓶并配制成500mL溶液.取出25.00mL,用0.100mol/LKMnO4标准溶液滴定,用去KMnO4标准溶液10.00mL,则x:y= . [已知反应(未配平):Ni2++MnO4﹣+H+→Ni2++Mn2++H2O].
查看答案和解析>>
科目: 来源: 题型:
【题目】最近日本科学家确认世界还存在着另一种“分子足球”N60,它与C60分子结构相似。N60在高温或撞击后会释放出巨大能量。下列对N60的说法不正确的是( )
A. N60和14N都是氮的同位素 B. N60和N2都是氮的同素异形体
C. N60中氮原子之间由共价键结合 D. N60的摩尔质量为840g/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”. 
(1)过氧化钠与水反应的化学方程式是 .
(2)装置I是制备纯净的(填化学式).则装置I中最适宜的试剂组合是(填字母). a.稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹K2 , 关闭K1 , 观察到预期现象后,打开K1 , 再关闭K2 . 实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃.
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是;
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+ 和Na+ . 某同学为了确认其成分,取部分试液,设计并完成了如下实验:下列说法正确的是( ) 
A.原溶液中c(Fe3+)=0.2molL﹣1
B.溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2molL﹣1
C.SO42ˉ、NH4+、Na+一定存在,CO32ˉ一定不存在
D.要确定原溶液中是否含有Fe2+ , 其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液成血红色,则含有Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯(ClO2)是高效安全的饮用水消毒剂,得到越来越广泛的应用.回答下列问题:
(1)实验室合成ClO2常用盐酸或双氧水还原氯酸钠(NaClO3).
①盐酸和NaClO3反应时有ClO2和Cl2生成,反应的离子方程式为 , 当反应中转移0.2mol 电子时,参加反应的还原剂的物质的量为 .
②使用双氧水作还原剂的优点是 .
(2)ClO2可用于合成亚氯酸钠(NaClO2).将ClO2通入NaOH溶液中,并加入适量双氧水,在稳定装置中充分反应可制得NaClO2成品. 已知:当pH≤2.0时,NaClO2能被I﹣完全还原成Cl﹣;二氧化氯(ClO2)是高效安全的饮用水消毒剂,得到越来越广泛的应用.回答下列问题:
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6 . 欲测定成品中NaClO2的含量,现进行如下操作:
步骤Ⅰ | 称取样品Wg配成溶液置于锥形瓶中,并调节PH≤2.0 |
步骤Ⅱ | 向锥形瓶中加入足量KI晶体,充分搅拌,并加入少量指示剂 |
步骤Ⅲ | 用c mol/L的Na2S2O3溶液滴定 |
①步骤2发生反应的离子方程式为 , 加入指示剂的名称是 .
②若上述滴定操作中平均消耗VmL Na2S2O3标准溶液,则成品中NaClO2的质量分数为(用含w、c、V的代数式表示).
(3)ClO2和Cl2均能将电镀废水中的CN﹣氧化为无毒的物质,自身被还原为Cl﹣ . 处理含相同量CN﹣的电镀废水,所需Cl2的物质的量是ClO2的倍.
查看答案和解析>>
科目: 来源: 题型:
【题目】水合肼(N2H4H2O)又称水合联氨,其纯净物为无色透明的油状液体,具有强碱性和吸湿性.将水合肼通入CuO胶体中,可发生如图所示的转化. 
(1)图示的转化中,②属于(填“非氧化还原反应”或“氧化还原反应”).
(2)转化①中,氧化剂与还原剂的物质的量之比为4:l,则X的化学式为 .
(3)转化②中,反应一段时间后,溶液中n(OH﹣)(填“增大”“减小”或“不变”).
(4)若①中参加反应的CuO物质的量为0.4mol,按图示转化过程进行后,④中生成的CuO物质的量也等于0.4mol,则③中参加反应的O2的物质的量与④中今加反应的NaClO的物质的量之比为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com