
科目: 来源: 题型:
【题目】X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去). 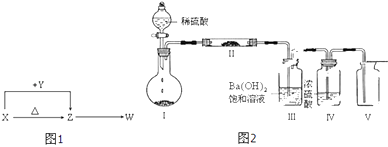
请回答:
(1)W的电子式是 .
(2)X与Y在溶液中反应的离子方程式是 .
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用如图2装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体.
①装置Ⅰ中反应的化学方程式是 ,
装置Ⅱ中物质的化学式是 .
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 , 所需仪器装置是(从图中选择必要装置,填写编号).
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知几种阴离子还原性强弱顺序为F-<Cl-<Br-<I-<S2-。某溶液含有相同浓度的F-、Cl-、Br-、I-、S2-,当向其中逐滴加入新制的饱和氯水直至过量时,最后被氧化的离子是 ( )
A.Br-B.Cl-C.F-D.S2-
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是环保部门监测有害气体常用的一种药品,它易溶于水,遇酸易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图。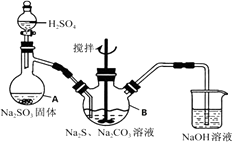
实验具体操作步骤为:
①打开分液漏斗使硫酸慢慢滴下,适当调节分液漏斗的滴速,使反应产生的SO2气体较均匀的通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体。
(1)写出仪器A的名称。
(2)写出A中发生反应的化学方程式。
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是。
(4)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42离子,该反应的离子方程式为。
(5)为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下图装置进行实验。
①实验装置的连接顺序依次是(填装置的字母代号),装置C中的试剂为。
②能证明固体中含有碳酸钠的实验现象是。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层;Z与X在周期表中位于同一主族.回答下列问题:
(1)X的电子排布式为 , Y的电子排布图为;
(2)ZX2的分子式是 , YX2电子式是;
(3)Y与Z形成的化合物的分子式是 , 该化合物中化学键的种类是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】现有100mL含Cu2+、Al3+、NH4+、H+、Cl-的溶液,向该溶液中逐滴加入2.5mol·L-1NaOH溶液,所加NaOH 溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示: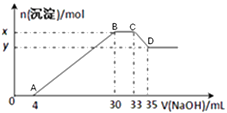
(1)B点的沉淀物的化学式为。
(2)原溶液中Cu2+的物质的量为 , 原溶液中Cl-物质的量浓度为。
(3)原溶液的pH= , x-y= 。
(4)经过滤得到D点的沉淀物,并多次用蒸馏水洗涤沉淀,判断沉淀是否洗涤干净的方法是
查看答案和解析>>
科目: 来源: 题型:
【题目】已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
(1)表中硫酸的质量分数W1为(不写单位,用含c1、p1的代数式表示)。
(2)物质的量浓度为c1mol· L-1质量分数为w1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为 mol· L-1 , 质量分数w1/2(填“大于”、“小于”或“等于”,下同)。
(3)质量分数为w2的氨水与w2/5的氨水等质量混合,所得溶液的密度 ![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用如图装置,写出除去下列物质中的杂质的方法,并写出化学方程式(括号内的气体为杂质). 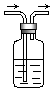
(1)CO2( SO2) , 化学方程式 .
(2)SO2 ( HCl ) , 化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com