
科目: 来源: 题型:
【题目】将3molO2加入到VL的反应器中,在高温下放电,经t1s建立了平衡体系:3O22O3 , 此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
A.
B.
C.
D.
查看答案和解析>>
科目: 来源: 题型:
【题目】(14分) 近期发现,H2S是继NO、CO之后第三个生命体系气体信号分子,它具有参与调解神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是_________(填标号)。
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。 
通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为、 , 制得等量H2所需能量较少的是。
(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) ![]() COS(g) +H2O(g)。在
COS(g) +H2O(g)。在 ![]() 610 k时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。 ①H2S的平衡转化率
610 k时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。 ①H2S的平衡转化率 ![]() =%,反应平衡常数K=。
=%,反应平衡常数K=。
②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率 ![]()
![]() ,该反应的
,该反应的 ![]() H0。(填“>”“<”或“=”)
H0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H2S转化率增大的是(填标号)
A. H2S B. CO2 C.COS D.N2
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下有①6.72L CH4②3.01×1023个HCl ③13.6g H2S ④0.2mol NH3四种气体,气体所占体积由小到大的顺序是(填序号,下同);所含氢原子数由小到大的顺序是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】4.35g二氧化锰能与足量浓盐酸(密度为1.19gcm﹣3、质量分数为36.5%)完全反应.求:
(1)浓盐酸中HCl的物质的量浓度:c(HCl)= .
(2)被氧化的HCl的物质的量:n(HCl)= .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关氮及其化合物说法正确的是
A. 实验室利用铁片与稀硫酸或稀硝酸反应制取H2
B. 氨易液化,可用来做制冷剂
C. 用向上排空气法收集铜粉与稀硝酸反应产生的NO
D. 常温下,N2既能与O2反应,又能与H2反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是( )
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10﹣5
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关卤素的说法错误的是
A. 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2
B. HF、HCl、HBr、HI的还原性依次增强
C. 淀粉-碘化钾酸性溶液在空气中变蓝,4I-+O2+4H+=2I2+2H2O
D. 次氯酸盐具有氧化性,故漂白粉可以漂白织物
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).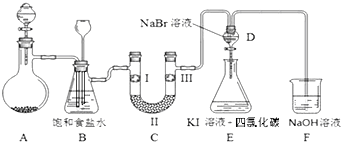
(1)制备氯气选用的药品为二氧化锰和浓盐酸,则相关的化学反应方程式为: .
(2)装置B中饱和食盐水的作用是 .
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入 .
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 无水CaCl2 | 浓硫酸 | 无水CaCl2 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D,E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为色,打开D装置中活塞,将D中少量溶液加入装置E中,振荡.观察到的现象是 . 经认真考虑,有同学提出该实验方案仍有不足,请说明其中不足的原因是 .
(5)装置F中用足量NaOH溶液吸收剩余的氯气,试写出相应的化学方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色溶液,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、NH4+、Cl﹣、CO32﹣和SO42﹣ . 现每次取100mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH溶液,整个过程没有沉淀产生,加热,收集到气体1.12L(标准状况)
③第三份加入足量BaCl2溶液后得干燥沉淀4.30g,沉淀经足量盐酸洗涤,干燥后剩余2.33g.
根据以上实验,肯定存在的离子有 , 肯定不存在的离子有 , 还有一种离子不能确定是否存在,要检验这种离子的实验操作方法是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com