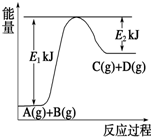
Ⅰ.已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
(1)该反应是
吸热
吸热
反应(填“吸热”或“放热”),该反应的△H=
E1-E2
E1-E2
kJ?mol
-1(用含E
1、E
2的代数式表示),1mol气体A和1mol气体B具有的总能量比1mol气体C和1mol气体D具有的总能量
一定低
一定低
(填“一定高”、“一定低”或“高低不一定”).
(2)若在反应体系中加入催化剂使逆反应速率增大,则E
1和E
2的变化是:E
1减小
减小
,E
2减小
减小
,△H
不变
不变
(填“增大”、“减小”或“不变”).
Ⅱ.已知下列热化学方程式
Fe
2O
3(s)+3CO(g)═2Fe(s)+3CO
2(g)△H
1=-25kJ?mol
-1①
3Fe
2O
3(s)+CO(g)═2Fe
3O
4(s)+CO
2(g)△H
2=-47kJ?mol
-1 ②
Fe
3O
4(s)+CO(g)═3FeO(s)+CO
2(g)△H
3=+19kJ?mol
-1③
写出FeO(s)被CO还原成Fe和CO
2的热化学方程式
CO(g)+FeO(s)=Fe(g)+CO2(g)△H=-11KJ/mol
CO(g)+FeO(s)=Fe(g)+CO2(g)△H=-11KJ/mol
.

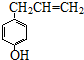 胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法:
胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法: 氨是重要的氮肥,合成原理为:N2(g)+3H2(g)
氨是重要的氮肥,合成原理为:N2(g)+3H2(g)  Ⅰ.已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
Ⅰ.已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.