
科目: 来源: 题型:
【题目】氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1)配平离子方程式:MnO4﹣+HSO3﹣+H+﹣﹣Mn2++SO42﹣+H2O
(2)用KMnO4进行滴定时,KMnO4溶液应装在中,判断滴定终点的现象是 .
(3)下列操作会导致测定结果偏高的是
A.未用标准浓度的酸性KMnO4溶液润洗滴定管
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定前滴定管尖嘴部分有气泡
D.观察读数时,滴定前仰视,滴定后俯视
(4)根据下表中测定的实验数据,计算KMnO4溶液体积的平均值为mL;NaHSO3溶液的物质的量浓度为mol/L(数据精确到0.1)
实验编号 | 待测NaHSO3溶液的体积/mL | KMnO4溶液的体积/mL |
1 | 20.00 | 15.98 |
2 | 20.00 | 17.00 |
3 | 20.00 | 16.02 |
查看答案和解析>>
科目: 来源: 题型:
【题目】根据所给的信息和标志,判断下列说法不正确的是( )
A | B | C | D |
|
|
|
|
古代中国人已用麻黄治疗咳嗽 | 用于杀菌消毒和衣物的洗涤漂白 | 不可以用氢氧化钠溶液将其溶解 | 废纸、塑料、玻璃、金属均可回收 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp).例如:Cu(OH)2 ![]() Cu2++2OH﹣ , Ksp=c(Cu2+)[c(OH﹣)]2=2×10﹣20 . 当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
Cu2++2OH﹣ , Ksp=c(Cu2+)[c(OH﹣)]2=2×10﹣20 . 当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
(1)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于 .
(2)要使0.2molL﹣1CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是配制250mL0.2mol·L-1氯化钠溶液的步骤:
①溶解②洗涤③移液④计算⑤定容⑥称量⑦盖好瓶塞,反复上下颠倒,摇匀。请你选出该溶液配制的操作先后顺序是
A. ②③⑤①⑥⑦④ B. ④⑥①③②⑤⑦
C. ④②⑤⑥①③⑦ D. ②⑥⑦④③⑤①
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯. ![]()
![]()
![]()
制备苯甲酸苯酯的实验步骤为:
步骤1:将20mL浓H2SO4与40mL冰醋酸在下图装置的烧杯中控制在5℃以下混合.
步骤2:向烧杯中继续加入过硫酸钾25g,用电磁搅拌器搅拌4~5分钟,将二苯甲酮9.1g溶于三氯甲烷后,加到上述混合液中,控制温度不超过15℃,此时液体呈黄色.
步骤3:向黄色液体中加水,直至液体黄色消失,但加水量一般不超过1mL,室温搅拌5h.
步骤4:将反应后的混合液倒入冰水中,析出苯甲酸苯酯,抽滤产品,用无水乙醇洗涤,干燥
(1)步骤1中控制在5℃以下混合的原因为 .
(2)步骤2中为控制温度不超过15℃,向混合液中加入二苯甲酮的三氯甲烷溶液的方法是 .
(3)步骤3中加水不超过1mL,原因是 .
(4)步骤4中抽滤用到的漏斗名称为 .
(5)整个制备过程中液体混合物会出现褐色固体,原因是;除去该固体操作为 . 
查看答案和解析>>
科目: 来源: 题型:
【题目】进行过滤操作应选用的一组仪器是
A. 烧杯、酒精灯、试管、铁架台(铁圈)、漏斗
B. 滤纸、烧杯、试管夹、漏斗、玻璃棒
C. 烧杯、漏斗、玻璃棒、铁架台(铁圈)、滤纸
D. 滤纸、试管、漏斗、铁架台(铁圈)、玻璃棒
查看答案和解析>>
科目: 来源: 题型:
【题目】甲同学通过查询资料知道,一定浓度的硝酸与Mg反应时,可同时得到NO2、NO、N2三种气体。该同学欲用下列仪器组装装置来直接验证有NO2、NO生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①NO2沸点为21.1 ℃、熔点为-11 ℃,NO沸点为-151 ℃、熔点为-164 ℃;
②镁也能与CO2反应;
③氮化镁遇水剧烈水解生成Mg(OH)2和氨气。

(1)为实现上述实验目的,所选用的仪器的正确连接方式是:A→ →E,实验中先打开开关K,通过导管向装置内通入CO2气体以排出装置内的空气,停止通入CO2的标志是 。
(2)确定还原产物中有NO2的现象是 ,实验中要多次使用装置F,第二次使用F的目的是 。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式 。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是 。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氨气生成 。
查看答案和解析>>
科目: 来源: 题型:
【题目】三氯化铁是合成草酸铁的重要原料.
(1)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)35H2O]的实验流程如图所示: 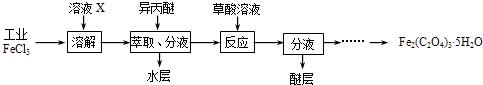
①为抑制FeCl3水解,溶液X为 .
②上述流程中FeCl3能被异丙醚萃取,其原因是;检验萃取、分液后所得水层中是否含有Fe3+的方法是 .
③所得Fe2(C2O4)35H2O需用冰水洗涤,其目的是 .
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4 , KMnO4标准溶液应置于右图所示仪器(填“甲”或“乙”)中.下列情况会造成实验测得Fe2(C2O4)35H2O含量偏低的是 .
a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
(2)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3 , 再由FeCl3合成Fe2(C2O4)35H2O.请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤;;调节溶液pH,将溶液蒸发浓缩、冷却结晶、过滤、洗涤干燥得FeCl36H2O; , 得到无水FeCl3 . ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com