
科目: 来源: 题型:
【题目】A(C2H4)是基本的有机化工原料.用A和常见的有机物可合成一种醚类香料和一种缩醛类香料.具体合成路线如图所示(部分反应条件略去): 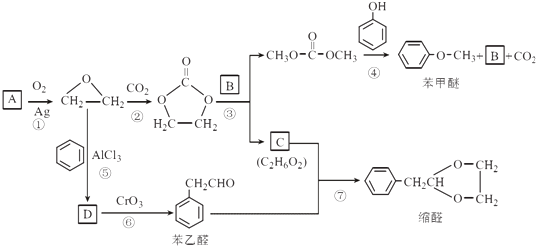
已知以下信息:
① ![]()
②D为单取代芳香族化合物且能与金属钠反应;每个D分子中只含有1个氧原子,D中氧元素的质量分数约为13.1%.
回答下列问题:
(1)A的名称是 , 图中缩醛的分子式是 .
(2)B的结构简式为 , C中含有的官能团名称是 .
(3)⑥的反应类型是 .
(4)⑤的化学方程式为 .
(5)请写出满足下列条件的苯乙醛的所有同分异构体的结构简式:含有苯环和 ![]() 结构,核磁共振氢谱有4组峰,峰面积之比为3:2:2:1.
结构,核磁共振氢谱有4组峰,峰面积之比为3:2:2:1.
(6)参照 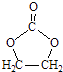 的合成路线,设计一条由2﹣氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2﹣氯丙烷和必要的无机试剂制备 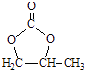 的合成路线(注明必要的反应条件).
的合成路线(注明必要的反应条件).
查看答案和解析>>
科目: 来源: 题型:
【题目】张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用.氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题: 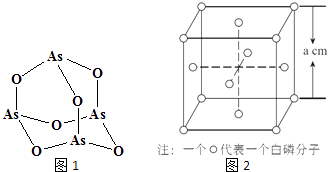
(1)As原子的核外电子排布式为 .
(2)P和S是同一周期的两种元素,P的第一电离能比S大,原因是 .
(3)NH4+中H﹣N﹣H的键角比NH3中H﹣N﹣H的键角(填“大”或“小”),原因是 .
(4)Na3AsO4中含有的化学键类型包括;AsO43﹣的空间构型为 , As4O6的分子结构如图1所示,则在该化合物中As的杂化方式是 .
(5)化合物NH5中的所有原子最外层都满足稳定结构,则NH5是晶体.
(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2(小圆圈表示白磷分子).己知晶胞的边长为a cm,阿伏加德罗常数为NA mol﹣l , 则该晶胞中含有的P原子的个数为 , 该晶体的密度为gcm﹣3(用含NA、a的式子表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】镁一次氯酸盐电池的工作原理如图,该电池反应为:Mg+ClO﹣+H2O═Mg(OH)2+Cl﹣ . 下列有关说法正确的是( ) 
A.电池工作时,正极a附近的pH将不断增大
B.电池工作时,C溶液中的溶质是MgCl2
C.负极反应式:ClO﹣+2e﹣+H2O=Cl﹣+2OH﹣
D.b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质转化在给定条件下能实现的是( )
A.FeS2 ![]() SO3
SO3 ![]() H2SO4
H2SO4
B.NaCl(aq) ![]() Na
Na ![]() Na2O2
Na2O2
C.Fe ![]() FeSO4(aq)
FeSO4(aq) ![]() Fe(OH)2
Fe(OH)2 ![]() Fe2O3
Fe2O3
D.Fe2O3 ![]() FeCl3(aq)
FeCl3(aq) ![]() Fe
Fe
查看答案和解析>>
科目: 来源: 题型:
【题目】锗是重要的半导体材料,应用于航空航天测控、光纤通讯等领域.一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下: 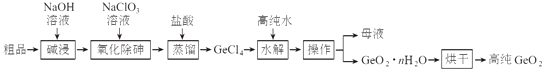
已知:①“碱浸”过程中的反应为:
GeO2+2NaOH═Na2GeO3+H2O
As2O3+2NaOH═2NaAsO2+H2O
②“蒸馏”过程中的反应为:Na2GeO3+6HCl═2NaCl+GeCl4+3H2O
③GeCl4的熔点为﹣49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃.
(1)锗的原子序数为32,锗在元素周期表中的位置为第周期族.
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4 , 其反应方程式为: .
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是 .
(4)工业上与蒸馏操作相关的设备有
A.蒸馏釜
B.离心萃取机
C.冷凝塔
D.加压过滤机
(5)“水解”操作时发生的化学反应方程式为 , “水解”操作时保持较低温度有利于提高产率,其最可能的原因是(答一条即可).
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的高纯二氧化锗产品,则杂质脱除率为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】氮及其化合物在生产生活中有广泛应用.
(1)已知:CO可将部分氮的氧化物还原为N2 . 反应Ⅰ:2CO(g)+2NO(g)N2(g)+2CO2(g)△H=﹣746kJmol﹣1
反应Ⅱ:4CO(g)+2NO2(g)N2(g)+4CO2(g)△H=﹣1200kJmol﹣1
写出CO将NO2还原为NO的热化学方程式 .
(2)在密闭容器中充入5mol CO和4mol NO,发生上述反应I,图1为平衡时NO的体积分数与温度、压强的关系. 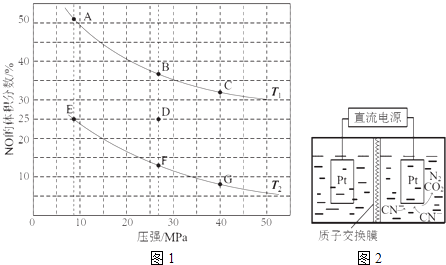
回答下列问题:
①温度:T1T2(填“<”或“>”).
②某温度下,在体积为2L的密闭容器中,反应进行10分钟放出热量373kJ,用CO的浓度变化表示的平均反应速率v(CO)= .
③某温度下,反应达到平衡状态D点时,容器体积为2L,此时的平衡常数K=(结果精确到0.01);若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的点
(3)某温度时,亚硝酸银AgNO2的 Ksp=9.0×10﹣4、Ag2SO4的Ksp=4.0×10﹣5 , 当向含NO2﹣、SO42﹣混合溶液中加入AgNO3溶液至SO42﹣恰好完全沉淀(即SO42﹣浓度等于1.0×10﹣5 molL﹣1)时,c(NO2﹣)= .
(4)如图2,在酸性条件下,电解水中CN﹣可转化为CO2和N2 , 请写出阳极的电极反应式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是( )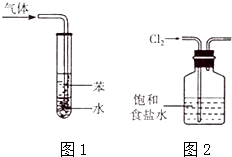
A.用pH试纸测量新制氯水的pH
B.用量筒量取 20mL 0.5000molL﹣1 H2SO4溶液于烧杯中,加水80mL,配制成0.1000molL﹣1H2SO4溶液
C.图1所示装置可用于吸收NH3或HC1气体,并防止倒吸
D.实验室用图2所示装置除去Cl2中的少量HCl
查看答案和解析>>
科目: 来源: 题型:
【题目】某原电池总反应为:Cu+2Fe3+═Cu2++2Fe2+ , 下列能实现该反应的原电池是( )
A | B | C | D | |
电极材料 | Cu、Zn | Cu、Ag | Cu、C | Fe、Zn |
电解液 | FeCl3 | Fe2(SO4)3 | Fe(NO3)2 | CuSO4 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,向一个容积为2L的真空密闭容器中(事先装入催化剂)通入1 mol N2和3 mol H2,发生下列反应:N2+3H2![]() 2NH3,3 min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
2NH3,3 min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
A.0.2 mol·L-1·min-1 B.0.6 mol·L-1·min-1
C.0.1 mol·L-1·min-1 D.0.3 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com