
科目: 来源: 题型:
【题目】偏钒酸镁在化工“新型材料”光电领域有着重要的用途。以硼泥[主要成分是MgO(52.1%),还有Fe2O3、FeO、Al2O3、SiO2等杂质]为原料设计制备偏钒酸镁的生产工艺如图所示:
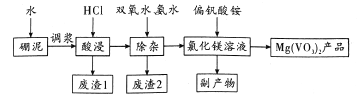
回答下列问题:
(l)Mg(VO3)2 中V的化合价为_____,副产物的电子式为_______。
(2)酸浸时,反应温度需控制在80℃,在实验室可采取的措施为______。写出”酸浸”后溶液中存在的金属阳离子_______,废渣1可用于制作_______,该物质在信息传输中具有重要应用。
(3)“除杂”过程加人双氧水的目的是_______(用离子方程式表示)。此过程中使Fe3+、Al3+浓度均小于l×10-6mol·L-1,在室温下需调节pH范围为__________[已知Ksp[Fe(OH)3]= 1×10-39, Ksp[Al(OH)]=1×10-33, pH=9.3时,Mg2+开始沉淀]。
(4)如何检验滤液中Fe3+是否被除尽,简述检验操作:__________。
(5)偏钒酸氨可由VOSO4溶液中加入氯酸钾将其氧化,然后用氨水调节pH即可制得,写出VO2+被氯酸钾氧化的离子方程式_________。
(6)现用a t硼泥生产Mg(VO3)2,若生产过程的产率为6%,则能生产出Mg(VO3)2产品的
质量为_________t (用含a、b的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硒(Se)是第4周期第ⅥA族元素,下列叙述不正确的是( )
A.硒是一种金属性很强的元素
B.硒可以形成SeO2和SeO3
C.硒的氢化物化学式为H2Se
D.硒的最高价氧化物对应水化物的化学式是H2SeO4
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[一lg c(M2+)]与溶液pH的变化关系如图所示,已知该温度下,Ksp[Cu(OH)2]2],下列说法正确的是 ( )

A. b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中:C(Fe2+):C(Cu2+):1:104.6
C. 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液
D. 除去CuSO4溶液中含有的少量Fe2+,可加入适量Cu0
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. AlCl3溶液和Al2(SO4)3溶液加热,蒸发,浓缩结晶,灼烧,所得固体的成分相同
B. 配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,后再加水稀释到所需的浓度
C. 向CuCl2溶液中加入CuO,调节pH可除去溶液中混有的Fe3+
D. 泡沫灭火器中常使用的原料是Na2CO3和Al2(SO4)3
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来AIST报告正在研制一种“高容量、低成本”的锂—铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH一,下列说法不正确的是 ( )

A. 放电时,Li+透过固体电解质向Cu极移
B. 放电时,正极的电极反应式为O2+2H2O+4e一=4OH—
C. 通空气时,铜被腐蚀,表面产生Cu2O
D. 通空气时,整个反应过程中,铜相当于是催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活、社会密切相关,下列有关说法正确的是
A. 古有“青蒿一握,以水二升渍,绞取汁”,今用乙醚从黄花蒿中可提取青蒿素是利用氧化还原反应原理
B. 食用“地沟油”对人体危害很大,但可以通过蒸馏的方式获得汽油、柴油等,实现资源的再利用。
C. 牛奶中加入果汁会产生沉淀,是因为发生了酸碱中和反应
D. CO2是大量使用的灭火剂,但着火的镁条在CO2中继续燃烧说明它也可以助燃
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应经常伴随着颜色变化。下列有关反应的颜色变化正确的是
A. 苯酚遇三氯化铁溶液变血红色
B. 淀粉溶液遇碘酸钾变蓝色
C. 植物油遇溴水变黄色
D. 氧化铜遇热的乙醇变红色
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,纯水中存在电离平衡:H2O![]() H++OH-。欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
H++OH-。欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
A. H2SO4 B. AlCl3
C. NaHCO3 D. NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次增大的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A. 原子半径:W>Z>Y>X>M
B. 常见气态氢化物的稳定性:X<Y<Z
C. 1 mol WM溶于足量水中完全反应,共转移2 mol电子
D. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com