
科目: 来源: 题型:
【题目】甲、乙两个密闭容器中均发生反应:C(s)+2H2O(g)![]() CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 平衡 常数 | |
C(s) | H2O(g) | H2(g) | ||||
甲 | 2 | T1 | 2.0 | 4.0 | 3.2 | K1 |
乙 | 1 | T2 | 1.0 | 2.0 | 1.2 | K2 |
下列说法正确的是( )
A. K1=12.8
B. T1<T2
C. T1℃时向甲容器中再充入0.1 mol H2O(g),则平衡正向移动,CO2(g)的体积分数增大
D. 若在T2温度下,向2 L密闭容器中充入1.0 mol CO2和2.0 mol H2,达平衡时,CO2的转化率小于40%
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 合成氨反应是放热反应,所以工业上采用低温条件以提高氨的产率
B. 钢铁水闸可用牺牲阳极或外加电流的阴极保护法延缓其腐蚀
C. Na2O2与水反应产生1 mol O2,理论上转移的电子数约为4×6.02×1023
D. 保持温度不变,向稀氨水中缓慢通入CO2,溶液中![]() 的值增大
的值增大
查看答案和解析>>
科目: 来源: 题型:
【题目】在废水处理、粗盐提纯等过程中通常会涉及离子检验、除杂等过程。
(1)某工厂废水只含Na+、K+、Cu2+、Ba2+、Mg2+、OH-、CO32-中的若干种。实验小组对废水进行了检测:
步骤1:对废水进行观察,废水为无色澄清液体。
步骤2:取少量废水,向水样中加入过量BaCl2溶液,有白色沉淀生成,静置。
步骤3:取少量步骤2所得上层清液,向其中滴加酚酞,溶液变红。
①由步骤1可得的结论是____。
②步骤2中所发生反应的离子方程式为___。
③实验中不能确定是否存在的离子是____。
④请设计实验方案对溶液中还未能确定的离子进行检测,方法是:___。
(2)某粗盐溶液经检测其中含有的杂质离子是Ca2+、Mg2+、Br-、SO42-。实验小组经过下列实验过程最终获得NaCl晶体:
步骤1:向溶液中加入试剂除去Ca2+、Mg2+和SO42-,过滤,向滤液中加入盐酸至无气泡产生。
步骤2:向步骤1所得溶液中通入适量的气体X,充分反应后加入CCl4,振荡后分液。
步骤3:将步骤2所得水层蒸发结晶。
①按使用顺序写出步骤1所用试剂的化学式:_____。
②步骤2中发生反应的离子方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关物质的转化关系如图所示。C为常见的调味品,D是常见的无色液体。E、F、H和J均为气体,其中H和J为单质,且两者在一定条件下可生成E。
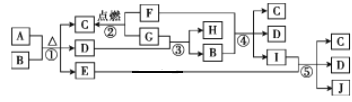
(1)物质的性质决定物质的用途。物质I的溶液可用作家用消毒剂、漂白液,是因为物质I具有__性。
(2)写出反应①的化学方程式:_____。
(3)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目:___。
(4)写出反应④的离子方程式:____。
(5)写出反应⑤的化学方程式:____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物X是一种用于合成γ分泌调节剂的药物中间体,其结构简式如右图所示。下列有关化合物X的说法正确的是( )
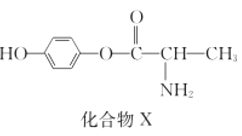
A. 化合物X分子中没有手性碳原子
B. 化合物X能与FeCl3溶液发生显色反应
C. 1 mol化合物X最多能与2 mol NaOH反应
D. 化合物X能发生水解反应,一定条件下可水解得到一种α氨基酸
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
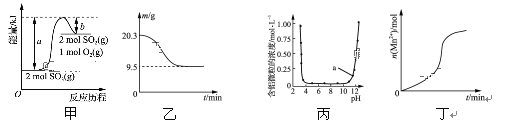
A. 由图甲可知,2SO3(g)![]() 2SO2(g)+O2(g) ΔH=(b-a)kJ·mol-1
2SO2(g)+O2(g) ΔH=(b-a)kJ·mol-1
B. 图乙表示0.1 mol MgCl2·6H2O在空气中充分加热时残留固体质量随时间的变化
C. 图丙表示Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中存在大量Al3+
D. 图丁表示10 mL 0.01 mol·L-1酸性KMnO4溶液与过量的0.1 mol·L-1的H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对反应有催化作用)
查看答案和解析>>
科目: 来源: 题型:
【题目】关于Zn+2HCl=ZnCl2+H2的反应,下列说法正确的是( )
A.单质Zn中Zn的化合价升高,被还原,是氧化剂
B.HCl中H的化合价降低,被氧化,HCl是还原剂
C.H2是还原产物
D.该反应是复分解反应,也是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】将1.60gCuSO4固体置于下图所示的装置(固定及夹持类仪器未画出)中加热到1100℃,使其分解,分解过程中可以观察到:石英管中固体由白色变为黑色,最终变为红色;BaCl2溶液中生成白色沉淀,品红溶液褪色,集气瓶中收集到无色气体。
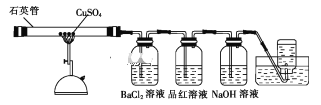
(1)石英主要成分的化学式是_____;高温分解CuSO4固体使用石英管而不使用普通玻璃管的原因是_____。
(2)石英管中剩余红色固体质量为0.72 g,经检测为不含硫元素的纯净物。则该固体的化学式为__。
(3)将BaCl2溶液中生成的白色沉淀过滤并洗涤,向洗涤后的沉淀中加入稀盐酸,无明显现象。
①沉淀的化学式为_____。
②检验沉淀是否洗净的方法是___。
(4)若NaOH溶液足量,则其中发生反应的离子方程式为____。
(5)集气瓶中收集的无色气体是____(填化学式),检验该气体的方法是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com