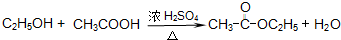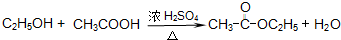(2009?清远模拟)为测定某有机化合物A的结构,进行如下实验.
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH
2O和8.8gCO
2,消耗氧气6.72L(标准状况下).则该物质中各元素的原子个数比是
n(C):n(H):n(O)=2:6:1
n(C):n(H):n(O)=2:6:1
;
(2)质谱仪测定有机化合物的相对分子质量为46,则该物质的分子式是
C2H6O
C2H6O
;
(3)根据价键理论,预测A的可能结构并写出结构简式
CH3CH2OH、CH3-O-CH3
CH3CH2OH、CH3-O-CH3
;
(4)有机物A分子中有三种不同化学环境的氢原子,则A的结构简式为
CH3CH2OH
CH3CH2OH
.
(5)A在一定条件下脱水可生成B,B可合成包装塑料C,请写出B转化为C的化学反应方程式:
.
(6)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉.请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应方程式:
.
(7)A可通过粮食在一定条件下制得,由粮食制得的A在一定温度下密闭储存,因为发生一系列的化学变化而变得更醇香.请写出最后一步反应的化学方程式:
.