
科目: 来源: 题型:
【题目】某兴趣小组探究SO2气体的还原性,装置如图所示,下列说法不合理的是
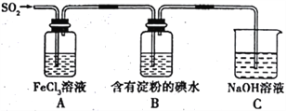
A. A装置中FeCl3溶液逐渐变为浅绿色,可以说明SO2有还原性
B. B装置中蓝色退去,说明还原性:SO2>I-
C. C装置中吸收尾气有可能倒吸
D. A、B装置中发生的反应转移电子数一定相等。
查看答案和解析>>
科目: 来源: 题型:
【题目】上世纪末,科学家研制得到一种新的分子,它具有空心的、类似足球的结构![]() 如图
如图![]() ,化学式为
,化学式为![]() ,下列说法中正确的是
,下列说法中正确的是![]()
![]()
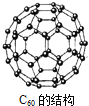
A. ![]() 是一种新型的化合物
是一种新型的化合物
B. ![]() 中含有离子键
中含有离子键
C. ![]() 和金刚石、石墨都是碳元素的不同单质
和金刚石、石墨都是碳元素的不同单质
D. ![]() 的摩尔质量为720
的摩尔质量为720
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在体积为5L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)

根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=__________,升高温度,K值_______(填“增大”、“诚小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=_____________。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是___________。
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,该反应使用催化剂的目的是_____________________。已知反应Cu2O+CO![]() 2Cu+CO2若原反应体系中含少量CO2________(填“有利于”“不利于”)维持催化剂Cu2O的量不变。请标出反应Cu2O+CO
2Cu+CO2若原反应体系中含少量CO2________(填“有利于”“不利于”)维持催化剂Cu2O的量不变。请标出反应Cu2O+CO![]() 2Cu+CO2电子转移的方向和数目:___________________________,标准状况下2.24LCO2参与反应,电子转移数为___________个。
2Cu+CO2电子转移的方向和数目:___________________________,标准状况下2.24LCO2参与反应,电子转移数为___________个。
查看答案和解析>>
科目: 来源: 题型:
【题目】中科院的科研人员在Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如下图。
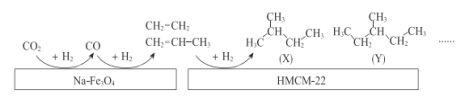
(1)Na-Fe3O4和HMCM-22 在反应中的作用为_______________
(2)(X)的系统命名的名称为_______________
(3)(Y)的一氯代物有_________________种
(4)(X)与(Y)的关系为 ________________
(5)在HMCM-22 表面生成摩尔质量为128g/mol且含两种氢的烷烃(Z),写出其结构简式___________,
(6)在HMCM-22 表面生成一种同温同压蒸气密度是氢气57倍且含有一种氢的烷烃(M),写出其与氯气反应生成一氯代烃的方程式______________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2(g)+2ICl(g)![]() I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
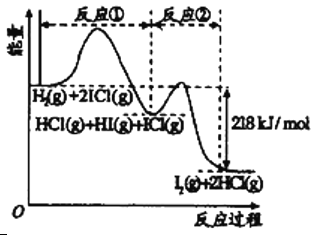
下列有关说法正确的是
A. 反应①为吸热反应
B. 反应①和②均是同种元素间发生的氧化还原反应
C. 反应①比反应②的速率慢,与图中相应峰高有关
D. HI(g)+ICl(g) ![]() I2(g)+HCl(g)生成1摩尔HCl放出218kJ的热量
I2(g)+HCl(g)生成1摩尔HCl放出218kJ的热量
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家屠呦呦因创造性地研制出抗疟新药青蒿素和双氢青蒿素(对疟原虫有100%的抑制率)而获2015年诺贝尔医学奖。如图为青蒿素的键线式,以下关于青蒿素的说法错误的是

A. 含有酯基,可水解
B. 含有过氧键,有较强氧化性,且不够稳定
C. 青蒿素的化学式C15 H24O5
D. 在水中溶解度不大,易溶于有机溶剂
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c0(X)、c0(Y)、c0(Z)(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c0(X)、c0(Y)、c0(Z)(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A. c0(X)∶c0(Y)=3∶1
B. 平衡时,Y和Z的生成速率之比为2∶3
C. X、Y的转化率不相等
D. c0(X)的取值范围为0 mol·L-1<c0(X)<0.14 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】锂-空气电池原理模型如图所示,下列说法不正确的是

A. 电池正极可以吸附空气中氧气作为氧化剂
B. 正极反应为2Li+ + O2 + 2e- ![]() Li2O2
Li2O2
C. 电解质能传递锂离子和电子,不可以用水溶液
D. 负极反应Li - e-=Li+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com