
科目: 来源: 题型:
【题目】(Ⅰ)如图中的A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。请填空:

(1)电源A的a为____极。
(2)滤纸B上发生的总反应方程式为___________________。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为_____________,电极f上发生的反应为____,槽中盛放的电镀液可以是____(只要求填一种电解质溶液)。
(Ⅱ)电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。
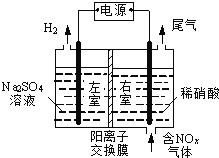
若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式_____________________。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为_____mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )

A. 若A是铁,则E可能为稀硝酸
B. 若A是CuO,E是碳,则B为CO
C. 若A是NaOH溶液,E是CO2,则B为NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关氯元素及其化合物的表示正确的是
A. 质子数为17、中子数为20的氯原子:2017ClB. 次氯酸的结构式:H-Cl-O
C. 氯分子的电子式:![]() D. 氯乙烯分子的结构简式:H3C—CH2Cl
D. 氯乙烯分子的结构简式:H3C—CH2Cl
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是某蛋白质的结构片段:

(1)上述蛋白质的结构片段的水解产物中不属于α氨基酸的结构简式是_____________________。
(2)上述蛋白质的结构片段水解后的氨基酸中,某氨基酸中碳、氢原子数比值最大。
①该氨基酸与NaOH反应的化学方程式为________________________。
②该氨基酸二分子缩合形成环状物质的分子式为_______________。
③该氨基酸的同分异构体中,属于硝基化合物且苯环上除硝基外只有甲基的同分异构体有________种。
(3)已知上述蛋白质结构片段的式量为364,则水解成的各氨基酸的式量之和为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知聚乳酸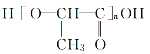 可在乳酸菌作用下分解,下列有关聚乳酸的说法正确的是( )
可在乳酸菌作用下分解,下列有关聚乳酸的说法正确的是( )
A. 聚乳酸是一种纯净物
B. 聚乳酸的单体是HO—CH2—CH2—COOH
C. 聚乳酸是由单体之间通过加聚而合成的
D. 聚乳酸是一种高分子材料
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)甲同学设计实验的依据是____________________________;写出对应装置中选用的物质:A_________,B__________,C___________;其中装置B中所盛试剂的作用为_____________;C中反应的离子方程式为___________________。
(2)乙同学的实验原理是_____________________________________;写出B处的离子方程式:________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ. CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+1/2O2(g) ![]() CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是______(填字母)。
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是______(填字母)。
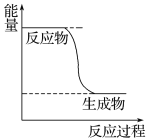
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C===O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速率v(H2)=________________,则CH3OH的转化率为___________。
Ⅱ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
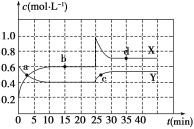
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示)______________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是___________。
Ⅲ.当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为________,负极的电极反应式为_______________________________。当反应中收集到标准状况下224 mL气体时,消耗的a电极质量为________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
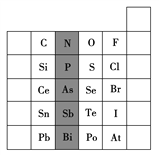
(1)阴影部分元素N在元素周期表中的位置为____周期第____族。根据元素周期律,预测酸性强弱:H3AsO4____H3PO4(填“>”或“<”)。
(2)S的最高化合价和最低化合价的代数和为____,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度____(填“更大”“更小”或“相同”)。
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是____。
(4)下列说法错误的是____(填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
①用物质 A 表示的反应的平均速率为 0.3 mol/(L·s)
②反应前容器内的压强与平衡后容器内的压强之比为1:1
③ 2 s 时物质A的转化率为30% ④ X="2"
其中正确的是
A. ①③④B. ①④C. ②③D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com