
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЬѕМўЯТЃЌжЦБИТШввЭщ(C2H5Cl)ЕФЗНЗЈгаЃКЂйгУввЭщгыТШЦјЗДгІЃЛЂкгУввЯЉгыТШЛЏЧтЗДгІЃЌСНжжЗНЗЈжаФФвЛжжвЊИќКУЃЌаДГіЛЏбЇЗНГЬЪН________ЃЌИУЗДгІЕФРраЭЪЧ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЖЯПЊ1molHЁЊHМќЁЂ1molNЁдNЁЂ1molNЁЊHМќЗжБ№ашвЊЮќЪеЕФФмСПЮЊ436kJЁЂ946kJЁЂ391kJЁЃдђгЩN2КЭH2ЗДгІЩњГЩ1 molNH3ашвЊ_____ЃЈЬюЁАЗХГіЁБЛђЁАЮќЪеЁБЃЉ____kJЕФФмСП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЦЛЙћДзЪЧвЛжжгЩЦЛЙћЗЂНЭЖјаЮГЩЕФОпгаНтЖОЁЂНЕжЌЁЂМѕЗЪЕШУїЯдвЉаЇЕФНЁПЕЪГЦЗЁЃЦЛЙћЫс(2ЃєЧЛљЖЁЖўЫс)ЪЧетжжвћСЯЕФжївЊЫсадЮяжЪЃЌЦЛЙћЫсЕФНсЙЙМђЪНЮЊ![]() ЁЃЯТСаЯрЙиЫЕЗЈВЛе§ШЗЕФЪЧ(ЁЁЁЁ)
ЁЃЯТСаЯрЙиЫЕЗЈВЛе§ШЗЕФЪЧ(ЁЁЁЁ)
A. ЦЛЙћЫсдквЛЖЈЬѕМўЯТФмЗЂЩњДпЛЏбѕЛЏЗДгІ
B. 1 molЦЛЙћЫсгызуСПNaHCO3ШмвКЗДгІЯћКФ2 mol NaHCO3
C. 1 molЦЛЙћЫсгызуСПNaЗДгІЩњГЩ33.6 L H2(БъзМзДПіЯТ)
D. 1 molЦЛЙћЫсЗжБ№КЭзуСПNaЛђNaOHЗДгІЯћКФСНепЮяжЪЕФСПЯрЕШ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСђЫсЙЄвЕжаЗЯдќЕФГЩЗжЮЊSiO2ЁЂFe2O3ЁЂAl2O3ЁЂMgOЁЃ ФГЬНОПадбЇЯАаЁзщЕФЭЌбЇЩшМЦвдЯТЪЕбщЗНАИЃЌНЋСђЫсдќжаН№ЪєдЊЫиЗжБ№зЊЛЏЮЊЧтбѕЛЏЮяГСЕэЖјЗжРыПЊРДЁЃ
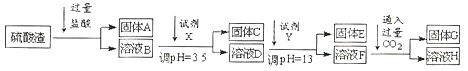
вбжЊГЃЮТЯТЃЌВПЗжбєРызгвдЧтбѕЛЏЮяаЮЪНГСЕэЪБШмвКЕФpHШчЯТЃК
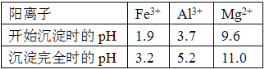
ЃЈ1ЃЉЙЄвЕЩЯгУЙЬЬхAзїдСЯжЦШЁЫЎВЃСЇЕФЛЏбЇЗНГЬЪНЮЊ_________ЁЃ
ЃЈ2ЃЉЙЬЬхEЕФЛЏбЇЪНЮЊ_________ЁЃ
ЃЈ3ЃЉЪЕбщЪвгУ11.9mol/LЕФХЈбЮЫсХфжЦ250mL3.0mol/LЕФЯЁбЮЫсЃЌЫљгУЕФВЃСЇвЧЦїГ§ЩеБЁЂВЃСЇАєКЭСПЭВЭтЃЌЛЙашвЊ_______ЁЃ
ЃЈ4ЃЉЩЯЪіСїГЬжаЕФЪдМСYзюКУбЁгУЯТСажаЕФ_______ЃЈбЁЬюзжФИБрКХЃЉЁЃ
AЃЎЫЎ BЃЎСђЫс CЃЎАБЫЎ DЃЎЧтбѕЛЏФЦ
ЃЈ5ЃЉаДГіЗДгІFЁњHЕФРызгЗНГЬЪН_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдСЖаПГЇЕФЭягЗЯдќжаИїдЊЫиНјааЗжРыЃЌФмМѕЩйЛЗОГЮлШОЃЌЭЌЪБжЦЕУЪГЦЗаПЧПЛЏМСЕФдСЯZnSO4ЁЄ7H2OЪЕЯжзЪдДЕФдйРћгУЁЃЦфСїГЬЭМШчЯТЁЃ

[ЯрЙизЪСЯ]
ЂйЭягЗЯдќжаКЌгаЭЁЂаПЁЂягЁЂЬњЁЂЩщЕШдЊЫиЃЌЦфКЌСПвРДЮМѕЩйЁЃ
ЂкFeAsO4ФбШмгкЫЎЃЛZnSO4ЁЄ7H2OвзШмгкЫЎЃЌФбШмгкОЦОЋЁЃ
ЂлZn(OH)2ЪєгкСНадЧтбѕЛЏЮяЁЃ
ЂмТЫвКIжагаFe2ЃЋЁЂZn2ЃЋЁЂCu2ЃЋЁЂCd2ЃЋКЭЩйСПЕФAsO![]() ЁЃ
ЁЃ
ЂнгаЙиРызгГСЕэЭъШЋЕФpH
Н№ЪєРызг | Fe3ЃЋ | Zn2ЃЋ | Mn2ЃЋ | Cu2ЃЋ | Cd2ЃЋ |
ГСЕэЭъШЋpH | 3.2 | 8.0 | 9.8 | 6.4 | 9.4 |
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЬсИпЭягЗЯдќНўГіТЪПЩвдВЩгУЕФЗНЗЈЪЧЃЈаДГіЦфжавЛЕуМДПЩЃЉ____ЃЛ
ЃЈ2ЃЉЯђТЫвКIжаж№ЕЮЕЮШЫЫсадKMnO4ШмвКПЩгыAsO![]() ЗЂЩњЗДгІЩњГЩFeAsO4ЃЌаДГіИУЗДгІЕФРызгЗНГЬЪН____ЃЛМгШыЫсадKMnO4ШмвКВЛФмЙ§СПЃЌХаЖЯИУЕЮЖЈжеЕуЕФЯжЯѓЪЧ____ЃЛТЫдќЂђжаГ§СЫFeAsO4ЭтЃЌЛЙга____ЃЛ
ЗЂЩњЗДгІЩњГЩFeAsO4ЃЌаДГіИУЗДгІЕФРызгЗНГЬЪН____ЃЛМгШыЫсадKMnO4ШмвКВЛФмЙ§СПЃЌХаЖЯИУЕЮЖЈжеЕуЕФЯжЯѓЪЧ____ЃЛТЫдќЂђжаГ§СЫFeAsO4ЭтЃЌЛЙга____ЃЛ
ЃЈ3ЃЉжЦЕУЕФZnSO4ЁЄ7H2OашЯДЕгЃЌЯДЕгОЇЬхЪБгІбЁгУЪдМСЮЊ____ЃЛ
ЃЈ4ЃЉЩЯЪіСїГЬГ§СЫЪЕЯжЖдетаЉдЊЫиНјааЬсШЁЗжРыФмМѕЩйЛЗОГЮлШОЃЌЭЌЪБжЦЕУZnSO4ЁЄ7H2OЪЕЯжзЪдДЕФдйРћгУЃЌЛЙПЩвдЕУЕНИБВњЮя___
ЃЈ5ЃЉЛиЪеЫљЕУЕФCdПЩгУгкжЦдьФјягМюадЖўДЮЕчГиЃЌЕчГиЕФЙЄзїЪБЃЌе§МЋNiO(OH)зЊЛЏЮЊNi(OH)2ЃЌдђГфЕчЪБЕчГиЕФе§МЋЗДгІЪНЮЊ____ЃЛ
ЃЈ6ЃЉШєaПЫЭягЗЯдќКЌгаb molFeдЊЫиЃЌМгШыСЫc mol KMnO4,дђЭягЗЯдќжаAsдЊЫиЕФжЪСПЗжЪ§ЮЊ____ЁЃЃЈВЛПМТЧягдЊЫигыKMnO4ЕФЗДгІЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдгкУмБеШнЦїжаЕФЗДгІ2SO3(g)![]() O2(g)ЃЋ2SO2(g)ЃЌдквЛЖЈЬѕМўЯТn(SO3)КЭn(O2)ЫцЪБМфБфЛЏЕФЙиЯЕШчЭМЫљЪОЁЃЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
O2(g)ЃЋ2SO2(g)ЃЌдквЛЖЈЬѕМўЯТn(SO3)КЭn(O2)ЫцЪБМфБфЛЏЕФЙиЯЕШчЭМЫљЪОЁЃЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
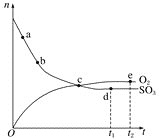
A. ЕуcДІЗДгІДяЕНЦНКтB. ЕуbЕФе§ЗДгІЫйТЪБШЕуaЕФДѓ
C. ЕуcЕФФцЗДгІЫйТЪБШЕуeЕФДѓD. Еуd(t1ЪБПЬ)КЭЕуe(t2ЪБПЬ)ДІn(SO2)вЛбљДѓ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧ(NAЮЊАЂЗќМгЕТТоГЃЪ§)(ЁЁЁЁ)
A. 12 gЪЏФЋжаКЌгаCЁЊCМќЕФИіЪ§ЮЊ1.5 NA
B. 12 gН№ИеЪЏжаКЌгаCЁЊCМќЕФИіЪ§ЮЊ4 NA
C. 60 g SiO2жаКЌгаSiЁЊOМќЕФИіЪ§ЮЊ2 NA
D. 124 g P4жаКЌгаPЁЊPМќЕФИіЪ§ЮЊ4 NA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙтЛЏбЇбЬЮэЪЧЦћГЕЮВЦјдкзЯЭтЯпзїгУЯТЩњГЩЕФгаКІЧГРЖЩЋбЬЮэЃЌгЩЕЊЕФбѕЛЏЮяКЭЬўРрЕШвЛДЮЮлШОЮяЃЌгыЫќУЧЗЂЩњвЛЯЕСаЙтЛЏбЇЗДгІЩњГЩЕФГєбѕЁЂШЉРрЁЂЙ§бѕввѕЃЯѕЫсѕЅ(PAN)ЕШЖўДЮЮлШОЮязщГЩЁЃЙтЛЏбЇбЬЮэЕМжТблОІМАеГФЄЪмДЬМЄЃЌв§ЗЂКєЮќЕРМВВЁЃЌбЯжиЪБЪЙШЫЭЗЭДЁЂХЛЭТЃЌЩѕжСЫРЭіЁЃЯТСаа№ЪіжаДэЮѓЕФЪЧЃЈ ЃЉ

A. ЙтЛЏбЇбЬЮэЕФЗжЩЂМСЮЊПеЦј
B. NO2ЮЊЫсадбѕЛЏЮя
C. O2зЊЛЏГЩO3ЕФЗДгІЮЊЗЧбѕЛЏЛЙдЗДгІ
D. ЦћГЕНкФмМѕХХДыЪЉПЩвдЛКНтЙтЛЏбЇбЬЮэДјРДЕФЮлШО
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдгкБНввЯЉЃЈ![]() ЃЉгаЯТСаа№ЪіЃКЂй ФмЪЙЫсадKMnO4ШмвКЭЪЩЋЃЛЂк ФмЪЙфхЕФЫФТШЛЏЬМШмвКЭЪЩЋЃЛЂл ПЩШмгкЫЎЃЛЂм ПЩШмгкБНжаЃЛЂн ФмгыХЈЯѕЫсЗЂЩњШЁДњЗДгІЃЛЂо ЫљгаЕФдзгПЩФмЙВЦНУцЁЃЦфжае§ШЗЕФЪЧЃЈ ЃЉ
ЃЉгаЯТСаа№ЪіЃКЂй ФмЪЙЫсадKMnO4ШмвКЭЪЩЋЃЛЂк ФмЪЙфхЕФЫФТШЛЏЬМШмвКЭЪЩЋЃЛЂл ПЩШмгкЫЎЃЛЂм ПЩШмгкБНжаЃЛЂн ФмгыХЈЯѕЫсЗЂЩњШЁДњЗДгІЃЛЂо ЫљгаЕФдзгПЩФмЙВЦНУцЁЃЦфжае§ШЗЕФЪЧЃЈ ЃЉ
A. ЂйЂкЂлЂмЂн B. ЂйЂкЂнЂо C. ЂйЂкЂмЂнЂо D. ШЋВПе§ШЗ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЬњКЭюмЪЧСНжжживЊЕФЙ§ЖЩдЊЫиЁЃ
ЃЈ1ЃЉюмЮЛгкдЊЫижмЦкБэЕУЕк_____________зхЃЌЦфЛљЬЌдзгжаЮДГЩЖдЕчзгЕФИіЪ§ЮЊ______ЁЃ
ЃЈ2ЃЉ[Fe(H2NCONH2)]6(NO3)3ЕФУћГЦЪЧШ§ЯѕЫсСљФђЫиКЯЬњЃЈЂѓЃЉЃЌЪЧвЛжжживЊЕФХфКЯЮяЁЃИУЛЏКЯЮяжаFe3+ЕФКЫЭтЕчзгХХВМЪНЮЊ____________________ЃЌЫљКЌЗЧН№ЪєдЊЫиЕФЕчИКадгЩДѓЕНаЁЕФЫГађЪЧ____________________ЁЃ
ЃЈ3ЃЉФђЫиЗжзгжаЁЂЬМдзгЮЊ________дгЛЏЃЌЗжзгжаІвМќгыІаМќЕФЪ§ФПжЎБШЮЊ____________________ЁЃ
ЃЈ4ЃЉFeOОЇЬхгыNaClОЇЬхНсЙЙЯрЫЦЃЌБШНЯFeOгыNaClЕФОЇИёФмДѓаЁЃЌЛЙашвЊжЊЕРЕФЪ§ОнЪЧ______ЁЃ
ЃЈ5ЃЉCo(NH3)5BrSO4ПЩаЮГЩСНжжюмЕФХфКЯЮяЃЌНсЙЙЗжБ№ЮЊ[Co(NH3)5Br]SO4КЭ[Co(SO4)(NH3)5]BrЁЃвбжЊCo3ЃЋЕФХфЮЛЪ§ЪЧ6ЃЌЮЊШЗЖЈюмЕФХфКЯЮяЕФНсЙЙЃЌЯжЖдСНжжХфКЯЮяНјааШчЯТЪЕбщЃКдкЕквЛжжХфКЯЮяШмвКжаМгЯѕЫсвјШмвКВњЩњАзЩЋГСЕэЃЌдкЕкЖўжжХфКЯЮяШмвКжаМгШыЯѕЫсвјШмвКВњЩњЕЛЦЩЋГСЕэЁЃдђЕкЖўжжХфКЯЮяЕФХфЬхЮЊ____________________ЁЃ
ЃЈ6ЃЉАТЪЯЬхЪЧЬМШмНтдкІУЃFeжааЮГЩЕФвЛжжМфЯЖЙЬШмЬхЃЌЮоДХадЃЌЦфОЇАћЮЊУцаФСЂЗННсЙЙЃЌШчЯТЭМЫљЪОЃЌдђИУЮяжЪЕФЛЏбЇЪНЮЊ____________________ЁЃШєОЇЬхУмЖШЮЊdgЁЄcm3ЃЌдђОЇАћжазюНќЕФСНИіЬМдзгЕФОрРыЮЊ____________________pmЃЈАЂЗќйЄЕТТоГЃЪ§ЕФжЕгУNAБэЪОЃЌаДГіМђЛЏКѓЕФМЦЫуЪНМДПЩЃЉЁЃ

ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com