
科目: 来源: 题型:
【题目】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾 (K2Cr2O7),其工艺流程及相关物质溶解度曲线如下图所示。
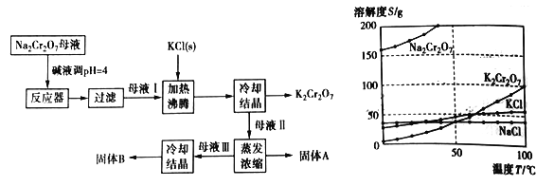
(1)向Na2Cr2O7母液中加碱液调pH的目的是_____________________。
(2)通过冷却结晶析出大量K2Cr2O7的原因是________________________________。
(3)固体A的主要成分为__________(填化学式),用热水洗涤固体A,回收的洗涤液转移到母液___________(填“I”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能耗降低。固体B的主要成分为___________________(填化学式)。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.500 g 配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-l H2SO4溶液和足量KI溶液(铬的还原产物为Cr3+),放置于暗处5 min,然后加入100 mL蒸馏水、3 mL 淀粉指示剂,用0.1200 mol·L-l Na2S2O3标准溶液滴定(已知I2+ 2S2O32-=2I-+S4O62-)。
①酸性溶液中KI 与K2Cr2O7反应的离子方程式为_____________________________。
②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为__________%( 保留2 位小数,设整个过程中其他杂质不参与反应)。进一步提纯产品的方法是___________________。
(5)+6价Cr的毒性很高,工业上用电解法来处理含Cr2O72-的废水。下图为电解装置示意图,电极材料分别为铁和石墨。通电后,Cr2O72-在b极附近转变为Cr3+,一段时间后Cr3+最终可在a 极附近变成Cr(OH)3沉淀而被除去。

①在以上处理过程中,Cr2O72-转化为毒性较低的Cr3+的离子方程式为________________________。
②a电极的电极反应式是是____________________;电解一段时间后在阴极区有Fe(OH)3和Gr(OH)3沉淀生成,若电解后的溶液中c(Cr3+)为3×10-5mol·L-1,则溶液中c(Fe3+)为____________ mol·L-1。已知:Ksp=[Fe(OH)3]=4.0×10-38,K[Cr(OH)3]=6.0×10-31。
【答案】 除去Fe3+ 低温下K2Cr2O7的溶解度远小于其他组分,且随温度的降低,K2Cr2O7的溶解度明显减小 NaCl Ⅱ K2Cr2O7 Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O 94.08 重结晶 Cr2O72-+6Fe2++ 14H+=2Cr3++6Fe3++7H2O 2H++2e-=H2↑ 2×10-12
【解析】考查化学工艺流程,(1)根据题目信息,母液中含有少量的Fe3+,加碱液的目的是除去Fe3+;(2)根据温度与溶解度的关系,K2Cr2O7的溶解度受温度的影响较大,低温时K2Cr2O7的溶解度远小于其他组分,且温度降低,K2Cr2O7的溶解度受温度的影响较大;(3)母液I中加入KCl,发生Na2Cr2O7+KCl=K2Cr2O7+NaCl,采用冷却降温得到K2Cr2O7固体,即母液II中含有大量的NaCl,因此蒸发浓缩得到的固体是NaCl;冷却结晶中有大量的K2Cr2O7析出,但溶液中含有少量的K2Cr2O7,蒸发浓缩时,NaCl表面附着一部分K2Cr2O7,为了提高产率又可使能耗降低,因此需要把洗涤液转移到母液II中,达到类似富集的目的;因此固体B的主要成分是K2Cr2O7;(4)①根据操作,得出K2Cr2O7作氧化剂,本身被还原成Cr3+,I-被氧化成I2,因此有Cr2O72-+I-→Cr3++I2,然后采用化合价升降法、原子守恒配平即可,离子方程式为Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;②根据离子方程式,得出关系式为Cr2O72-~3I2~6S2O32-,则求出样品中K2Cr2O7的质量为 =2.352g,纯度为2.352/2.500×100%=94.08%;进一步提纯需要重新溶解,冷却结晶,此方法叫重结晶;(5)①b电极为阳极,应是失去电子,化合价应升高,而Cr2O72-中Cr的化合价降低,因此b电极为铁,此电极反应式为Fe-2e-=Fe2+,然后利用Cr2O72-的氧化性,与Fe2+发生反应,离子反应方程方式为Cr2O72-+6Fe2++ 14H+=2Cr3++6Fe3++7H2O;②根据①的分析,a电极为阴极,电极反应式为2H++2e-=H2↑;Cr3+和Fe3+共存在同一溶液中,因此有
=2.352g,纯度为2.352/2.500×100%=94.08%;进一步提纯需要重新溶解,冷却结晶,此方法叫重结晶;(5)①b电极为阳极,应是失去电子,化合价应升高,而Cr2O72-中Cr的化合价降低,因此b电极为铁,此电极反应式为Fe-2e-=Fe2+,然后利用Cr2O72-的氧化性,与Fe2+发生反应,离子反应方程方式为Cr2O72-+6Fe2++ 14H+=2Cr3++6Fe3++7H2O;②根据①的分析,a电极为阴极,电极反应式为2H++2e-=H2↑;Cr3+和Fe3+共存在同一溶液中,因此有 ,解得c(Fe3+)=2.0×10-12mol·L-1。
,解得c(Fe3+)=2.0×10-12mol·L-1。
点睛:氧化还原反应方程式的书写是学生的一个难点,学生往往找不出反应物或生成物,或者溶液的环境选错,这是对题的理解上不透彻,如本题的(5)①根据信息,Cr2O72-在b极附近转变为Cr3+,b极为阳极,阳极上失去电子化合价升高,而现在Cr的化合价降低,因此只能说明b极的材料是Fe,Fe-2e-=Fe2+,然后还原Cr2O7-,因此有Cr2O72-+Fe2+→Fe3++Cr3+,根据化合价升降法进行配平,即Cr2O72-+6Fe2+→2Cr3++6Fe3+,Fe2+、Fe3+、Cr3+不与OH-大量共存,因此溶液显酸性,根据反应前后所带电荷数守恒、原子守恒进行配平即可。
【题型】综合题
【结束】
10
【题目】“低碳经济”正成为科学家研究的主要课题,为了减少空气中的温室气体,并且充分利用二氧化碳资源,科学家们设想了一系列捕捉和封存二氧化碳的方法。
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式如下:
6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ΔH=-76.0 kJ·mol-1
①上述反应中每生成1 mol Fe3O4,转移电子的物质的量为_______mol。
②已知:C(s)+2H2O(g)=CO2(g)+2H2(g) △H=+113.4kJ·mol-1,则反应:3FeO(s)+ H2O(g)= Fe3O4(s)+ H2(g)的△H=__________。
(2)用氨水捕集烟气中的CO2生成铵盐是减少CO2排放的可行措施之一。
①分别用不同pH的吸收剂吸收烟气中的CO2,CO2脱除效率与吸收剂的pH关系如图所示,若烟气中CO2的含量(体积分数)为12%,烟气通入氨水的流量为0.052 m3·h-1(标准状况),用pH为12.81的氨水吸收烟气30min,脱除的CO2的物质的量最多为____________(精确到0.01)。

②通常情况下温度升高,CO2脱除效率提高,但高于40℃时,脱除CO2效率降低的主要原因是______________。
(3)一定条件下,Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图所示。

①该反应的化学方程式为______________________;反应过程中碳元素的化合价为-2价的中间体是_________________。
②向一容积为2 L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2:0.2 mol·L-1、H2:0.8 mol·L-1、CH4:0.8 mol·L-1、H2O:1.6 mol·L-1,CO2的平衡转化率为_________________;300℃时上述反应的平衡常数K=___________________。
③已知该反应正反应放热,现有两个相同的恒容绝热(与外界无热量交换)密闭容器Ⅰ、Ⅱ,在Ⅰ中充入1molCO2和4molH2,在Ⅱ中充入1molCH4和2molH2O(g),300℃下开始反应。达到平衡时,下列说法正确的是
A.容器Ⅰ、Ⅱ中正反应速率相同
B.容器Ⅰ、Ⅱ中CH4的物质的量分数相同
C.容器Ⅰ中CO2的物质的量比容器Ⅱ中的多
D.容器Ⅰ中CO2的转化率与容器Ⅱ中CH4的转化率之和小于1
查看答案和解析>>
科目: 来源: 题型:
【题目】亚氯酸钠(NaClO2)在溶液中会生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都是具有漂白作用。已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是

A. HClO2的电离平衡常数的数值Ka=10-8
B. pOH=11时,ClO2-部分转化成ClO2和Cl-离子的方程式为:5ClO2-+2H2O=4ClO2+ Cl-+4OH-
C. pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有:c(Na+)+c(OH-)=c(H+)+ c(HClO2)
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年7月报道,南开大学科研团队在“可充室温钠-二氧化碳电池”的研究中取得突破进展,该电池放电时工作情况如图所示。下列说法错误的是

A. 金属Na为电池的负极
B. 放电时,电解液中Na+向碳电极移动
C. 充电时,碳电极发生的反应为:4Na++4e-+3CO2== 2Na2CO3+C
D. 放电时,每转移2 mol电子,消耗标准状况下的CO2 33.6 L
查看答案和解析>>
科目: 来源: 题型:
【题目】698K时,向VL的密闭容器中充入2molH2(g)和2molI2(g),发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH=-26.5kJ·mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。
2HI(g) ΔH=-26.5kJ·mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。
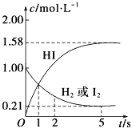
请回答下列问题:
(1)V=______。
(2)该反应达到最大限度的时间是_______,该时间内平均反应速率v(HI)=________。
(3)下列说法中可以说明反应2HI(g)![]() H2(g)+I2(g)已达到平衡状态的是_____。
H2(g)+I2(g)已达到平衡状态的是_____。
A.单位时间内生成nmolH2的同时生成2nmolHI
B.温度和体积一定时,容器内压强不再变化
C.条件一定,混合气体的平均相对分子质量不再变化
D.温度和压强一定时,混合气体的密度不再变化
(4)该反应达到平衡状态时,__________(填“吸收”或“放出”)的热量为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用,它的有效成分是下列物质的一种,这种物质是( )
A.Ca(ClO)2B.Na2O2C.H2O2D.NaClO
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,对于可逆反应A2(g)+3B2(g)![]() 2AB3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是
2AB3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是
A.恒容容器内混合气体的密度不再变化
B.AB 3的生成速率与B2的生成速率之比为2∶3
C.恒压容器内混合气体的总物质的量不再变化
D.单位时间内断裂a mol A≡A键,同时断裂6a mol A—B键
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W四种物质在一定条件下具有如下图所示的转化关系,下列判断错误的是

A. 若图中反应均为非氧化还原反应,当W为一元强碱时,则Z可能是NaAlO2
B. 若图中反应均为氧化还原反应,当W为非金属单质时,则Z可能是CO2
C. 若图中反应均为非氧化还原反应,当W为一元强酸时则X可能是NH3
D. 若图中反应均为氧化还原反应,当W为金属单质时,则Z可能是FeCl2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
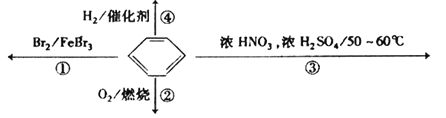
A. 反应![]() 为取代反应,有机产物的密度比水小
为取代反应,有机产物的密度比水小
B. 反应![]() 为取代反应,有机产物是一种烃
为取代反应,有机产物是一种烃
C. 反应![]() 中1mol苯最多与
中1mol苯最多与![]() 发生加成反应,是因为苯分子含有三个碳碳双键
发生加成反应,是因为苯分子含有三个碳碳双键
D. 反应![]() 为氧化反应,反应现象是火焰明亮并带有较多的黑烟
为氧化反应,反应现象是火焰明亮并带有较多的黑烟
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F均为短周期主族元素,且原子序数依次递增。A的原子核内无中子,B的原子最外层电子数是次外层电于数的2倍,C是地壳中含量最多的元素,D是短周期中金属性最强的元素,E与F位置相邻,F是同周期元素中原子半径最小的元素。
完成下列填空题:
(1)B在元素期表中的位置为_______,1个C原子核外有____个未成对的电子。
(2)D、E、F三种元素形成简单离子其半径由l大到小的顺序是_____________。(用离子符号表示)。
(3)写出D与C形成化合物的电子式______、_______。
(4)常温下,1molA的单质在C的单质中完全燃烧生成液态化合物,并放出286kJ的热量,该反应的热化学方程式为______________。
(5)非金属性的强弱:E_____F(填“强于”、“弱于”、“无法比较”),试从原子结构的角度解释其原因________________。
(6)Na2SO3可用作漂白织物时的去鼠剂。Na2SO3溶液及收Cl2后,溶液的酸性增强。写出该反应的离子方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com