
科目: 来源: 题型:
【题目】下列说法正确的是
A. 某种具有较好耐热性、耐水性和高频电绝缘性的高分子化合物的结构片段如下图,该树脂可由3种单体通过缩聚反应制备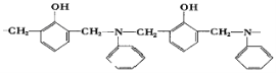
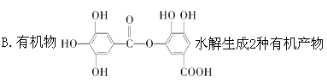
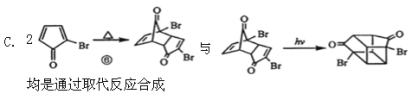
D.已知 ![]() ,合成
,合成![]() 所用的起始原料只能是2甲基1,3丁二烯和2丁炔
所用的起始原料只能是2甲基1,3丁二烯和2丁炔
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=___________,已知:K(300 ℃)>K(350 ℃),该反应的逆反应是_______反应(填“放热”或“吸热”)。
(2)图中表示NO2的变化的曲线是____________,用O2的浓度变化表示从0~2 s内该反应的平均速率v=_____________。
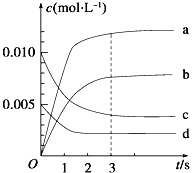
(3)能说明该反应已经达到平衡状态的是________。
a v(NO2)=2v(O2) b 容器内压强保持不变
c v逆(NO)=2v正(O2) d 容器内物质的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a 及时分离出NO2气体 b 适当升高温度
c 选择高效的催化剂 d 增大O2的浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O],俗名莫尔盐,蓝绿色的固体,易溶于水,几乎不溶于乙醇,在 100℃~110℃时分解,对光敏感。在空气中逐渐风化及氧化。在空气中比硫酸亚铁稳定,有还原性。常用作重铬酸钾、高锰酸钾等溶液的互相标定的标准物质。一般用废铁屑经以下流程制取:

(1)检验莫尔盐固体中亚铁离子,可将样品溶于水后,滴加 K3[Fe(CN)6]溶液,反应的现象是________________。
(2)下列说法中正确的有____。
A.用 NaOH 溶液洗涤废铁屑的作用是去除废铁屑表面的油污和氧化铁杂质
B.蒸发应用小火小心加热,直到出现大量晶体停火利用余热蒸干溶剂
C.过滤后可用少量乙醇洗涤
D.检验莫尔盐固体样品中铵离子,可将样品溶于水后,再加足量 NaOH 稀溶液,将湿润的红色石蕊试纸置于试管口,若观察到试纸变蓝,表明固体中存在 NH4+,否则无 NH4+
E.检验莫尔盐固体是否氧化变质,可将样品溶于水后,滴加 KSCN 溶液,溶液变红,说明氧化变质
(3)用重铬酸钾溶液标定(滴定)莫尔盐溶液浓度,若需配制浓度为 0.01000molL-1 的 K2Cr2O7 标准溶液 250mL,应准确称取____________________g K2Cr2O7(保留 4 位有效数字,已知 M( K2Cr2O7)=294.0gmol-1).配制该标准溶液时,下列仪器中不必要用到的有__________________ .
①电子天平 ②烧杯 ③温度计 ④玻璃棒 ⑤容量瓶⑥铁架台(带铁圈) ⑦胶头滴管
滴定操作中,如果滴定前装有 K2Cr2O7 标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将____(填“偏大”、“偏小”或“不变”)。
(4)向(NH4)2Fe(SO4)2 溶液中滴加一定量的 NaOH 溶液时,发生的总反应的离子方程式一定错误的是____。(填字母)
A.Fe2++2OH-===Fe(OH)2↓
B.NH4++OH-===NH3·H2O
C.Fe2++3OH-+NH4+===Fe(OH)2↓+NH3·H2O
D.Fe2++5OH-+3NH4+===Fe(OH)2↓+3NH3·H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】认真观察下列装置,回答下列问题:
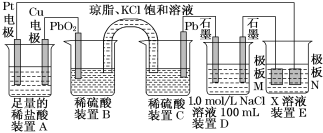
(1)装置B中PbO2上发生的电极反应方程式为________________
(2)装置A中总反应的离子方程式为_____________________________。
(3)若装置E中的目的是在Cu材料上镀银,则X为________,极板N的材料为________。
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为________L(标准状况下)。
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。
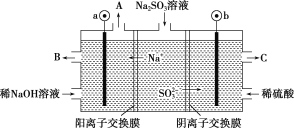
①图中a极连接电源的___________极,
②b极电极反应式为____________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分。

已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):
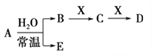
(1)元素⑧的最高价氧化物对应水化物的化学式是_________________________。
(2)元素⑤与As两种元素中,简单气态氢化物较稳定的是___________(填化学式)。
(3)元素②⑥⑦的简单离子半径由大到小的顺序是___________(用化学符号表示)。
(4)元素③的单质与元素②的最高价氧化物对应的水化物反应的离子方程式是________________。
(5)若A为红棕色气体,则X、D的化学式分别为___________、___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知亚硫酸钠隔绝空气加热到 600℃可以分解,实验流程如下图(所得气体是纯净物):
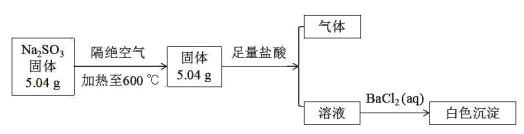
(1)硫元素在元素周期表中的位置_________________亚硫酸钠中含有的化学键类型 _________________ .
(2)写出亚硫酸钠受热分解的化学方程式 _________________ .
(3)下列说法正确的是 _________________ .
A.加热分解后的固体中氧元素质量为 1.92 克
B.生成白色沉淀的物质的量 0.04mol
C.分解后固体溶于水后,溶液中离子浓度大小顺序为c(Na+)> c(SO42-)>c(S2-)>c(OH-)>c(HS-)>c(H+)
D.将适量亚硫酸钠与分解后的固体混合,再加稀盐酸可能会出现沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有机合成设计中,所涉及的反应类型有错误的是
A. 由丙醛制 1,2﹣丙二醇:第一步还原,第二步消去,第三步加成,第四步取代
B. 由1-溴丁烷制1,3-丁二烯:第一步消去,第二步加成,第三步消去
C. 由乙炔合成苯酚:第一步三聚,第二步取代,第三步水解,第四步中和
D. 由![]() 制
制![]() :第一步加成,第二步消去,第三步加成,第四步取代
:第一步加成,第二步消去,第三步加成,第四步取代
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:Al、Fe、Cu 的合金与稀硝酸反应生成的气体只有 NO,实验过程如下:
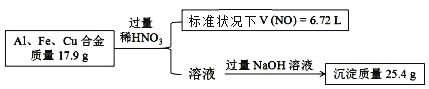
另取等量该合金,溶于足量 NaOH (aq),则可得气体的物质的量是
A. 0.22 mol B. 0.15 mol C. 0.3 mol D. 无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com