
科目: 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:

已知石油裂解已成为生产H的主要方法,E的溶液能发生银镜反应,G是具有香味的液体,试回答下列问题。
(1)F中所含官能团的名称是_____________________________________。
(2)G的结构简式为___________________________。
(3)写出D→E的化学方程式,并注明反应类型:____________________________。
(4)F→G的反应装置如图所示:

a.图中倒置球形干燥管的作用_____________________________;
b.试管Ⅱ中加有饱和Na2CO3溶液,其作用是: ____________________;
c.具有一个羟基的化合物M 10 g,与F反应生成产物11.85 g,并回收了未反应的M 1.3 g,则M的相对分子质量为____;
(5)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ,再测有机物层的厚度,实验记录如下:
实验编号 | 试管Ⅰ中试剂 | 试管II中试剂 | 有机层的厚度/cm |
A | 2ml乙醇、1ml乙酸、1ml18mol/L浓硫酸 | 饱和碳酸钠溶液 | 3.0 |
B | 2ml乙醇、1ml乙酸、 | 0.1 | |
C | 2ml乙醇、1ml乙酸、3ml 2mol/L硫酸 | 0.6 | |
D | 2ml乙醇、1ml乙酸、3ml 1mol/L硫酸 | 0.3 |
a.实验D与实验C相对照可证明___________________________________________________。
b.分析实验A、C的数据,可以推测出浓硫酸的__________提高了乙酸乙酯的产率。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)________。
①单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
②单位时间里,生成1 mol乙酸乙酯,同时生成1 mol乙酸
③单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
④混合物中各物质的浓度不再变化
(7)写出G的一种同分异构体(与G同类)的结构简式:_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在2 L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡。

(1)该反应的化学方程式是____________。
(2)反应起始至t时刻,Y的平均反应速率是_______________。
(3)关于该反应的说法,正确的是______。
A.到达t时刻该反应已停止
B.加入催化剂,一定能加快反应速率
C.在t时刻正反应速率等于逆反应速率
D.增大压强,一定能加快反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)如图1所示是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是 _______(填“吸热”或“放热”)反应,断键吸收的能量为___________ (填E1或E2)
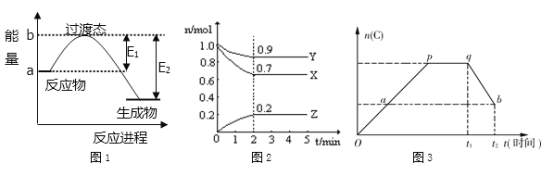
(2)某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质物质的量随时间的变化曲线如图2所示。根据图中数据,试填写下列空白:
①该反应在_____________min时达到平衡状态;
②该反应的化学方程式为:_________________________________________;
(3)一定温度下,对于反应2A(g) + B(g) ![]() 2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图3所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则:①p点时反应的v正_____v逆(填“>”、“<”或“=”);
2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图3所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则:①p点时反应的v正_____v逆(填“>”、“<”或“=”);
②a,b两点的正反应速率va________vb(填“>”、“<”或“=”)
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学反应方程式,并判断其反应类型(加成、取代、氧化)
①甲烷与氯气反应_______________________________,属于________反应
②乙烯通入溴水:_________________________________,属于________反应
③乙醇与金属钠反应:__________________________________,属于________反应
④由苯制取硝基苯:_______________________________,属于________反应;
⑤灼热的铜丝多次反复地插入乙醇中:___________________,属于_______反应;
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是_________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是________________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,Zn的密度为________________g·cm-3(列出计算式)。

查看答案和解析>>
科目: 来源: 题型:
【题目】化合物W可用作高分子膨胀剂,一种合成路线如下:

回答下列问题:
(1)A的化学名称为________。
(2)②的反应类型是__________。
(3)反应④所需试剂,条件分别为________。
(4)G的分子式为________。
(5)W中含氧官能团的名称是____________。
(6)写出与E互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积比为1∶1)______________。
(7)苯乙酸苄酯( )是花香型香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线__________(无机试剂任选)。
)是花香型香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线__________(无机试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为___________。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
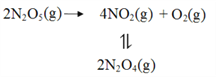
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解):
t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
p/kPa | 35.8 | 40.3 | 42.5. | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=4.4 kJ·mol1 ,2NO2(g)=N2O4(g) ΔH 2=55.3 kJ·mol1,则反应N2O5(g)=2NO2(g)+1/2O2(g)的ΔH =_______ kJ·mol1。
②研究表明,N2O5(g)分解的反应速率v=2×10-3×P(N2O5)(KPa/min)。t=62 min时,测得体系中P(O2)=2.9 kPa,则此时的P(N2O5)=________ kPa,v=_______kPa·min1。
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____63.1 kPa(填“大于”“等于”或“小于”)。
④25℃时N2O4(g)![]() 2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5![]() NO2+NO3 快速平衡
NO2+NO3 快速平衡
第二步 NO2+NO3→NO+NO2+O2 慢反应
第三步 NO+NO3→2NO2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______(填标号)。
A.v(第一步的逆反应)>v(第二步反应) B.反应的中间产物只有NO3
C.第二步中NO2与NO3的碰撞仅部分有效 D.第三步反应活化能较高
查看答案和解析>>
科目: 来源: 题型:
【题目】汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确的是( )。
A. 用盐的形式表示:BaSiO3·CuSiO3
B. 用氧化物形式表示:BaO·CuO·2SiO2
C. 易溶于强酸、强碱
D. 性质稳定,不易褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com