
科目: 来源: 题型:
【题目】将标准状况下的a L HCl(g)溶于1000g水中,得到的盐酸密度为b g·cm-3,则该盐酸的物的量浓度是( )mol·L-1
A. 1000ab/(22400+36.5a) B. ab/(22400+36.5a)
C. 1000ab/(22.4+36.5a) D. 1000ab/(22400+36.5)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应起了氮的固定作用的是( )
A. 氨经催化氧化生成NOB. NO与O2反应生成NO2
C. N2在一定条件下与Mg反应生成Mg3N2D. NH3与硝酸反应生成NH4NO3
查看答案和解析>>
科目: 来源: 题型:
【题目】将1mol N2O4气体充入容积为10L的密闭容器中,回答下列问题:

(1)100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应速率v(N2O4)为________________;反应N2O4(g)![]() 2NO2(g)的平衡常数K为___________。
2NO2(g)的平衡常数K为___________。
(2)当反应达到平衡时,对于反应N2O4(g)![]() 2NO2(g),改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是____________。
2NO2(g),改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是____________。
①气体颜色加深
②N2O4的体积分数增加
③恒温恒压充入He
④单位时间内消耗N2O4和NO2的物质的量之比等于1:2
(3)若起始时充入1molNO2气体,建立如下平衡2NO2(g)![]() N2O4(g),测得NO2的转化率为a%,在温度、体积不变时,再充入1molNO2气体,重新达到平衡时,测得NO2的转化率为b%,则a______b(填“>”、“<”或“=”);若恒温恒压时,充入1molNO2气体,反应2NO2(g)
N2O4(g),测得NO2的转化率为a%,在温度、体积不变时,再充入1molNO2气体,重新达到平衡时,测得NO2的转化率为b%,则a______b(填“>”、“<”或“=”);若恒温恒压时,充入1molNO2气体,反应2NO2(g)![]() N2O4(g)达到平衡后,再向容器内通入一定量的NO2气体,重新达到平衡时,NO2的体积分数_________(填“不变”、“增大”或“减小”)。
N2O4(g)达到平衡后,再向容器内通入一定量的NO2气体,重新达到平衡时,NO2的体积分数_________(填“不变”、“增大”或“减小”)。
(4)如下图a所示,连通的玻璃瓶中充入NO2气体,建立如下平衡2NO2(g)![]() N2O4(g),已知Fe3+对H2O2的分解具有催化作用,根据图b、c中的信息,推测A瓶中气体颜色比B瓶中的____________(填“深”或“浅”)。
N2O4(g),已知Fe3+对H2O2的分解具有催化作用,根据图b、c中的信息,推测A瓶中气体颜色比B瓶中的____________(填“深”或“浅”)。

查看答案和解析>>
科目: 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A. 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B. 当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C. 当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D. 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如下图。下列说法正确的是

A. 点①所示溶液中:c(CH3COO-)+c(OH-)=c(Na+)+c(H+)
B. 点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
C. 点③所示溶液中:NaOH与CH3COOH恰好完全中和,溶液呈中性
D. 在0.1000 mol·L-1 CH3COOH溶液中,由水电离出来的c(H+)= 10-13 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】对于MgCl2 溶液和 FeCl3溶液的有关说法,不正确的是
A. 配制FeCl3溶液时,为了防止溶液出现浑浊,可以向溶液中滴入少量盐酸
B. 为了除去MgCl2酸性溶液中的FeCl3,可在加热搅拌的条件下加入MgCO3,过滤后,再向滤液中加入适量盐酸
C. 向FeCl3溶液加FeCl3固体,水解平衡正向移动,FeCl3水解程度增大
D. 向FeCl3溶液加水,溶液颜色变浅,FeCl3水解程度增大
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒温恒容容器中发生反应2SO2(g)+O2(g)![]() 2SO3(g)△H<0,下列说法不正确的是
2SO3(g)△H<0,下列说法不正确的是
A. 容器内压强不再变化,说明反应达到平衡状态
B. 当c(SO2):c(O2)=1:2且保持不变,能表明反应达到平衡状态
C. 加入合适的催化剂可显著增大反应速率
D. 达到平衡状态时,相同时间内,每消耗2molSO3的同时生成1molO2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知t ℃时,0.01 mol/L NaOH溶液的pH=11,0.1 mol/L的HA溶液中c(H+)/c(OH-)=109
请回答下列问题:
(1)该温度下,水的离子积Kw=_____,0.1 mol/L的HA溶液中水电离出的c(OH-)=_____。
(2)在室温下,将pH之和为14的NaOH溶液和HA溶液等体积混合后,所得溶液呈_____(填“酸”“碱”或“中”)性。
(3)在室温下,蒸馏水稀释0.01 mol/L HA溶液时,下列呈减小趋势的是_____。
A.水的电离程度 B.c(HA)/c(A-)
C.溶液中c(H+)和c(OH-)的乘积 D.溶液中c(A-)·c(HA)的值
(4)室温下,取pH=2的盐酸和HA溶液各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示:
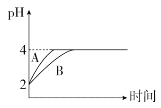
①图中表示HA溶液pH变化曲线的是____(填“A”或“B”)。
②设盐酸中加入Zn的质量为m1,HA溶液中加入Zn的质量为m2,则m1_____m2(填“>”“<”或“=”)。
(5)室温下,取0.01 mol/L的盐酸和HA溶液各100 mL,分别滴加0.01 mol/LNaOH溶液至恰好完全反应,所需NaOH溶液的体积前者____后者(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是
2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是

A. ①压强对反应的影响(p2>p1) B. ②温度对反应的影响
C. ③平衡体系增加N2对反应的影响 D. ④催化剂对反应的影响
查看答案和解析>>
科目: 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X___,沉淀A____。
(2)上述实验流程中①②③步均要进行的实验操作是___(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是______________________________。
(4)按此实验方案得到的溶液3中肯定含有______(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的___(填化学式),之后若要获得NaNO3晶体,需进行的实验操作是____(填操作名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com