
科目: 来源: 题型:
【题目】高温下,炼铁高炉中存在下列平衡:FeO(s)+CO(g)![]() Fe(s)+CO2(g)△H>0。试回答下列问题:
Fe(s)+CO2(g)△H>0。试回答下列问题:
(1)写出该反应的平衡常数表达式___________。
(2)升高温度,该反应的平衡常数K值将________(填“增大”、“减小”、“不变”),平衡体系中固体的质量将______( 填“增大”、“减小”、“不变”)。
(3)已知1100℃时该反应的平衡常数K=0.263.在该温度测得高炉中c(CO2)=0.025mol·L﹣1,c(CO)=0.1mol·L﹣1,此时该反应的化学反应速率是v(正)________ v(逆)(填“>”、“<”、“=”)。
(4)保持高炉温度为1100℃,向高炉中补充大量的空气,重新达到平衡后,该反应的平衡常数K值_____0.263(填”>”、“<”、“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺如图所示:

(1)对青蒿干燥破碎后,加入乙醚的目的是______。
(2)操作Ⅰ需要的玻璃仪器主要有烧杯、______,操作Ⅱ的名称是______。
(3)操作Ⅲ的主要过程可能是______(填字母)。
A. 加水溶解,蒸发浓缩、冷却结晶B. 加95%的乙醇,浓缩、结晶、过滤C. 加入乙醚进行萃取分液
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目: 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。

(1)下列哪个装置可防止铁棒被腐蚀________________。

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:
①A电极对应的金属是________(写元素名称),B电极的电极反应式是_________________________。
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“废气”的综合处理与应用技术是科研人员的重要研究课题,CO、SO2、NO2是重要的大气污染气体。
(1)捕集处理后的CO是制取新型能源二甲醚(CH3OCH3)的原料,已知:①CO(g)+H2O(g)![]() CO2(g)+H2(g),△H1=-41.0kJmol-1,②CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H2=-49.0kJmol-1,③CH3OCH2(g)+H2O(g)
CO2(g)+H2(g),△H1=-41.0kJmol-1,②CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H2=-49.0kJmol-1,③CH3OCH2(g)+H2O(g)![]() 2CH3OH(g)△H3=+23.5kJmol-1,则反应2CO(g)+4H2(g)
2CH3OH(g)△H3=+23.5kJmol-1,则反应2CO(g)+4H2(g)![]() CH3OCH2(g)+H2O(g)的△H=______。
CH3OCH2(g)+H2O(g)的△H=______。
(2)采用NaClO2溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性NaClO2溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表,依据表中数据,写出NaClO2溶液脱硝过程中发生的总反应的离子方程式:______。
离子 | NO3- | NO2- | Cl- |
c/(molL-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
(3)已知973K时,SO2与NO2反应生成SO3和NO,混合气体经冷凝分离出的SO3可用于制备硫酸。
①973K时测得:NO2(g)![]() NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)SO3(g)K3=20.则反应SO2(g)+NO2(g)
NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)SO3(g)K3=20.则反应SO2(g)+NO2(g)![]() O3(g)+NO(g)的K3=______。
O3(g)+NO(g)的K3=______。
②973K时,向体积为1L的恒容密闭容器中充入SO2、NO2各aml,平衡时SO2的转化率为______。
③恒压下SO2的分压p(SO2)随温度的变化如图所示。当温度升高时,SO2(g)+NO2(g)![]() SO2(g)+NO(g)的化学平衡常数______(填“增大”或”减小”),判断理由是______。
SO2(g)+NO(g)的化学平衡常数______(填“增大”或”减小”),判断理由是______。
(4)用纳米铁可去除污水中的NO3-,反应的离子方程式为4Fe+NO3-+10H+=4Fe2++NH4++3H2O;相同温度下,纳米铁粉去除不同水样中的NO3-的速率有较大差异,下表中Ⅰ和Ⅱ产生差异的原因可能是______;Ⅱ中0~20mim内用NO3-表示的平均反应速率为______molL-1min-1。
反应时间/min | 0 | 10 | 20 | 30 | 40 | |
Ⅰ | c(NO3-)/10-4molL-1 | 8 | 3.2 | 1.6 | 0.8 | 0.64 |
Ⅱ | c(NO3-)/10-4molL-1(含少量Cu2+) | 8 | 0.48 | 0.32 | 0.32 | 0.32 |
查看答案和解析>>
科目: 来源: 题型:
【题目】从某些植物树叶提取的挥发油中含有下列主要成分:

(1)B、C中互不相同官能团的名称分别为:_______、_______
(2)有关A、B、C三种物质的说法正确的是_______ (填序号)
a.均能发生加聚反应 b.只有B能与FeCl3发生显色反应
c.均不能与碳酸钠溶液反应 d.只有C能发生银镜反应
(3)A中苯环上的一卤代物的同分异构体的数目为________
(4)0.5mol B与足量的溴水充分反应,消耗_______ mol单质溴,其反应类型为:_______、______。
(5)己知: R1CH=CHR2![]() R1COOH+R2COOH.
R1COOH+R2COOH.
有机物C9H8O发生如下反应:
C9H8O ![]()
![]()
则C9H8O的结构简式为_______________。
(6)写出A与B在一定条件下相互反应,生成高分子化合物的化学方程式:__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
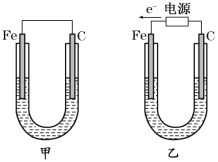
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的________棒,乙装置中的________棒。
②乙装置中阳极的电极反应式是:_______________________________。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:__________________________________。
②甲装置中碳极的电极反应式是____________________,乙装置碳极的电极反应属于________(填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因:____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E都是前20号元素中的常见元素,且核电荷数递增。A原子没有中子;B原子次外层电子数与最外层电子数之差等于电子层数;C元素是地壳中含量最高的元素;4.6gD单质与足量盐酸作用可产生2.24LH2(标准状态下);E的一价阴离子的核外电子排布与Ar的核外电子排布相同。请回答下列问题:
(1)写出A、B、D的元素符号:A____;B_____;D_____。
(2)C离子的电子式_____;E的离子结构示意图_____;
(3)实验室里检验E的单质常用的试剂是____;
(4)写出电解D、E形成化合物的水溶液的化学反应方程式_____;
(5)写出由A、B、C、D形成的化合物与由A、C、E形成的化合物发生反应的化学反应方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用铜和浓硫酸制备SO2的方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,现用3.2gCu与一定量的浓硫酸反应制SO2气体,铜完全溶解。请计算:
CuSO4+SO2↑+2H2O,现用3.2gCu与一定量的浓硫酸反应制SO2气体,铜完全溶解。请计算:
(1)求标准状况下产生SO2体积为多少______ L?
(2)若将反应后的溶液加水稀释至500mL,求反应后CuSO4溶液的浓度为多少______ mol·L-1?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com