
科目: 来源: 题型:
【题目】在25℃时,向50.00mL未知浓度的氨水中逐滴加入0.5mol·L-1的HC1溶液。滴定过程中,溶液的pOH[pOH=-lgc(OH-)]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
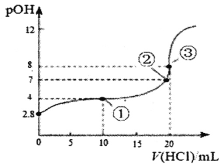
A. 图中②点所示溶液的导电能力弱于①点
B. ③点处水电离出的c(H+)=1×10-8mol·L-1
C. 图中点①所示溶液中,c(C1-)>c(NH4+)>c(OH-)>c(H+)
D. 25℃时氨水的Kb约为5×10-5.6mo1·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学课外兴趣小组为了探究影响化学反应速率的因素,做了以下实验。
(1)用三支试管各取5.0 mL、0.01 mol·L-1的酸性KMnO4溶液,再分别滴入0.1 mol·L-1 H2C2O4溶液,实验报告如下。

①实验1、3研究的是_________对反应速率的影响。
②表中V=_________mL。
(2)小组同学在进行(1)中各组实验时,均发现该反应开始时很慢,一段时间后速率会突然加快。对此该小组的同学展开讨论:
①甲同学认为KMnO4与H2C2O4的反应放热,温度升高,速率加快。
②乙同学认为随着反应的进行,因_________,故速率加快。
(3)为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:

①装置乙中仪器A的名称为_________。
②定性如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是____________________________________。
③定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】三氯化硼(BCl3),主要用作半导体硅的掺杂源或有机合成催化剂,还用于高纯硼或有机硼的制取。某兴趣小组用氯气和硼为原料,采用下列装置(部分装置可重复使用)制备BCl3。

已知:①BCl3的沸点为12.5℃,熔点为-107.3℃;遇水剧烈反应生成硼酸和盐酸;②2B+6HCl ![]() 2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
请回答下列问题:
(1)A装置可用氯酸钾固体与浓盐酸反应制氯气,反应的化学方程式为___________。
(2)装置从左到右的接口连接顺序为a→___________________→j。
(3)装里E中的试剂为___________,如果拆去E装置,可能的后果是____________。
(4)D装置中发生反应前先通入一段时间的氯气,排尽装置中的空气。若缺少此步骤,则造成的结果是_____。
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式________,硼酸也可用电渗析法制备,“四室电渗析法”工作原理如图所示:

则阳极的电极反应式__________________,分析产品室可得到H3BO3的原因________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡。请回答下列问题:
(1)常温下,物质的量浓度均为0.1mol·L-1的六种溶液
①Na2CO3、②NaCl、③NaOH、④(NH4)2SO4、⑤CH3COONa、⑥NH4NO3 , pH从大到小排列顺序为__________(填序号)。
(2)已知T℃时,Kw=1×10-12,在该温度时,将pH=9的NaOH溶液bL与pH=2的H2SO4溶液aL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3, 则a :b=__________。
(3)现有HA、HB两种酸。室温下用0.1mol· L-1NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如下图。

①由图可知;酸性HA______HB,b点对应的溶液中c(HB)_____c(B-)(填“>”“<”或“=”)。
②室温下HB的电离平衡常数Ka的数量级为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中,使2molN2和6molH2混合发生下列反应:
N2(g)+3H2(g)![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)当反应达到平衡时, N2和H2的转化率比是 。
(2)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时减小一倍,平衡将向 移动(填“向左”、“向右”或“不”)。
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将向___________移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将___________移动(填“向 左”、“向右”或“不”)。达到新平衡后,容器内温度 (填“大于”、“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯六水氯化锶晶体(SrCl2·6H2O)可作有机合成的催化剂。用碳酸锶矿石(含少量BaCO3、FeO、SiO2等杂质)制备高纯六水氯化锶晶体的过程如图所示。
已知:

I.25℃,Ksp[Fe(OH)3]=1.0×10-38 ,Ksp[Fe(OH)2]=1.0×10-16
Ⅱ.SrCl2·6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
请回答:
(1)步骤①中将矿石制成浆液能加快反应速率的原因是_____________________________。
(2)在“浆液”中加入工业盐酸,测得锶的浸出率与温度、时间的关系如图所示:

据此合适的工业生产条件为_________________________。
(3)步骤②“溶液”中加入30%的H2O2,其作用是_____________________________(用离子方程式表示)。
(4)步骤③所得滤渣的主要成分除Fe(OH)3外,还有_______________________(填化学式);25℃,为使Fe3+沉淀完全需调节溶液pH值最小为_____________(当离子浓度减小至1.0×10-5mol·L-1时,可认为沉淀完全)。
(5)关于上述流程中各步骤的说法,正确的是___________(填标号)。
A.步骤④用60℃的热水浴加热蒸发至有晶膜出现
B.步骤④冷却结晶过程中应通入HC1气体
C.步骤⑤干燥SrCl2·6H2O晶体可以采用减压干燥
(6)为测定所得SrCl2·6H2O(Mr=267)晶体样品的纯度,设计了如下方案:称取1.10g样品溶解于适量水中,向其中加入含AgNO31.70g的AgNO3溶液(溶液中除Cl-外,不含其它与Ag+反应生成沉淀的离子),C1-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.100 mol·L-1的NH4SCN标准溶液滴定剩余的AgNO3溶液,使剩余的Ag+以AgSCN白色沉淀的形式析出,当___________时达到滴定终点,用去NH4SCN溶液20.00 mL,则原SrCl2·6H2O晶体的纯度为________________%(计算结果保留1位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应A(g)![]() B(g)
B(g)
(1)该反应的速率方程可表示为V正=K正CA,V逆=K逆CB,K正和K逆在一定温度时为常数,分别称作正,逆反应速率常数。已知T1温度下,K正=0.004s-1 ,K逆=0.002s-1,该温度下反应的平衡常数值K=______。该反应的活化能Ea(正)大于Ea(逆),则![]() ____0(填“>”“<”或“=”)。
____0(填“>”“<”或“=”)。
(2)对于该反应A(g)![]() B(g),在313 K和353 K时A的转化率随时间变化的结果如图所示。
B(g),在313 K和353 K时A的转化率随时间变化的结果如图所示。

①在313 K时反应的平衡转化率α=_______%。平衡常数K313 K___K353 K(填“>”“<”或“=”),理由是________________________________。
②在353 K下:要提高A的转化率,可采取的措施是___________;要缩短反应达到平衡的时间,可采取的措施有____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1×10-12,如图是向10mL AgNO3溶液中逐渐加入0.1mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象。根据图象所得下列结论不正确的是[提示:Ksp(AgCl)>Ksp(AgI)]

A. 原AgNO3溶液的物质的量浓度为1mol·L-1
B. 图中x点满足c(Ag+)·c(Cl-)= Ks p( AgCl)
C. 相同实验条件下,把0.1mol·L-1的NaCl换成0.1mol·L-1NaI则图象在终点x的纵坐标小于6
D. 相同实验条件下,若改为0.2mol·L-1 NaCl溶液时,x点的横坐标小于100
查看答案和解析>>
科目: 来源: 题型:
【题目】向绝热恒容密闭容器中通入一定量的SO2和NO2,一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是

A. Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 B. 反应在c点达到平衡状态
C. 反应物的总能量低于生成物的总能量 D. 反应物浓度:a点小于b
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,可逆反应![]() 达到平衡,若:
达到平衡,若:
(1)A、B、C都是气体,减小压强,平衡向正反应方向移动,则![]() ____(填“>”“<”或“=”)p。
____(填“>”“<”或“=”)p。
(2)A、C是气体,而且![]() ,增大压强可使平衡发生移动,则平衡移动的方向是__________。
,增大压强可使平衡发生移动,则平衡移动的方向是__________。
(3)加热后,可使C的质量增加,则正反应是__________(填“放热”或“吸热”)反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com