
科目: 来源: 题型:
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO![]() 2CO2+N2。假设常温下在恒容的密闭容器中发生上述反应,试解答下列问题:
2CO2+N2。假设常温下在恒容的密闭容器中发生上述反应,试解答下列问题:
(1)上述条件下该反应能够自发进行,则反应的ΔH_____0(填写“>”、“<”、“=”)。
(2)能判断该反应达到化学平衡状态的依据是____________。
A.混合气体的压强保持不变
B.N2的浓度不再改变
C.消耗CO的物质的量与生成CO2的物质的量之比为1∶1
D.NO、CO、CO2、N2的物质的量之比为2∶2∶2∶1
(3)既要加快反应速率又要提高NO转化率,下列措施可行的是____________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)为了测定在某种催化剂作用下的反应速率,某科学家在某温度下用气体传感器测得不同时间的NO和CO浓度如表(均不考虑温度变化对催化剂催化效率的影响):
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) ( molL-1) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO) ( molL-1) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | X | 2.70×10-3 |
从表中数据分析可知:
①X=____________mol·L-1;
②前2s内的平均反应速率v(N2)=________________________mol·L-1·s-1;
③该温度下反应的平衡常数K=________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:N2(g)+3H2(g) ![]() 2 NH3(g) ΔH=-92.4 kJ·mol-1。一定条件下,现有容积相同且恒容的密闭容器甲与乙:① 向甲中通入1 mol N2和3 mol H2,达到平衡时放出热量Q1 kJ;② 向乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2 kJ。则下列关系式正确的是
2 NH3(g) ΔH=-92.4 kJ·mol-1。一定条件下,现有容积相同且恒容的密闭容器甲与乙:① 向甲中通入1 mol N2和3 mol H2,达到平衡时放出热量Q1 kJ;② 向乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2 kJ。则下列关系式正确的是
A. Q1=2Q2=92.4B. 92.4=Q1<2Q2
C. 92.4>Ql>2Q2D. Q1=2Q2<92.4
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,已知0-t1时,原电池的负极是Al片,反应过程中有红棕色气体产生。下列说法不正确的是

A. 0-t1时,正极的电极反应式为:2H++ NO3- - e-=NO2+ H2O
B. 0-t1时,溶液中的H+ 向Cu电极移动
C. t1时,负极的电极反应式为:Cu–2e-= Cu2+
D. t1时,原电池中电子流动方向发生改变是因为Al在浓硝酸中钝化,氧化膜阻碍了Al的进一步反应
查看答案和解析>>
科目: 来源: 题型:
【题目】看下列仪器装置图,回答下列问题:
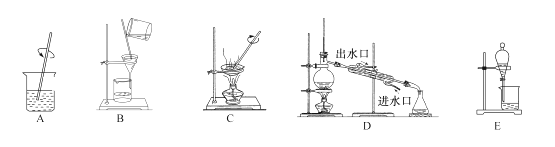
(1)粗盐的提纯需要上面的哪些装置?___________(填字母符号)
(2)分离以下混合物应该选择使用什么装置?(填字母符号)
①酒精和水:___________,
②食盐和水:___________,
③二氧化锰和KCl:___________,
④花生油和水:___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成。其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子。下列说法错误的是( )
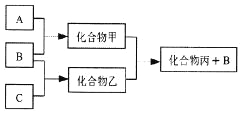
A. Z元素位于第二周期第VIA族
B. 可用排水法收集化合物乙
C. 元素X、Y、Z的原子半径大小关系为X<Z<Y
D. 化合物甲溶于化合物丙中,存在的微粒有5种
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,向Al2O3和过量C粉的混合物中通入氯气,可制得易水解的AlCl3,实验装置如图所示。下列说法不正确的是
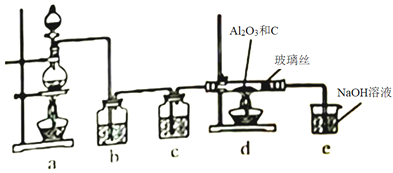
A. c中盛装的是浓硫酸
B. 实验时应先点燃d处酒精灯,再点燃a处酒精灯
C. 此反应中的尾气,除氯气外都可直接排放到大气中
D. 该装置不完善,其中应改进的一项是在d、e之间添加一个干燥装置
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应不属于氧化还原反应的是( )
A.3 NO2 + H2O = 2 HNO3 + NOB.FeCl3+3NaOH=3NaCl+Fe(OH)3↓
C.2KMnO4![]() K2MnO4 + MnO2 + O2↑D.Cl2 + 2NaOH ═NaClO + NaCl + H2O
K2MnO4 + MnO2 + O2↑D.Cl2 + 2NaOH ═NaClO + NaCl + H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列有关实验叙述正确的是________(填序号)。
a.试管、烧杯均可用于给液体、固体加热
b.使食盐水中NaCl结晶析出时,常用到的仪器有坩埚、酒精灯、玻璃棒、泥三角
c.用分液漏斗分离水和乙酸混合液
d.分液时,下层液体先从分液漏斗下口放出,换一个接收容器,再将上层液体从分液漏斗下口放出
e.用托盘天平称取25.20g氯化钠
f.取用金属钠时,没用完的钠要放回原瓶
(2)实验室用密度为1.25g/mL,质量分数为36.5%的浓盐酸配制240mL 0.1mol/L的盐酸,应量取浓盐酸体积__mL。使用的仪器除玻璃棒、烧杯、量筒外,还需要_____、____。
(3)在容量瓶使用方法中,下列操作不正确的是(填序号)___。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.配置溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2㎝处,再改用胶头滴管加蒸馏水到刻度线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2㎝处,再改用胶头滴管加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
F.定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25 ℃时三种金属硫化物的溶度积常数分别是:Ksp(FeS)=6.3×10-18 mol2·L-2、Ksp(CuS)=1.3×10-36 mol2·L-2、Ksp(MnS)=2.5×10-13mol2·L-2,下列说法中正确的是
A. 25 ℃时,FeS的溶解度大于MnS的溶解度
B. 25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol·L-1
C. 除去某溶液中的Cu2+,可以选用FeS或MnS作沉淀剂
D. 因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生
查看答案和解析>>
科目: 来源: 题型:
【题目】液流电池是一种新型可充电的高性能蓄电池,其工作原理如下图。两边电解液存储罐盛放的电解液分别是含有V3+、V2+的混合液和VO2+、VO2+酸性混合液,且两极电解液分开,各自循环。下列说法不正确的是( )

A.充电时阴极的电极反应是V3++e-=V2+
B.放电时,VO2+作氧化剂,在正极被还原,V2+做还原剂,在负极被氧化
C.若离子交换膜为质子交换膜,充电时当有1mol e-发生转移时,左槽电解液的H+的物质的量增加了1mol
D.若离子交换膜为阴离子交换膜,放电时阴离子由左罐移向右罐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com