
科目: 来源: 题型:
【题目】反应A(g)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
A. v(A)=0.15mol/(Lmin)
B. v(B)=0.04mol/(Ls)
C. v(C)=0.03mol/(Ls)
D. v(D)=0.4mol/(Lmin)
查看答案和解析>>
科目: 来源: 题型:
【题目】在10L密闭容器中,1molA和3molB在一定条件下反应:A(g)+xB(g)![]() 2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
A.平衡时,物质的量比A:B:C=2:11:4
B.x值等于4
C.A的转化率20%
D.B的平均反应速率为0.04mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。回答下列问题:
I.采样
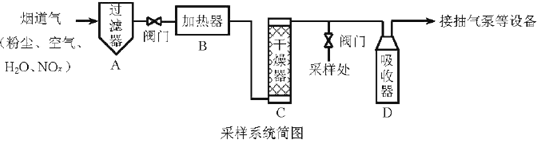
采样步骤:
①检验系统气密性;②加热器将烟道气加热至140。C;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
II. NOx含量的测定
将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3-,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。
(1)NO被H2O2氧化为NO3-的离子方程式是___________。
(2)滴定操作使用的玻璃仪器主要有___________。
(3)滴定过程中发生下列反应:
3Fe2+ +NO3-+4H+ = NO↑+3Fe3+ +2H2O
Cr2O72-+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为_________mg·m-3。
(4)判断下列情况对NOx含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)若缺少采样步骤③,会使测试结果___________。若FeSO4标准溶液部分变质,会使测定结果___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用密度为1.18g/ml,质量分数为36.5%浓盐酸配制250ml0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250ml0.1mol/L的盐酸溶液.应量取盐酸体积_________ml,应选用容量瓶的规格__________________ml。
(2)配制时,其正确的操作顺序是________。
A.用30ml水洗涤烧杯 2﹣3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30ml),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250ml的容量瓶中
D.将容量瓶盖紧、振荡、摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1﹣2cm处
a.BCAFED b.BCFED c.BCAED
(3)操作B中,使用量筒量取液体时视线俯视会造成配制液体浓度__________(偏高、偏低或无影响)。操作E中加水超过刻度线该如何处理?____________
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)?
a.没有进行A操作____________;
b.加蒸馏水时不慎超过了刻度___________;
c.定容时俯视_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义。
请回答下列问题:
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观。

①图中所示所属的分类方法为___________。
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是___________________。
A.具有还原性 B.属于氧化物 C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在________________。
药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
药品 | 乙醇、乙酸 | 活性炭、红磷 | 锌粒、铜片 | 氯化钠、氯化钾 |
A.甲柜 B.乙柜 C.丙柜 D. 丁柜
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、碳酸钠)”能发生反应。将一定量的稀硫酸逐滴滴入到氢氧化钠和碳酸钠的混合溶液中,边滴加边搅拌,直至有少量气泡产生,此过程中共发生的离子反应有_______个。
(2)含铁元素的物质有很多,在生产、生活中应用广泛。取少量某油漆的原料Fe2O3(红棕色粉末),加人适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式为_______________________________,另在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入2 mL上述棕黄色溶液,继续加热至液体呈_______色,停止加热,证明所得分散系类型的实验方法的名称是_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用6 g CaCO3与100 mL稀盐酸反应制取少量的CO2,反应过程中生成的CO2的体积(已折算为标准状况)随反应时间变化的情况如右图所示。下列说法正确的是

A. OE段表示的平均反应速率最快,可能的原因是该反应是放热反应
B. EF段用HC1浓度的减小表示的该反应的平均反应速率为0.2 mol/(L·min)
C. 在F点收集到的CO2的体积最大
D. 在G点以后收集的CO2的量不再增多,原因是稀盐酸已反应完全
查看答案和解析>>
科目: 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)![]() 2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
A.生成B的速率与C分解的速率相等
B.A、B、C的浓度相等
C.单位时间生成nmolA,同时生成2nmolC
D.A、B、C的分子数之比为1:3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
![]()
下列说法中不正确的是( )
A. 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B. 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C. B和Cl2的反应是氧化还原反应
D. 当X是强酸时,C在常温下是气态单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com