
【题目】在10L密闭容器中,1molA和3molB在一定条件下反应:A(g)+xB(g)![]() 2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
A.平衡时,物质的量比A:B:C=2:11:4
B.x值等于4
C.A的转化率20%
D.B的平均反应速率为0.04mol·L-1·min-1
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
【题目】物质G是制备抗癌药物吉非替尼过程中重要的中间体,某研究小组按照下列线路合成中间体G。

已知: 、
、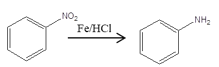 、
、 (同时还有H2O或卤化氢生成)
(同时还有H2O或卤化氢生成)
请回答:
(1)下列说法正确的是_______。
A.化合物A能够使酸性高锰酸钾溶液褪色
B.化合物A中含有4种不同的官能团
C.化合物C具有碱性
D.化合物G的分子式为C15H20N3O3
(2)上述路线中合成A的反应类型为______,化合物E的结构简式为______。
(3)写出C到D的化学反应方程式________。
(4)请设计以乙烯为原料转变为物质C的合成线路(用流程图表示,无机试剂任选)___。
(5)写出化合物B(C8H7NO2)可能的同分异构体_______。须同时满足:①能发生银镜反应;②1H—NMR谱显示分子中含有苯环,且分子中有4种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 100g46%甲酸(HCOOH)水溶液所含的氧原子数为5NA
B. 标准状况下,18g冰水中共价键的数目为NA
C. 56g铁与71gCl2充分反应,转移电子数目为3NA
D. 7.8gNa2O2与足量的水(H218O)反应生成的氧气所含的中子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO)制备草酸镍晶体(NiC2O4·2H2O)的流程如下:
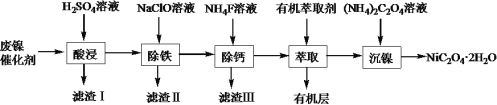
(1)NiC2O4·2H2O中C的化合价是______。既能加快“酸浸”反应速率又能提高“酸浸”原料利用率的操作措施为_____________。
(2)“滤渣Ⅰ”的主要成分是_____________。若控制温度为80℃、pH=2时,“除铁”产生的“滤渣Ⅱ”的主要成分为黄钠铁矾(Na2Fe6(SO4)4(OH)12),写出生成黄钠铁矾沉淀的离子方程式:__________________。
(3)已知“滤渣Ⅲ”的主要成分为CaF2,则“萃取”操作中加入有机萃取剂的作用是__________。
(4)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是_________。
(5)高能锂离子电池的总反应为2Li + FeS = Fe + Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
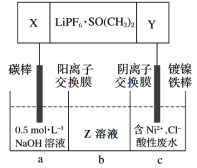
①电极X的反应材料是_________(填化学式);中间隔室b可以得到的主要物质Z是_________(填化学式)。
②电解总反应的离子方程式为_________。已知F=96500C/mol,若电池工作t min,维持电流强度为I A,理论回收Ni_________g(写出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用图示装置进行实验,反应进行足够长时间后装置II中实验现象正确的是
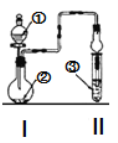
① | ② | ③ | II中实验现象 | |
A | 浓盐酸 | 大理石 | 氯化钡溶液 | 产生大量白色沉淀 |
B | 浓氨水 | 碱石灰 | 硫酸亚铁溶液 | 产生大量白色沉淀 |
C | 冰醋酸 | 乙醇和浓硫酸 | 饱和碳酸钠溶液 | 溶液分层,上层为油状液体 |
D | 浓盐酸 | KMnO4 | 氢硫酸 | 产生淡黄色沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可用已知浓度的标准I2溶液进行滴定(弱酸性性环境)。该反应的化学方程式为:C6H8O6+I2 = C6H6O6+2HI具体测定步骤及测得数据如下:取10 mL 6 mol·L-1CH3COOH溶液,加入100 mL蒸馏水,将溶液加热煮沸后冷却。精确称取0.2000 g样品,溶解于上述冷却的溶液中,加入1mL指示剂,立即用浓度为0.0500 mol·L-1的标准I2溶液进行滴定到终点,消耗21.00 mL I2溶液。
(1)实验中的指示剂是____________确定达到滴定终点的现象是_____________。
(2)盛装标准I2溶液的是_________(酸式或碱式)滴定管,若滴定结束时俯视滴定管读数(其它操作正确)则滴定结果_______(偏高、偏低或无影响)。
(3)加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用,其目的是_____________。
(4)计算样品中维生素C的质量分数____________(要求列式,且式中各物理量带单位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为___未成对电子数为___个。
(2)丙酮(![]() )分子中碳原子轨道的杂化类型是___,丙酮分子中含有σ键的数目为____个。
)分子中碳原子轨道的杂化类型是___,丙酮分子中含有σ键的数目为____个。
(3)C、H、O三种元素的电负性由小到大的顺序为___。
(4)乙醇的沸点高于丙酮,这是因为___。
(5)利用价层电子对互斥理论判断PCl3的立体构型是___。
(6)某FexNy的晶胞如图-1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图-2 所示,其中更活泼的Cu替代型产物的化学式为___。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com