
科目: 来源: 题型:
【题目】实验室用图所示装置电解氯化铜溶液,实验中观察到碳(I)电极质量增加,碳(II)电极有气体放出。下列说法正确的是
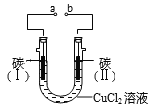
A. a为电源负极
B. 电极Ⅱ上发生还原反应
C. 电子流向:a→Ⅰ→Ⅱ→b
D. 该装置将电能转化为化学能
查看答案和解析>>
科目: 来源: 题型:
【题目】如图电化学原理可用于治理水中硝酸盐的污染,下列说法不正确的是
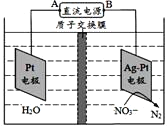
A. A为电源正极
B. 在Pt电极上发生氧化反应
C. 阴极电极反应式为2NO3-+6H2O+10e-=N2+12OH
D. 质子从Pt电极移向Ag-Pt电极
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,恒容密闭容器中发生某可逆反应,A、B、C三种气体的物质的量浓度随时间的变化如图所示。请回答下列问题:
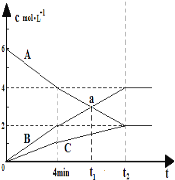
(1)此反应的化学方程式为___。
(2)反应从开始至4min末,用A表示的平均反应速率为____。
(3)t2的值___8(填“大于”、“等于”或“小于”),其原因是___。
(4)某同学经分析得出如下结论,其中正确的是___(填选项序号)。
①该反应在t1时刻达到了反应限度
②保持条件不变,延续足够长的时间,容器中将可能不存在A物质
③该反应达到了反应限度后物质B的质量将保持不变
④改变反应条件将可能改变反应的限度
查看答案和解析>>
科目: 来源: 题型:
【题目】半导体有单质、二元化合物、三元化合物等之分,其中三元半导体CuAlO2(或Cu2Al2O4)的制取,常采用CuO与Al2O3或Al(OH)3共热的方法。试分析并回答:
(l)试完成如下化学方程式:
_______CuO+_______ Al2O3![]() _______Cu2Al2O4+_______ ↑
_______Cu2Al2O4+_______ ↑
(2)上述反应能发生的理由主要是_____________。
(3)Al(OH)3有碱式和酸式两种电离方式,若25℃时,其酸式电离为Al(OH)3![]() AlO2-+H++H2O K=2.0×10-13,则入Al(OH)3+OH-
AlO2-+H++H2O K=2.0×10-13,则入Al(OH)3+OH-![]() AlO2-+2H2O的平衡常数K’=_______(列式并计算)。该反应的△H_______(填“<”“>”或“=”)0。
AlO2-+2H2O的平衡常数K’=_______(列式并计算)。该反应的△H_______(填“<”“>”或“=”)0。
(4)经实验测定,“AlO2-” 的形式应该是[Al(OH)4]-,则AlCl3溶液与Na[Al(OH)4]溶液作用的离子方程式是_________________。
(5)用石墨电极电解Na[Al(OH)4] 溶液是制取高品质用Al(OH)3的方法之一。该电解反应的离子方程式是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某白色粉状固体X,它是碘的一种较稳定氧化物,M=334 g·mol-1;有关化学性质与转化如下:
①X在343K时,与CO作用生成B和CO2;
②X在573K时,分解生成A和B;
③X与水作用生成D;
④D+HCl→B+Z+H2O;
⑤Z与氯仿在一定条件下生成灭火剂Y等。
又知A、B、Z是常见单质。试分析并回答:
(1)组成B的元素处于第_____________族。
(2)写出②的化学方程式:_______________。
(3)写出Y的分子式:_________
(4)B与KI作用生成的阴离子的符号是_________
(5)写出④的离子方程式:____________。
(6)根据较为完全的反应①,再利用某一经典反应原理(方法),在工业上可以测定废气中CO的含量。试简述其测定方法:________。
(7)Z与氯仿反应的方程式一般为Z+氯仿→Y+氢化物,但也有另一种可能,其化学方程式是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物M为烃的含氧衍生物,为研究M的组成与结构,依次进行了如下实验:
实验步骤 | 解释或实验结论 |
1、升温使M汽化,测其密度是相同条件下NO的3倍。 | 由此可知M的摩尔质量为 _________ |
2、称取9.0 g M在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g | 由此可知M的分子式为 ________ |
3、通过M的红外光谱图发现该分子中含有C—C、C—H、C—O、O—H、C=O,且该物质可与碳酸钠溶液反应放出气体,1mol该物质与足量金属钠反应可得1mol氢气。 | (1)M中可与碳酸钠溶液反应放出气体的官能团的名称为:_________ |
4、M的核磁共振氢谱如图:
| (2)M中含有_______种氢原子 |
5、综上所述,可知 M的结构简式为_________。 | |
6、N的分子式为C8H8O3,为芳香族化合物,与M具有相同数目和种类的官能团,则满足条件的N的同分异构体共有____种,其中苯环上有两个取代基,遇FeCl3溶液显紫色的N的结构简式为______(写出一种即可)。 | |
查看答案和解析>>
科目: 来源: 题型:
【题目】在某温度时,密闭容器中进行反应:X(g)+4Y(g)![]() 2Z(g)+3R(g),其中X、Y、Z、R的起始浓度依次为0.1、0.4、0.2、0.3(单位均为mol·L-1,下同),则达平衡时,各物质的浓度不可能的是
2Z(g)+3R(g),其中X、Y、Z、R的起始浓度依次为0.1、0.4、0.2、0.3(单位均为mol·L-1,下同),则达平衡时,各物质的浓度不可能的是
A.c(X)=0.15B.c(Z)=0.3C.c(Y)=0.9D.c(R)=0.6
查看答案和解析>>
科目: 来源: 题型:
【题目】如图曲线a和b是可溶性一元强碱与盐酸互滴的滴定曲线,下列说法正确的是
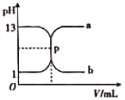
A.可溶性一元强碱、盐酸的物质的量浓度均为1mol·L-1
B.p点为滴定终点(两者恰好完全反应),溶液呈中性
C.酚酞不能用作该滴定的指示剂
D.曲线b是可溶性一元强碱滴定盐酸的滴定曲线
查看答案和解析>>
科目: 来源: 题型:
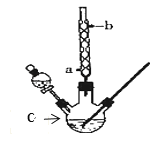
【题目】某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去)。已知下列数据:
乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 | |
熔点/℃ | ﹣117.3 | 16.6 | ﹣83.6 | |
沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
请回答下列问题:
(1)仪器C的名称为______,球形冷凝管的作用是_____。
(2)向C中加入反应物,待充分反应后,将C中的混合物倒入装有饱和碳酸钠溶液的烧杯中充分振荡洗涤。饱和碳酸钠溶液作用是(填字母):_____
A.中和乙酸并溶解乙醇
B.碳酸钠溶液呈碱性,有利于乙酸乙酯的水解
C.加速乙酸乙酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(3)经多次振荡洗涤、静置分液后,为了进一步提纯乙酸乙酯,可采用蒸馏的方法,蒸馏时控制温度在__左右,温度计的水银球应位于____。
(4)若实验所用乙酸质量为2.4g,乙醇质量为2.1g,得到纯净的产品质量为2.64g,则乙酸乙酯的产率是______。
(5)乙酸乙酯与氢氧化钠溶液发生反应的化学方程式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,将一元酸 HA 的溶液和 KOH 溶液等体积混合(忽略体积变化),实验数据如下表:

下列判断不正确的是( )
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=KW/1×10-9mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol/L
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com