
科目: 来源: 题型:
【题目】Ni2O3主要用作陶瓷、搪瓷和玻璃的着色剂,也可用于镍粉的制造。以镍粉废料为原料制备Ni2O3的工艺如下:
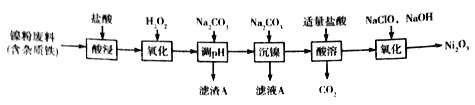
回答下列问题:
(1)Ni2O3中Ni的化合价为_________。
(2)提高“酸浸”、“酸溶”速率时,温度不宜过高,其原因是__________。
(3)加入H2O2“氧化”的离子方程式为_____________;滤渣A的主要成分是________(填化学式)。
(4)工艺中分步加入Na2CO3的作用是________;为提高原料的利用率,应控制加入NaClO与NaOH的物质的量之比为_________。
(5)工业上,用镍为阳极,电解0.1mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率(电流效率是指电解时,在电极上实际沉积的物质的量与理论析出量之比)及镍的成粉率的影响如图所示:
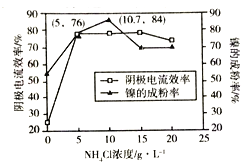
①为获得高纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为______mol/L.
②当NH4Cl溶液的浓度大于15g/L时,阴极有气体生成,导致阴极电流效率降低,请结合平衡移动原理解释其原因:_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关金属的工业制法中,正确的是
A. 以海水为原料制得精盐,再电解精盐的水溶液制取钠
B. 用海水、石灰乳等为原料,经一系列过程制得氧化镁,用H2还原氧化镁制得镁
C. 以铁矿石、焦炭、空气、石灰石等为原料,通过反应产生的CO在高温下还原铁矿石制得铁
D. 从铝土矿中获得氧化铝再制得氯化铝固体,电解熔融的氯化铝得到铝
查看答案和解析>>
科目: 来源: 题型:
【题目】下列变化符合图示的是
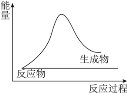
①冰雪融化②KMnO4分解制O2③铝与氧化铁的反应④钠与水反应⑤二氧化碳与灼热的木炭反应⑥碘的升华⑦Ba(OH)2·8H2O和NH4Cl的反应
A.②⑥⑦B.③④C.①②⑤⑥⑦D.②⑤⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
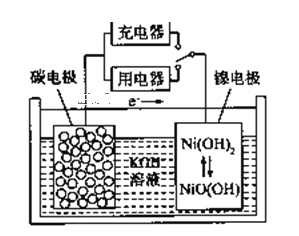
A. 充电时,阴极的电极反应为:Ni(OH)2+OH-+e-=NiO(OH)+H2O
B. 放电时,负极的电极反应为:H2-2e-+2OH-=2H2O
C. 放电时,OH-移向镍电极
D. 充电时,将电池的碳电极与外电源的正极相连
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化)。下列各组物质中,不能满足此转化关系的是( )
物质 选项 | X | Y | Z |
A | Al | Al2O3 | NaAlO2 |
B | Fe | FeCl3 | FeCl2 |
C | C | CO | CO2 |
D | Cl2 | HCl | NaCl |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式正确的是( )
A. 甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 已知在120℃、101 kPa下,1 gH2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+![]() O2(g)===H2O(g) ΔH=-242 kJ·mol-1
O2(g)===H2O(g) ΔH=-242 kJ·mol-1
D. 25℃、101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)===K2SO4(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示是元素周期表的部分轮廓图,根据元素①~⑩在周期表中的位置按题目要求回答:
① | |||||||||||||||||
② | ③ | ④ | |||||||||||||||
⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||||
⑨ | |||||||||||||||||
⑩ |
(1)写出由元素①③④按原子个数比4:2:3组成的物质的化学式_______,其含有的化学键类型有________。
(2)元素⑤~⑧形成的简单离子中,离子半径由大到小的顺序为____________(用离子符号表示)。
(3)元素③⑦⑨的简单气态氢化物沸点由高到低的顺序排列是______(用化学式表示)。
(4)写出元素⑩的原子结构示意图______。
(5)元素②和④组成的一种化合物是引起温室效应的主要气体,其电子式为_________,将少量该化合物通入由元素④⑤⑥组成的一种盐溶液中,写出相应的化学方程式_____。
(6)元素⑧的一种氧化物通入氯化钡溶液无沉淀,通入硝酸钡溶液却会产生白色沉淀,写出少量该氧化物通入硝酸钡溶液的离子方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物的种类繁多,包含烃和烃的衍生物,官能团决定有机物的化学性质,请按要求回答下列问题。
I.已知乙二醇( ![]() )、丙三醇(
)、丙三醇(![]() )都与乙醇含有相同的官能团,都属于醇类物质,与乙醇具有相似的化学性质。
)都与乙醇含有相同的官能团,都属于醇类物质,与乙醇具有相似的化学性质。
请按要求完成下列问题:
(1)写出醇类物质都含有的官能团的电子式_______________。
(2)乙醇、乙二醇( ![]() )、丙三醇(
)、丙三醇(![]() )别与足量金属钠作用,产生等量的氢气。则这三种醇的物质的量之比为______。
)别与足量金属钠作用,产生等量的氢气。则这三种醇的物质的量之比为______。
(3)写出乙醇的催化氧化的化学方程式__________,反应类型:________ ;
(4)丙三醇(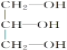 )与足量乙酸发生酯化反应的化学方程式(反应条件与乙醇酯化反应相同)_____。
)与足量乙酸发生酯化反应的化学方程式(反应条件与乙醇酯化反应相同)_____。
II.以下是用苯作原料制备一系列化合物的转化关系图,已知:R-NO2![]() R-NH2(其中-R代表烃基)
R-NH2(其中-R代表烃基)
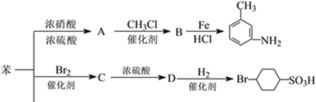
(5)写出A→B的化学反应方程式______,反应类型:_________。
(6)C中含有的官能团的名称为________;D的结构简式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10﹣2,K2=5.4×10﹣5。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。回答下列问题:
(1)草酸中含有的官能团名称是______。
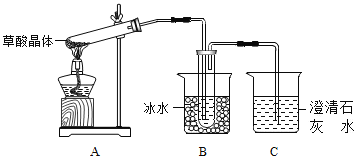
(2)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是______,由此可知草酸晶体分解的产物中有_____。装置B的主要作用是_______。
(3)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和如图所示的部分装置(可以重复选用)进行实验。

①乙组同学的实验装置中,依次连接的合理顺序为A、B、_____。装置H反应管中盛有的物质是_____(填化学式)。
②能证明草酸晶体分解产物中有CO的现象是____________;
(4)设计实验:①证明草酸的酸性比碳酸的强(简述操作步骤和现象,下同)______;
②用简单的方法鉴别草酸和甲酸______。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组模拟上述过程,所设计的装置如图所示:
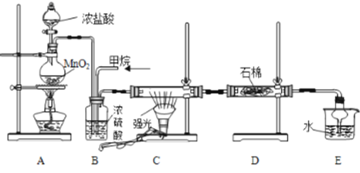
(1)A中制取Cl2时若将MnO2换成另一种固体即可不用加热并能快速制取氯气,写出该快速制氯气过程的离子方程式为______。
(2)B装置有三种功能:①控制气流速度;②___________;③___________。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是___________。
(4)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是___________。
(5)该装置还存在的明显缺陷是____________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com