
科目: 来源: 题型:
【题目】对乙酰氨基酚,俗称扑热息痛(Paracetamol),具有很强的解热镇痛作用,工业上通过下列方法合成(图中B1和B2、C1和C2分别互为同分异构体,无机产物略去):
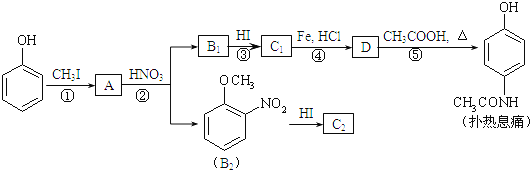
已知:R-NO2![]() R-NH2 请按要求填空:
R-NH2 请按要求填空:
(1)写出A分子中官能团名称:_________;C1的结构简式为:___________________。
(2)写出由D生成扑热息痛的化学方程式:________________________________。
(3)④的反应类型:_____________。
(4)工业上设计反应①、②、③,而不是只通过反应②得到C1、C2,其目的是:_______________________。
(5)扑热息痛有很多同分异构体,符合下列要求的同分异构体有5种:(1)是对位二取代苯;(II)苯环上两个取代基一个含氮不含碳、另一个含碳不含氮;(III)两个氧原子与同一原子相连。其中2种的结构简式是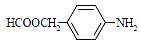 和
和![]() ,写出另3种同分异构体的结构简式____________、____________、____________。
,写出另3种同分异构体的结构简式____________、____________、____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位,请据图回答下列问题:
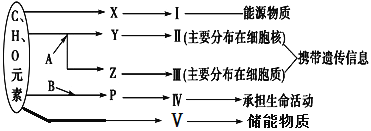
(1)图中A代表的元素是(用元素符号填写)_______________。图中X是_______________,Ⅰ在小麦种子中主要是指_______________。
(2)Ⅴ在动物、植物细胞均含有,是生物体内理想的储能物质,则Ⅴ是_______________。
(3)物质P是_______________,其结构通式为______________________________;若Ⅳ分子由n个P分子(平均相对分子质量为m)组成的2条链组成,则该Ⅳ分子的相对分子质量大约为______________。从理论上分析,该Ⅳ物质至少有_____个氨基和_____个羧基。
(4)生物体中的Ⅱ、Ⅲ的基本组成单位是__________各单位间是通过______________键连接起来的,可以通过___________________________对细胞进行染色,染色后Ⅱ呈现出_______色,Ⅲ呈现出_______色。
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.已知:Na2SO3(aq)+S(s)![]() Na2S2O3(aq),实验可知该反应较慢。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
Na2S2O3(aq),实验可知该反应较慢。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
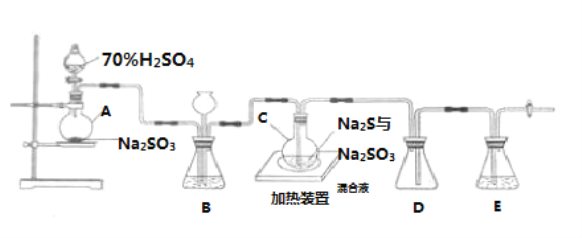
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若_______,则整个装置气密性良好。装置D的作用是______________________________________ 。
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___________。
a.蒸馏水 b .饱和Na2SO3溶液
c.饱和NaHSO3溶液 d . 饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是____________。烧瓶C中反应达到终点的现象是____________________。待C中反应完成后应立即关闭分液漏斗的旋塞,原因是_______________________。
(3)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O35H2O,其中可能含有Na2SO3、Na2SO4等杂质,利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:_______________________________________________。供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
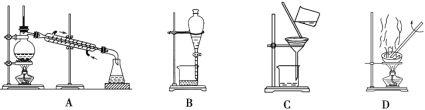
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl等杂质,选择装置________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________(填“上”或“下”)口进水。装置B在操作时为使液体顺利滴下,除打开下端活塞外,还应进行的具体操作是________________________________。
(4)为了除去KCl中的Ca2+、Mg2+、![]() 及泥沙,得到纯净的KCl,可将混合物溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序进行提纯,正确的步骤及顺序是___________。
及泥沙,得到纯净的KCl,可将混合物溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序进行提纯,正确的步骤及顺序是___________。
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液 ⑥加过量KOH溶液 ⑦加过量K2CO3溶液
A.②⑤④①③ B.⑥⑤⑦①③ C.④①②⑤③ D.④②⑤①③
查看答案和解析>>
科目: 来源: 题型:
【题目】对一种未知有机物的结构测定,往往需要多种复杂方法相结合,一般来说,主要包括以下几个方面:①相对分子质量;②元素组成(种类和比例);③该有机物的各种性质的研究;④结构的确定。
(1)相对分子质量的确定一般有质谱法,蒸气密度法等。蒸气密度法是指一定条件下将有机物气化,测定该条件下的密度,利用气态方程式计算相对分子质量。蒸气密度法的要求是该有机物在______。如果沸点过高,可以采用________方法。质谱法是在一定条件下让有机物失去电子变成阳离子,测其相对分子质量。该过程中,复杂的有机物分子往往变成小的片断,如C4H10断裂成CH3CH2CH2+、CH3CH2+、CH3+、CH3CH2CH2CH2+等,其式量最大的就是其相对分子质量。该法测定某有机物A质谱中显示相对分子质量最大是72。
(2)组成元素的测定往往采用元素分析仪,以前也常用燃烧法。称取3.6 gA,跟足量氧气充分燃烧后通过浓硫酸,浓硫酸增重5.4 g,剩余气体通过碱石灰,碱石灰增重11 g,则该有机物的分子式为________。
(3)核磁共振谱常用氢谱和碳谱,它主要测定分子中具有不同特点的C或H的种类与比例。如对于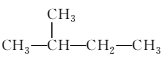 ,经测定,C谱有四个峰,其数值高低比例为2∶1∶1∶1;H谱有四个峰,其数值高低比例为1∶2∶3∶6。有机物A碳谱有两个峰,峰高比为4∶1。氢谱有一个峰。试写出有机物A的结构简式________。
,经测定,C谱有四个峰,其数值高低比例为2∶1∶1∶1;H谱有四个峰,其数值高低比例为1∶2∶3∶6。有机物A碳谱有两个峰,峰高比为4∶1。氢谱有一个峰。试写出有机物A的结构简式________。
查看答案和解析>>
科目: 来源: 题型:
【题目】德国化学家凯库勒认为,苯分子的结构中碳碳间以单、双键交替排列结合成环状。为了验证凯库勒的观点,某同学设计了以下实验方案:

①按如图所示的装置连接好仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量FeBr3,塞上橡皮塞,打开止水夹K1、K2、K3;
④待烧瓶a中收集满气体后,将导管b的下端插入烧杯D里的水中,挤压预先盛有水的胶头滴管,观察实验现象。
(1)A中所发生反应的反应类型为________,能证明凯库勒观点错误的实验现象是________________________________________________________________。
(2)装置B的作用是___________________________________。
(3)装置A中发生反应的化学方程式:________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾天气频繁出现,严重影响人们的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
浓度mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断试样的pH=________________。
(2)为减少SO2的排放,常将煤转化为清洁气体燃料:
已知:H2(g)+ ![]() O2(g) =H2O(g) △H= -241.8kJ·mol-1
O2(g) =H2O(g) △H= -241.8kJ·mol-1
C(s)+ ![]() O2(g) =CO(g) △H = -110.5kJ·mol-1
O2(g) =CO(g) △H = -110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:_________________________________________________。
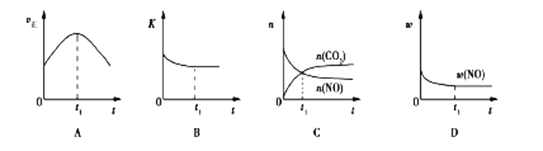
(3)汽车尾气净化的主要原理:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g); △H<0,若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填序号)。(如图中v正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
2CO2(g)+N2(g); △H<0,若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填序号)。(如图中v正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
(4)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”之一。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质)。一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
物质 温度/℃ | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式______________________;
②计算上述反应T1℃时的平衡常数K1=______________________;若T1<T2,则该反应的△H _____0(填“>”、“<”或“=”)。
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为________;
查看答案和解析>>
科目: 来源: 题型:
【题目】通常将一定量的有机物充分燃烧转化为简单的无机物,然后根据产物的质量确定有机物的组成。如图所示是用燃烧法确定有机物分子式的常用装置。
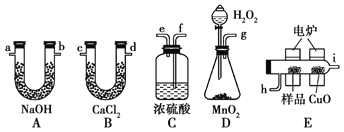
请回答下列问题:
(1)使产生的O2按从左到右的方向流动,则所选装置中各导管的正确连接顺序是________(填字母)。
(2)装置C中浓硫酸的作用是_____________________________________。
(3)燃烧管中CuO的作用是________________________________。
(4)若准确称取0.69 g样品(只含C、H、O三种元素中的两种或三种),充分燃烧后,A管质量增加1.32 g,B管质量增加0.81 g,则该有机物的实验式为________。
(5)要确定该有机物的分子式,还要知道该有机物的____,经测定其蒸气密度为 2.054 g/L(已换算为标准状况),则其分子式为______。
(6)该物质的核磁共振氢谱如图所示,则其结构简式为____。

查看答案和解析>>
科目: 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线。
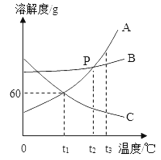
(1)P点表示的含义是__。
(2)t1℃时,将35gA物质加入到50g水中,形成___(填“饱和”或“不饱和”)溶液。
(3)B中混有少量的A,提纯B的方法是__。
(4)将等质量的A、B、C三种固体物质分别配成t3℃时的饱和溶液,所得溶液的质量最多的是___。
(5)将t1℃时A、B、C三种物质的饱和溶液升温到t3℃时,所得溶液的溶质质量分数由大到小的关系是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】NiOOH难溶于水,常作电池的正极材料。利用某含镍废料(主要成分为NiO,另含有SiO2、Fe2O3、CuO三种杂质)制备NiOOH的工业流程如图。
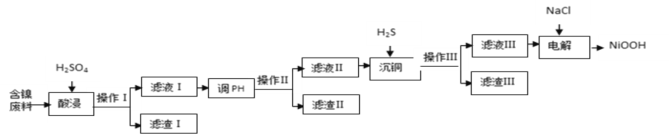
已知:
Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | |
开始沉淀的pH | 1.5 | 4.4 | 6.7 |
沉淀完全的pH | 3.7 | 6.9 | 9.2 |
(1)提高酸浸速度的方法为_______________________、_____________________(任写2条)
(2)滤渣Ⅰ的成分为__________;若滤渣Ⅱ为Fe(OH)3,则“调pH”的范围为_____________.
(3)沉铜时发生反应的离子方程式为______________________________________________。
(4)电解过程是控制在碱性条件下阳极产生ClO-,并用ClO-将Ni2+氧化的过程。请写出氧化过程中发生反应的离子方程式____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com