
科目: 来源: 题型:
【题目】下列说法正确的是
A. 测定盐酸和NaOH溶液反应的中和热时,每次实验均应测量三个温度,即盐酸的起始温度、NaOH溶液的起始温度和反应后的终止温度
B. HCl和NaOH反应的中和热ΔH=57.3 kJ·mol1,则稀H2SO4和稀Ca(OH)2溶液反应的中和热 ΔH=2×57.3 kJ·mol1
C. 燃烧热是指在101 kPa时可燃物完全燃烧时所放出的热量
D. S(s)+ ![]() O2(g)
O2(g)![]() SO3(g) ΔH=315 kJ·mol1(燃烧热)
SO3(g) ΔH=315 kJ·mol1(燃烧热)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下在一个2 L的恒容密闭容器中发生反应4A(s)+3B(g)![]() 2C(g)+D(g),经2 min达平衡状态,此时B反应消耗了0.9 mol,下列说法正确的是
2C(g)+D(g),经2 min达平衡状态,此时B反应消耗了0.9 mol,下列说法正确的是
A. 平衡时,v(A)∶v(B)∶v(C)∶v(D) =4∶3∶2∶1
B. 混合气的平均相对分子质量可作为平衡标志
C. 充入惰性气体使压强增大可加快反应速率
D. C的平均反应速率为0.5 mol/(L·min)
查看答案和解析>>
科目: 来源: 题型:
【题目】X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。回答下列问题:
(1)元素X在元素周期表中位于___区,单质X的晶体类型为_____,其中X原子的配位数为_____。
(2)Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是__________。
(3)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为____________。
(4)X与Y形成的一种化合物的立方晶胞如图所示。
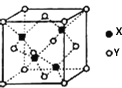
该化合物的化学式为_______,已知此晶体的密度为ρg·cm–3,阿伏伽德罗常数为NA,则此晶胞中X与Y的最近距离是______cm。(写出计算式,不要求计算结果。)
查看答案和解析>>
科目: 来源: 题型:
【题目】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在___对自旋相反的电子,基态氮原子的价层电子排布图为____。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为__其中氧原子的杂化方式为_______。
(3)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:
已知:相关物质的溶解度(20℃)AgCl:1.5×10-4g Ag2SO4:0.796 g
(1)甲同学的实验如下:
序号 | 操作 | 现象 |
实验Ⅰ | 将2 mL 1 mol/L AgNO3溶液加入到1 mL 1 mol/L FeSO4溶液中 | 产生白色沉淀,随后有黑色固体产生 |
取上层清液,滴加KSCN 溶液 | 溶液变红 |
注:经检验黑色固体为Ag
① 白色沉淀的化学式是_____________。
② 甲同学得出Ag+氧化了Fe2+的依据是_______________。
(2)乙同学为探究Ag+和Fe2+反应的程度,进行实验Ⅱ。
a.按右图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
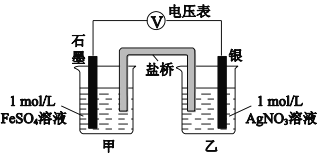
b.随后向甲烧杯中逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
① a中甲烧杯里的电极反应式是___________。
② b中电压表指针逆向偏移后,银为_________极(填“正”或“负”)。
③ 由实验得出Ag+和Fe2+反应的离子方程式是___________。
(3)为进一步验证乙同学的结论,丙同学又进行了如下实验:
序号 | 操作 | 现象 |
实验Ⅲ | 将2 mL 2 mol/L Fe(NO3)3溶液加入有银镜的试管中 | 银镜消失 |
实验Ⅳ | 将2 mL1 mol/L Fe2(SO4)3溶液加入有银镜的试管中 | 银镜减少,未消失 |
实验Ⅴ | 将2 mL 2 mol/L FeCl3溶液加入有银镜的试管中 | 银镜消失 |
① 实验Ⅲ___________(填“能”或“不能”)证明Fe3+氧化了Ag,理由是_____________。
② 用化学反应原理解释实验Ⅳ与Ⅴ的现象有所不同的原因:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关有机物结构的叙述不正确的是( )
A.一氟一氯甲烷只有一种结构,可以证明甲烷是正四面体结构
B.构成乙烯分子的所有原子都在同一平面内,其分子中只含有极性键
C.邻二甲苯没有同分异构体表明苯的凯库勒结构式不准确
D.![]() 和CH3一CH=CH2互为同分异构体
和CH3一CH=CH2互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒。某兴趣小组进行下面实验探究,查阅资料知道:① HNO2为弱酸,② 2NO + Na2O2 = 2NaNO2,③ 2NO2 + Na2O2 = 2NaNO3 ④ 酸性KMnO4溶液可将NO和NO2-均氧化为NO3-,MnO4-还原成Mn2+。NaNO2的制备方法可有如下2种方法(夹持装置和加热装置已略,气密性已检验):
制备装置1:
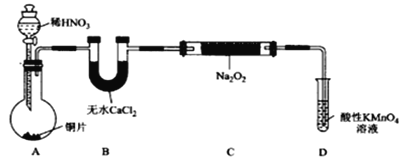
制备装置2:
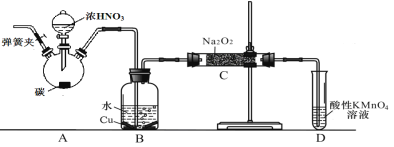
(1)在制备装置1中:
①如果没有B装置,C中发生的副反应有_________;
②甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质;于是在A装置与B装置间增加了_____装置,改进后提高了NaNO2的纯度;
③ D装置发生反应的离子方程式为______。
(2)在制备装置2中:
① B装置的作用是_______________________;
②写出装置A烧瓶中发生反应的化学方程式并用单线桥标出电子的转移___________;
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用硫碘开路循环联产氢气和硫酸的工艺流程如图所示:
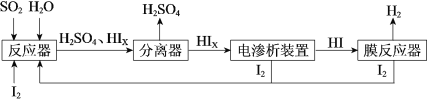
请回答下列问题:
(1)在反应器中发生反应的化学方程式是_______。
(2)在膜反应器中发生反应:2HI(g)H2(g)+I2(g) H>0。若在一定条件密闭容器中加入1 mol HI(g),n(H2)随时间(t)的变化关系如图所示:
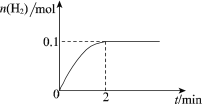
①该温度下,反应平衡常数K=_______,若升高温度,K值将_______(填“增大”、“减小”或“不变”)。
②用化学平衡原理解释使用膜反应器及时分离出H2的目的是______。
(3)电渗析装置如图所示:
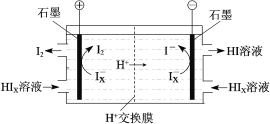
①结合电极反应式解释阴极区HIx转化为HI的原理是___。
②该装置中发生的总反应的化学方程式是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】PHB树脂可用于制作外科手术缝合线,有机物K是一种抗惊厥药物,它们的合成路线如图:
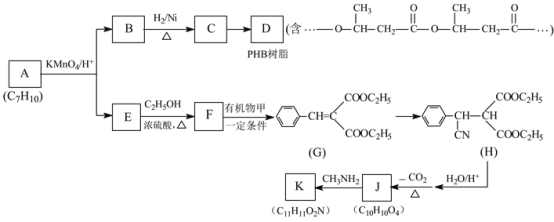
已知:
①RCN![]() RCOOH
RCOOH
②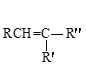
![]() RCOOH+
RCOOH+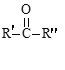
③RCHO+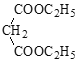
![]()
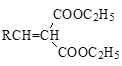 + H2O
+ H2O
R、R′、R″代表烃基
(1)有机物甲的结构简式为____________。
(2)写出一定条件下C→D的化学方程式:____________。
(3)写出E→F的化学方程式:__________________。
(4)A的结构简式为______________。
(5)已知1 mol J最多与2 mol NaHCO3反应;K分子结构中含有一个五元环与一个六元环。写出一定条件下J→K的化学方程式:____________。
(6)S是A的一种同分异构体,分子中没有环状结构,S的核磁共振氢谱有三个峰,峰面积之比为6:3:1,则S的结构简式为___________(写出一种即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化铁黄(化学式为FeOOH)是一种黄色颜料,工业上用废铁为主要原料生产氧化铁黄的一种工艺流程如下:
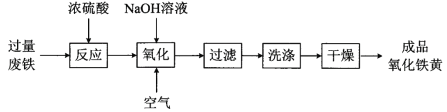
(1)氧化铁黄中铁元素的化合价为_____,废铁在反应前常用热的纯碱溶液清洗表面油污,其原理是______ (写离子方程式)。
(2)氧化过程生成氧化铁黄的化学方程式是_____________。
(3)上述流程中,检验“洗涤”是否完全的方法是________。
(4)氧化时应控制pH的合理范围是3.5-4.0,pH过小导致氧化铁黄产率较低的可能原因是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com