
科目: 来源: 题型:
【题目】写出下列转化的化学方程式,注明反应类型。
(1)甲苯→TNT ___________________
(2)乙烯→聚乙烯__________________
(3)1,3—丁二烯与氯气1,4—加成__________________
(4)溴乙烷和氢氧化钠的乙醇溶液共热___________________
(5)乙醇在铜催化下和氧气反应__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求回答下列问题:
①干冰与CO2; ②白磷与红磷; ③![]() Cl与
Cl与![]() Cl;
Cl;
④液氯与氯水; ⑤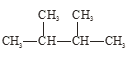 与
与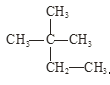 。
。
在上述各组物质中:
(1)互为同位素的是_____________;
(2)互为同素异形体的是__________,
(3)互为同分异构体的是_________;
(4)属于同种物质的是_________。(填序号)
查看答案和解析>>
科目: 来源: 题型:
【题目】碳的单质及其化合物是常见的物质。完成下列填空:
已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为:C(石墨)+O2(g)→CO2(g)+393.51kJ;C(金刚石)+O2(g)→CO2(g)+395.41kJ
(1)等质量时石墨的能量比金刚石的___(选填“高”或“低”),由石墨制备金刚石是___反应(选填“吸热”或“放热”)。
由焦炭与石英在高温的氮气流中反应,可制得一种新型陶瓷材料——氮化硅(Si3N4):C+SiO2+N2→Si3N4+CO(未配平)
(2)配平后的化学方程式各物质的化学计量数依次是___。若已知CO生成速率为v(CO)=12mol/(L·min),则N2消耗速率为v(N2)=___mol/(L·min)。
一定温度下10L密闭容器中发生某可逆反应,其平衡常数表达式为:K=![]() 。
。
(3)该反应的化学方程式为___。
(4)能判断该反应一定达到平衡状态的是___。
a.v正(H2O)=v逆(CO)
b.容器中气体的相对分子质量不随时间改变
c.消耗nmolH2同时消耗nmolCO
d.容器中物质的总物质的量不随时间改变
(5)已知常温下0.1mol/L碳酸氢钠溶液的pH=8.4,该溶液中的c(H2CO3)___c(CO32-)(选填“>”、“=”或“<”);该溶液电中性的表达式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇分子中不同的化学键如图,关于乙醇在各种反应中断裂键的说法不正确的是( )
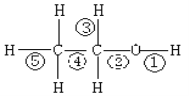
A. 乙醇和钠反应,键①断裂
B. 在铜催化下和O2反应,键①③断裂
C. 1700C乙醇制乙烯时,键②⑤断裂
D. 1400C乙醇制乙醚的反应,键①⑤断裂
查看答案和解析>>
科目: 来源: 题型:
【题目】黑火药是我国古代四大发明之一,它的爆炸反应为:2KNO3+3C+S![]() K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑
完成下列填空:
(1)上述反应中的还原剂为___,还原产物有___,当有1molKNO3参加反应时,转移电子的数目为___。
(2)KNO3晶体类型是___,其晶体中存在的化学键有___。
(3)硫原子的核外电子排布式为___,原子核外有___种不同能量的电子。将SO2和Cl2分别通入品红溶液中,产生的现象是___;若将SO2和Cl2等体积混合后再缓缓通入品红溶液,发现品红溶液___,其原因是___。
(4)S、C和N三种元素的原子半径从小到大的顺序是___;K2S溶液中除OH-外其它各离子物质的量浓度的大小顺序为___。
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有___。
a.同温同浓度溶液pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
d.分解温度:CH4>H2S
查看答案和解析>>
科目: 来源: 题型:
【题目】绿色化学又称环境友好化学,它的主要特点之一是提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”。下列反应符合绿色化学这一特点的是( )
A.工业冶炼Fe2O3 + 3CO![]() 2Fe + 3CO2
2Fe + 3CO2
B.实验室制取二氧化碳CaCO3+2HCl=CaCl2+H2O+CO2↑
C.用生石灰制熟石灰CaO+H2O=Ca(OH)2
D.实验室制取氢气Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E、F六种物质,它们的相互转化关系如下图(反应条件略,有些反应的产物和反应的条件没有全部标出)。已知A、B、E是单质,其中A着火只能用干燥的沙土灭火,B在常温下为气体,C俗名称为烧碱,D为无色无味液体。

(1)写出A、B、F的化学式 A______ B ______ F ______。
(2)写出A和D反应生成B和C的化学方程式_____________。若生成3mol的B,则转移的电子数目为_______________ 。
(3)写出E与C、D反应生成的B和F离子方程式____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用电石制取乙炔的装置如下图所示,请填空:

(1)写出仪器的名称:①是________________,②是________________;
(2)制取乙炔的化学方程式是________________;
(3)仪器①中加入的是________________,其目的是________________;
(4)将乙炔通入KMnO4酸性溶液中观察到的现象是________________,乙炔发生了___________反应(填“加成”或“取代”或“氧化”,下同);
(5)为了安全,点燃乙炔前应________________,乙炔燃烧时的实验现象是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列曲线中,纵坐标表示生成氢氧化铝的量,横坐标表示加入试剂的体积。从下边图中选出选项:
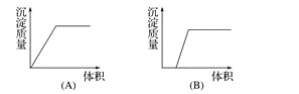
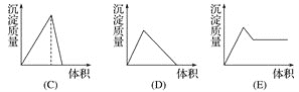
(1)向盐酸酸化的氯化铝溶液中逐滴滴入氨水至过量__________。
(2)向氢氧化钠与偏铝酸钠混合液中通入二氧化碳过量__________。
(3)向氨水中逐滴滴入氯化铝溶液至过量__________。
(4)向氯化铝溶液中滴加氢氧化钠至过量__________。
(5)向偏铝酸钠溶液滴加盐酸至过量______________。
(6)向氯化镁和氯化铝混合液中加氢氧化钠至过量____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com