
科目: 来源: 题型:
【题目】研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式:_____________。
(2)在海洋循环中,通过如图所示的途径固碳。
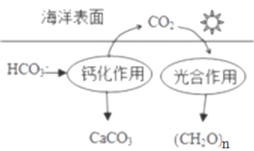
①写出钙化作用的离子方程式:_____________。
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程式如下,将其补充完整:_____________+_____________=(CH2O)x+x18O2+xH2O,_____________
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2,用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如图所示),将虚线框中的装置补充完整并标出所用试剂。_____________

②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xmol/LHCl溶液滴定,消耗ymLHCl溶液,海水中溶解无机碳的浓度=_____________mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】在某温度下,可逆反应mA(g) + nB(g) ![]() pC(g) + qD(g)的平衡常数为K,下列说法正确的是( )
pC(g) + qD(g)的平衡常数为K,下列说法正确的是( )
A. K值越小,达到平衡时,反应物的转化率越大
B. K值越大,达到平衡时,生成物的含量越大
C. 反应物的转化率越大,达到平衡时,K值越大
D. 温度越高,达到平衡时,K值越大
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要0.1 mol·L1NaOH溶液500 mL。
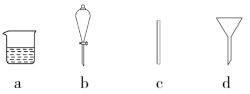
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,还需要的玻璃仪器是________。
(2)根据计算用托盘天平称取的NaOH固体质量为__________g。
(3)关于容量瓶的四种叙述:
①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是______(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)容量瓶上需标有以下五项中的_________________(填序号)。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(5)配制时,其正确的操作顺序是_________(用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(6)下列配制的溶液浓度偏低的是____________(填序号)。
A.称量NaOH时,砝码错放在左盘
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
E.配制前,容量瓶中有少量蒸馏水
查看答案和解析>>
科目: 来源: 题型:
【题目】现有一瓶气体为NH3,气体的物质的量为0.2mol。
①气体的质量为______,气体中含氢原子的物质的量为____ mol。
②气体中所含分子数为_____。
③气体在标准状况下的体积为______。
④将气体甲完全溶解于水中形成500mL溶液,所得溶液溶质的物质的量浓度为______ molL-1。
⑤将④中所得溶液取出100mL,加水稀释至1000ml,所得溶液溶质的物质的量浓度为 ______ molL-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】t ℃时,某平衡体系中含有X、Y、Z、W四种物质,此温度下发生反应的平衡常数表达式为K=![]() 。有关该平衡体系的说法正确的是
。有关该平衡体系的说法正确的是
A. 当混合气体的平均相对分子质量保持不变时,反应达平衡
B. 增大压强,各物质的浓度不变
C. 升高温度,平衡常数K增大
D. 增加X的量,平衡既可能正向移动,也可能逆向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】在CH3COONa溶液里,加入下列物质使水解平衡向左移动,并且pH变大的是 ( )
A. 加入适量纯CH3COOH
B. 加入少量NaCl固体
C. 加入少量NaOH固体
D. 加水稀释
查看答案和解析>>
科目: 来源: 题型:
【题目】有七种元素,其中A、X、Y、D、E为短周期主族元素,Z、G为第四周期元素,它们的原子序数依次增大。请回答问题。
A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
X | 元素原子的核外 |
Y | 原子的第一至第四电离能分别是: |
D | 原子核外所有 |
E | 元素的主族序数与周期数的差为4 |
Z | 是前四周期中电负性最小的元素 |
G | 在周期表的第七列 |
(1)已知![]() 为离子化合物,写出其电子式_______________。
为离子化合物,写出其电子式_______________。
(2)X基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈_____形;![]() 的空间构型为__________。
的空间构型为__________。
(3)某同学根据上述信息,推断Y基态原子的核外电子排布为:
![]()
该同学所画的电子排布图违背了________________________。
(4)G位于元素周期表的_________区,原子结构示意图为____________________。
(5)![]() 中心原子的杂化方式为_________,其空间构型为____________________。
中心原子的杂化方式为_________,其空间构型为____________________。
(6)Z元素的基态原子价电子排布式为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有四种短周期元素A、B、C、D,已知:①C、D在同一周期,A、B在同一主族;②它们可以组成化合物A2C、B2C2、DC2、D2A4等;③B的阳离子与C的阴离子的核外电子排布相同;④B2C2同A2C或DC2反应都生成气体C2,B与A2C反应生成气体A2,A2与气体C2按体积比2∶1混合后点燃能发生爆炸,其产物是一种常温下常见的无色无味的液体。请回答:
(1)写出元素符号:A________、D________。
(2)在A2C、B2C2、DC2和D2A4中,含有离子键和非极性共价键的化合物的电子式是________,按原子轨道重叠方式,其非极性键的类型是________;化合物分子中的键角是180°的是________(填结构式)。
(3)D2A4是_______分子(填极性或非极性),1个该分子中含有________个σ键、________个π键。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)中国古代四大发明之一——黑火药,它的爆炸反应为2KNO3+3C+S![]() A+N2↑+3CO2↑。
A+N2↑+3CO2↑。
①除S外,上列元素的电负性从大到小依次为____。
②在生成物中,含极性共价键的分子的中心原子轨道杂化类型为____。
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为____。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为____,Q2+的未成对电子数是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com