
科目: 来源: 题型:
【题目】2019年6月5日美国商务部表示,美方将采取“空前行动”,确保对科技业和军方极其关键的战略性矿物及稀土供应无虞。我国稀土出口量世界第一。以氟碳铈矿(主要含CeFCO3,少量其他稀土盐LnFCO3、非稀土元素Fe、Al、Mg和SiO2等)为原料制备CeO2的一种工艺流程如图所示:

(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是_________________________________。“氧化焙烧”时,CeFCO3和其他稀土盐LnFCO3分别转化为CeO2和Ln2O3,请写出生成的CeO2化学方程式为:________________________。
(2)“氯化”过程的目的是将CeO2和Ln2O3分别转化为可溶性的CeCl3和LnCl3,除去Fe2O3、Al2O3、MgO、SiO2等杂质。若溶液中c(Ce3+)=0.01mol/L,为确保不析出Ce(OH)3沉淀,则溶液的pH________(填pH的范围)。(已知Ksp[Ce(OH)3=1.0×10-20])
(3)CeO2和Ln2O3混合物中加入稀盐酸,Ln2O3溶解生成LnOCl的化学方程式为:___________________________________________________。
(4)化工生产条件的选择:
①“氯化”条件的选择
将氧化焙烧后氟碳铈矿和氯化铵按1:3、1:4、1:5、1:6、1:7质量比混合,在325℃下真空焙烧60min。稀土矿氧化物转化成稀土氯化物的氯化率如图所示:

氧化焙烧后氟碳铈矿和氯化铵的最佳质量比为________。
②“氧化”条件的选择
氧化过程中,反应温度、反应时间对混合稀土氯化物氧化率的关系如图所示:

最佳温度和时间是_________,原因是_________________________________________。
(5)取上述流程中得到的CeO2产品0.4500g,加硫酸溶解后,用0.1000molL-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其它杂质均不反应),消耗25.00mL标准溶液.该产品中CeO2的质量分数为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】原子核外p能级、d能级等原子轨道上电子排布为“全空”“半满”“全满”的时候一般更加稳定,称为洪特规则的特例。下列事实不能作为这个规则的证据的是( )
A.硼元素的第一电离能小于铍元素的第一电离能
B.磷元素的第一电离能大于硫元素的第一电离能
C.基态铜原子的核外电子排布式为![]() 而不是
而不是![]()
D.某种激发态碳原子的核外电子排布式为![]() 而不是
而不是![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】为了除去KCl固体中少量的MgCl2、MgSO4,可选用Ba(OH)2、盐酸和K2CO3三种试剂,按如下步骤操作:

(1)图中三种试剂分别为:A___________、B___________、C____________.
(2)①加入过量A的目的是___________________________;
②加入过量B的目的是_____________________________;
③加热煮沸的目的是_______________________________;
④操作Ⅰ和操作Ⅱ的名称分别是_______、_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】用常见烃A与某些烃的含氧衍生物可以制备PI(聚2-甲基-1,3-丁二烯)和PVB塑料。流程如图:
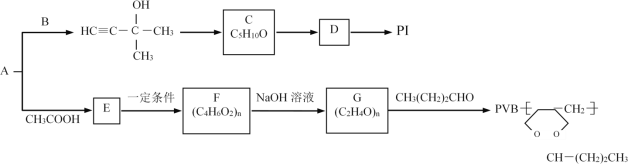
完成下列填空:
(1)A的名称是___,B的结构简式为___,C→D的反应条件是___,D→PI的反应类型是___。
(2)E中所含官能团的名称是___,写出符合下列条件的E的所有同分异构体的结构简式:___。
a.能发生银镜反应和水解反应
b.能与氢气发生加成反应
c.分子结构中含有一个甲基
(3)写出F→G的化学反应方程式:___。
(4)试用电石和乙醛等原料(无机试剂任选)制取1,3-丁二烯(合成正丁橡胶的原料),写出合成路线___。
(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目: 来源: 题型:
【题目】碳、氮元素及其化合物与人类的生产生活密切相关,试回答下列有关问题:
(1)NH3极易溶于水,其水溶液俗称氨水。用水稀释0.1molL-1的氨水,溶液中随着水量的增加而减小的是___________(填序号)。
A.![]() B.
B.![]() C.c(H+)c(OH-) D.
C.c(H+)c(OH-) D.![]()
(2)NO2可用氨水吸收生成NH4NO3。25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是______________(用离子方程式表示)。向该溶液中滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将________(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为________mol/L-1。(NH3·H2O的电离平衡常数为Kb=2×10-5)
(3)以甲烷为燃料的新型电池的成本大大低于以氢气为燃料的传统燃料电池,下图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图。

①B电极的反应式为_______________________。
②若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol·L-1的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗甲烷的体积为_________(标准状况)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有A、B、C三种气体,A是密度最小的气体,B在通常情况下呈黄绿色,纯净的A可以在B中安静地燃烧生成C。把气体B通入到适量石灰乳中可以得到白色浑浊物D。请据此回答下列问题:
(1)写出下列各反应的化学方程式
①纯净的A在B中安静地燃烧生成C_______________
②将气体B通入到水中:__________。
③将气体B通入到NaOH溶液中:_______________________
④将气体B通入到适量石灰乳中:_______________________
(2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是________(用字母表示)。
(3)将白色浑浊物D溶于水得到澄清溶液,分别取适量该澄清液两份。
①向第一份中滴加碳酸钠溶液观察到出现沉淀,发生反应的化学方程式为______________、________。
②向第二份溶液中滴加硝酸酸化的硝酸银溶液,会观察到____________(填现象)。
③白色浑浊物D因具有漂白性又称为______________,该物质在空气中容易变质的原因为_______________(用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】活性炭可处理大气污染物NO。T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
活性炭/mol | NO/mol | A/mol | B/mol | |
起始状态 | 2.030 | 0.100 | 0 | 0 |
2 min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)2 min内,用NO表示该反应的平均速率v(NO)=______mol·L-1·min-1。
(2)该反应的化学方程式是______;T℃时,它的平衡常数K=9/16,则2 min时反应______(填“是”或“不是”)平衡状态;已知升高温度时,K增大,则该反应为______(填“吸热”或“放热”)反应。
(3)为了提高反应速率和NO的转化率,可采取的措施是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】有如图所示各步变化,A为金属,B为淡黄色固体,且每一物质均含有A元素。

(1)试推断以下物质:
B.____________,C.____________,D.____________,E.____________(填化学式)。
(2)写出B→C的化学方程式:____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国十分重视保护空气不被污染,奔向蓝天白云,空气清新的目标正在路上。硫、氮、碳的大多数氧化物都是空气污染物。完成下列填空:
I.(1)碳原子的最外层电子排布式为___。氮原子核外能量最高的那些电子之间相互比较,它们不相同的运动状态为___。硫元素的非金属性比碳元素强,能证明该结论的是(选填编号)___。
A.它们的气态氢化物的稳定性
B.它们在元素周期表中的位置
C.它们相互之间形成的化合物中元素的化合价
D.它们的最高价氧化物对应水化物的酸性强弱
Ⅱ.已知NO2(g)+SO2(g)![]() NO(g)+SO3(g),在一定容积的密闭容器中进行该反应。
NO(g)+SO3(g),在一定容积的密闭容器中进行该反应。
(2)在一定条件下,容器中压强不发生变化时,___(填“能”或“不能”)说明该反应已经达到化学平衡状态,理由是:___。
在一定温度下,若从反应体系中分离出SO3,则在平衡移动过程中(选填编号)___。
A.K值减小 B.逆反应速率先减小后增大
C.K值增大 D.正反应速率减小先慢后快
Ⅲ.化学家研究利用催化技术进行如下反应:2NO2+4CO![]() N2+4CO2+Q(Q>0)
N2+4CO2+Q(Q>0)
(3)写出该反应体系中属于非极性分子且共用电子对数较少的物质的电子式___。按该反应正向进行讨论,反应中氧化性:___>___。
若该反应中气体的总浓度在2min内减少了0.2mol/L,则用NO2来表示反应在此2min内的平均速率为___。
(4)已知压强P2>P1,试在图上作出该反应在P2条件下的变化曲线___。

该反应对净化空气很有作用。请说出该反应必须要选择一个适宜的温度进行的原因是:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】将质量相等的铁片和铜片用导线相连浸入500 mL硫酸铜溶液中构成如图1的装置:
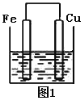
(以下均假设反应过程中溶液体积不变)。
(1)铁片上的电极反应式为______________,
(2)铜片周围溶液会出现___________的现象。
(3)若2 min后测得铁片和铜片之间的质量差为1.2 g,计算:导线中流过的电子的物质的量为__________mol;
(4)金属的电化学腐蚀的本质是形成了原电池。如下图所示,烧杯中都盛有稀硫酸。
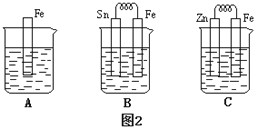
①图2 B中的Sn为________极,Sn极附近溶液的pH(填“增大”“减小”或“不变”)____。
②图2 C中被腐蚀的金属是___________。比较A、B、C中纯铁被腐蚀的速率由快到慢的顺序是______。
(5)人们应用原电池原理制作了多种电池,以满足不同的需要。燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
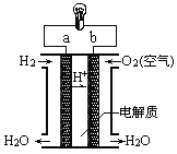
①氢氧燃料电池的正极电极反应是:___________________。电池工作一段时间后硫酸溶液的浓度_____________(填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com