
【题目】现有A、B、C三种气体,A是密度最小的气体,B在通常情况下呈黄绿色,纯净的A可以在B中安静地燃烧生成C。把气体B通入到适量石灰乳中可以得到白色浑浊物D。请据此回答下列问题:
(1)写出下列各反应的化学方程式
①纯净的A在B中安静地燃烧生成C_______________
②将气体B通入到水中:__________。
③将气体B通入到NaOH溶液中:_______________________
④将气体B通入到适量石灰乳中:_______________________
(2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是________(用字母表示)。
(3)将白色浑浊物D溶于水得到澄清溶液,分别取适量该澄清液两份。
①向第一份中滴加碳酸钠溶液观察到出现沉淀,发生反应的化学方程式为______________、________。
②向第二份溶液中滴加硝酸酸化的硝酸银溶液,会观察到____________(填现象)。
③白色浑浊物D因具有漂白性又称为______________,该物质在空气中容易变质的原因为_______________(用化学方程式表示)。
【答案】H2+Cl2![]() 2HCl Cl2+H2OHCl+HClO Cl2+2NaOH=NaCl+NaClO+H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O BC CaCl2+Na2CO3=CaCO3↓+2NaCl Ca(ClO)2+Na2CO3=CaCO3↓+2NaClO 生成白色沉淀 漂白粉 Ca(ClO)2+H2O+CO2=2HClO+CaCO3、2HClO
2HCl Cl2+H2OHCl+HClO Cl2+2NaOH=NaCl+NaClO+H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O BC CaCl2+Na2CO3=CaCO3↓+2NaCl Ca(ClO)2+Na2CO3=CaCO3↓+2NaClO 生成白色沉淀 漂白粉 Ca(ClO)2+H2O+CO2=2HClO+CaCO3、2HClO![]() 2HCl+O2↑
2HCl+O2↑
【解析】
A是密度最小的气体,应为H2,B在通常情况下呈黄绿色,应为Cl2,纯净的A可以在B中安静地燃烧生成D,则D为HCl,把气体Cl2通入到适量石灰乳中可以得到白色浑浊物D,则D为CaCl2和Ca(ClO)2的混合物,结合对应物质的性质解答该题。
A是密度最小的气体,应为H2,B在通常情况下呈黄绿色,应为Cl2,纯净的A可以在B中安静地燃烧生成D,则D为HCl,把气体Cl2通入到适量石灰乳中可以得到白色浑浊物D,则D为CaCl2和Ca(ClO)2的混合物,
(1)①A与B反应是氢气在点燃条件下与氯气反应生成氯化氢,反应方程式为:H2+Cl2![]() 2HCl,
2HCl,
故答案为:H2+Cl2![]() 2HCl;
2HCl;
②氯气与水反应生成盐酸和次氯酸,反应的方程式为:Cl2+H2OHCl+HClO,
故答案为:Cl2+H2OHCl+HClO;
③氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,
故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;
④氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应的方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(2)氯气溶于水会生成盐酸能与硝酸银生成氯化银沉淀,HCl与硝酸银反应生成氯化银沉淀,
故答案为:BC;
(3)①D为CaCl2和Ca(ClO)2的混合物,滴加碳酸钠溶液发生的化学反应为CaCl2+Na2CO3=CaCO3↓+2NaCl、Ca(ClO)2+Na2CO3=CaCO3↓+2NaClO,
故答案为:CaCl2+Na2CO3=CaCO3↓+2NaCl、Ca(ClO)2+Na2CO3=CaCO3↓+2NaClO;
②向第二份溶液中滴加硝酸酸化的硝酸银溶液,氯离子和银离子反应生成氯化银白色沉淀,
故答案为:生成白色沉淀;
③因为具有漂白性又称为漂白粉;在空气中容易与二氧化碳、水发生反应变质,其反应的方程式为:Ca(ClO)2+H2O+CO2=2HClO+CaCO3、2HClO![]() 2HCl+O2↑;
2HCl+O2↑;
故答案为:漂白粉;Ca(ClO)2+H2O+CO2=2HClO+CaCO3、2HClO![]() 2HCl+O2↑。
2HCl+O2↑。


科目:高中化学 来源: 题型:
【题目】研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式:_____________。
(2)在海洋循环中,通过如图所示的途径固碳。

①写出钙化作用的离子方程式:_____________。
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程式如下,将其补充完整:_____________+_____________=(CH2O)x+x18O2+xH2O,_____________
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2,用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如图所示),将虚线框中的装置补充完整并标出所用试剂。_____________

②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xmol/LHCl溶液滴定,消耗ymLHCl溶液,海水中溶解无机碳的浓度=_____________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示(吸附在金催化剂表面上的物种用·标注)。

下列说法正确的是( )
A.水煤气的变换反应是吸热反应
B.该历程中逆向的最大能垒(活化能)E逆=2.02eV
C.催化剂能够使物质的能量升高
D.反应历程中,生成过渡态I比过渡态II容易
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用蒸馏水稀释10mLpH=11的氨水。下列叙述正确的是( )
A.该10mL氨水的浓度为0.001mol/L
B.稀释至100mL时,溶液的pH小于10
C.稀释时,溶液中所有的离子的浓度均变小
D.稀释过程中,![]() 的值一定增大
的值一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:

(1)图是1 mol NO2和1 mol CO反应生成CO2 和NO过程中的能量变化示意图,请写出NO2 和CO反应的热化学方程式______________________。
(2)在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
T/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
请回答下列问题:
①试比较K1、K2的大小,K1_________K2(填”>”“=“或”<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_________(填序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v正(N2)=3v逆(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g) ![]() N2(g)+3H2(g)的平衡常数K为______。当测得NH3、N2、H2的浓度分别为3 mol L1、2 mol L1、1 mol L1时,则该反应的v正(N2)____v逆(N2)(填”>”“=“或”<”)
N2(g)+3H2(g)的平衡常数K为______。当测得NH3、N2、H2的浓度分别为3 mol L1、2 mol L1、1 mol L1时,则该反应的v正(N2)____v逆(N2)(填”>”“=“或”<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年6月5日美国商务部表示,美方将采取“空前行动”,确保对科技业和军方极其关键的战略性矿物及稀土供应无虞。我国稀土出口量世界第一。以氟碳铈矿(主要含CeFCO3,少量其他稀土盐LnFCO3、非稀土元素Fe、Al、Mg和SiO2等)为原料制备CeO2的一种工艺流程如图所示:

(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是_________________________________。“氧化焙烧”时,CeFCO3和其他稀土盐LnFCO3分别转化为CeO2和Ln2O3,请写出生成的CeO2化学方程式为:________________________。
(2)“氯化”过程的目的是将CeO2和Ln2O3分别转化为可溶性的CeCl3和LnCl3,除去Fe2O3、Al2O3、MgO、SiO2等杂质。若溶液中c(Ce3+)=0.01mol/L,为确保不析出Ce(OH)3沉淀,则溶液的pH________(填pH的范围)。(已知Ksp[Ce(OH)3=1.0×10-20])
(3)CeO2和Ln2O3混合物中加入稀盐酸,Ln2O3溶解生成LnOCl的化学方程式为:___________________________________________________。
(4)化工生产条件的选择:
①“氯化”条件的选择
将氧化焙烧后氟碳铈矿和氯化铵按1:3、1:4、1:5、1:6、1:7质量比混合,在325℃下真空焙烧60min。稀土矿氧化物转化成稀土氯化物的氯化率如图所示:

氧化焙烧后氟碳铈矿和氯化铵的最佳质量比为________。
②“氧化”条件的选择
氧化过程中,反应温度、反应时间对混合稀土氯化物氧化率的关系如图所示:

最佳温度和时间是_________,原因是_________________________________________。
(5)取上述流程中得到的CeO2产品0.4500g,加硫酸溶解后,用0.1000molL-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其它杂质均不反应),消耗25.00mL标准溶液.该产品中CeO2的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配平下列方程式(不需写出配平过程)
________H2S+_______HNO3 =________S↓ +________NO↑ +_______H2O
________S+________KOH=________K2S+________K2SO3 +________H2O
________KMnO4+________HCl(浓)=________KCl+________MnCl2+________Cl2↑+________H2O
(2)在酸性条件下,向含铬废水中加入FeSO4溶液,可将Cr2O![]() 还原为Cr3+,该过程的离子反应方程式为________________________。
还原为Cr3+,该过程的离子反应方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
![]()
A. 氢氧燃料电池工作时,![]() 在负极上失去电子
在负极上失去电子
B. ![]() 溶液加热后,溶液的pH减小
溶液加热后,溶液的pH减小
C. 常温常压下,![]() 中含有的分子数为
中含有的分子数为![]() 个
个
D. 室温下,稀释![]() 溶液,溶液的导电能力增强
溶液,溶液的导电能力增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以NH4Cl酸性蚀铜废液[含NH4Cl,Cu(NH3)4Cl2、CuCl、CuSO4及盐酸等]为原料制备CuCl并回收Cu(OH)2的工艺流程如图:
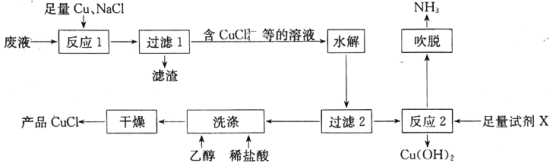
已知:CuCl溶于浓盐酸,难溶于水,不溶于乙醇。
回答下列问题:
(1)“反应1”中,NaCl、Cu与CuSO4反应的离子方程式为__;生产中常将“过滤1”的滤渣返回到“反应1”中,其目的是__。
(2)“水解”步骤中,溶液中的CuCl43-在加入大量水稀释即可析出CuCl,原因是__(结合离子方程式,从平衡角度分析)。
(3)湿的CuCl在空气中易被氧化为Cu2(OH)3Cl,该反应的化学方程式为__。
(4)“反应2”需加入的试剂X是__;“吹脱”出来的NH3可用于生产碳铵化肥,主要反应的化学方程式为__。
(5)测定产品中CuCl质量分数的步骤如下:称取ag产品,加入稍过量的FeCl3溶液,待溶解后用邻菲罗啉作指示剂,立刻用cmol·L-1的Ce(SO4)2标准溶液滴定到终点,消耗标准溶液VmL。则产品中CuCl的质量分数为__(已知滴定反应为Ce4++Fe2+=Ce3++Fe3+,列出计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com