
����Ŀ��һ����NH4Cl����ʴͭ��Һ[��NH4Cl��Cu(NH3)4Cl2��CuCl��CuSO4�������]Ϊԭ���Ʊ�CuCl������Cu(OH)2�Ĺ���������ͼ��
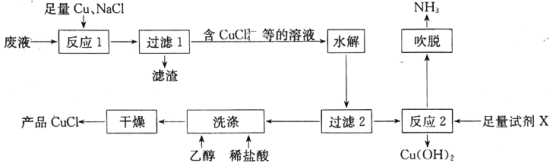
��֪��CuCl����Ũ���ᣬ������ˮ���������Ҵ���
�ش��������⣺
��1������Ӧ1���У�NaCl��Cu��CuSO4��Ӧ�����ӷ���ʽΪ__�������г���������1�����������ص�����Ӧ1���У���Ŀ����__��
��2����ˮ���������У���Һ�е�CuCl43-�ڼ������ˮϡ�ͼ�������CuCl��ԭ����__(������ӷ���ʽ����ƽ��Ƕȷ���)��
��3��ʪ��CuCl�ڿ������ױ�����ΪCu2(OH)3Cl���÷�Ӧ�Ļ�ѧ����ʽΪ__��
��4������Ӧ2���������Լ�X��__����������������NH3����������̼炙��ʣ���Ҫ��Ӧ�Ļ�ѧ����ʽΪ__��
��5���ⶨ��Ʒ��CuCl���������IJ������£���ȡag��Ʒ�������Թ�����FeCl3��Һ�����ܽ�����ڷ�������ָʾ����������cmol��L-1��Ce(SO4)2����Һ�ζ����յ㣬���ı���ҺVmL�����Ʒ��CuCl����������Ϊ__(��֪�ζ���ӦΪCe4����Fe2��=Ce3����Fe3�����г�����ʽ)��
���𰸡�Cu+Cu2++8Cl-![]() 2CuCl43- ���ͭԪ�ص������� CuCl43-
2CuCl43- ���ͭԪ�ص������� CuCl43-![]() CuCl+3Cl-��ϡ��ʱ��ƽ��������������ķ����ƶ�����ƽ������ 4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl��12CuCl+3O2+6H2O=4Cu2(OH)3Cl+4CuCl2 NaOH��Һ NH3+H2O+CO2=NH4HCO3
CuCl+3Cl-��ϡ��ʱ��ƽ��������������ķ����ƶ�����ƽ������ 4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl��12CuCl+3O2+6H2O=4Cu2(OH)3Cl+4CuCl2 NaOH��Һ NH3+H2O+CO2=NH4HCO3 ![]() ��100%
��100%
��������
NH4Cl����ʴͭ��Һ[��NH4Cl��Cu(NH3)4Cl2��CuCl��CuSO4�������]������ͭ���ʺ��Ȼ��ƣ�����CuCl43-��ˮ�������CuCl����CuCl����Ũ���ᣬ������ˮ���������Ҵ��������Ҵ����ӡ�
��1������Ӧ1���У�����������ԭ��Ӧԭ����NaCl��Cu��CuSO4��Ӧ�����ӷ���ʽΪCu+Cu2++8Cl-![]() 2CuCl43-����������ͭԪ�أ������г���������1�����������ص�����Ӧ1���У���Ŀ�������ͭԪ�ص������ʡ�
2CuCl43-����������ͭԪ�أ������г���������1�����������ص�����Ӧ1���У���Ŀ�������ͭԪ�ص������ʡ�
��2����ˮ���������У���Һ�е�CuCl43-�ڼ������ˮϡ�ͼ�������CuCl��ԭ����CuCl43-![]() CuCl+3Cl-��ϡ��ʱ��ƽ��������������ķ����ƶ�����ƽ�����ơ�
CuCl+3Cl-��ϡ��ʱ��ƽ��������������ķ����ƶ�����ƽ�����ơ�
��3��ʪ��CuCl�ڿ������ױ�����ΪCu2(OH)3Cl������������ԭ��Ӧԭ�����÷�Ӧ�Ļ�ѧ����ʽΪ4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl��12CuCl+3O2+6H2O=4Cu2(OH)3Cl+4CuCl2��
��4������2����Һ�к���Cu2+ ����Ӧ����������ͭ����ˣ�����Ӧ2���������Լ�X��NaOH��Һ����������������NH3����������̼炙��ʣ��������к���笠���̼Ԫ�أ�̼Ԫ�ض�Ϊ̼�������Ҫ��Ӧ�Ļ�ѧ����ʽΪNH3+H2O+CO2=NH4HCO3��
��5����֪�ζ���ӦΪCe4����Fe2��=Ce3����Fe3������cmol��L-1��Ce(SO4)2����Һ�ζ����յ㣬���ı���ҺVmL�����÷�Ӧ������0.01cVmol���������ӣ���Ʒ��CuCl���Ȼ����ķ�ӦΪCuCl+Fe3+=Cu2++Fe2+ +Cl-������Ʒ��CuCl�����ʵ���Ϊ0.01cVmol����Ʒ��CuCl����������Ϊ![]() ��100%��
��100%��


 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C�������壬A���ܶ���С�����壬B��ͨ������³ʻ���ɫ��������A������B�а�����ȼ������C��������Bͨ�뵽����ʯ�����п��Եõ���ɫ������D����ݴ˻ش��������⣺
(1)д�����и���Ӧ�Ļ�ѧ����ʽ
�ٴ�����A��B�а�����ȼ������C_______________
�ڽ�����Bͨ�뵽ˮ�У�__________��
�۽�����Bͨ�뵽NaOH��Һ�У�_______________________
�ܽ�����Bͨ�뵽����ʯ�����У�_______________________
(2)����������ֱ�ͨ��������������Һ�У����ְ�ɫ������������________(����ĸ��ʾ)��
(3)����ɫ������D����ˮ�õ�������Һ���ֱ�ȡ�����ó���Һ���ݡ�
�����һ���еμ�̼������Һ�۲쵽���ֳ�����������Ӧ�Ļ�ѧ����ʽΪ______________��________��
����ڶ�����Һ�еμ������ữ����������Һ����۲쵽____________(������)��
�۰�ɫ������D�����Ư�����ֳ�Ϊ______________���������ڿ��������ױ��ʵ�ԭ��Ϊ_______________(�û�ѧ����ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֳ���Ԫ�ص����ʻ�ṹ��Ϣ���±����Ը�����Ϣ�ش��й����⡣
Ԫ�� | A | B | C | D |
���� �ṹ ��Ϣ | ������ӹ���7���˶�״̬ | ԭ�ӵ�M����1�ԳɶԵ�p���� | һ�ֺ��ص�������Ϊ35��������Ϊ64 | �ж���ͬλ�أ�����һ�������������ԭ��������У |
��1��д��Bԭ�ӵĵ����Ų�ʽ______��д��Cԭ�ӵĵ����Ų�ʽ______
��2������Ԫ���зǽ�������ǿ��Ԫ����______����������ǿ��Ԫ����______����һ����������Ԫ����______��
��3��һ��������B��C���ʼ��ܷ�Ӧ����Ӧ�ķ�Ӧ����ʽΪ______��
��4����֪S+6HNO3=H2SO4+6NO2��+2H2O���÷�Ӧ�����������������ȡ���ᣬ���÷�Ӧ��������˵����Ԫ�صķǽ����Ա���Ԫ�ص�ǿ��������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���amol������bmol�����Ļ������ͨ��һ���̶��ݻ����ܱ������У�������ӦN2(g)��3H2(g) ![]() 2NH3(g)��
2NH3(g)��
(1)����Ӧ���е�ijʱ��tʱ��nt(N2)��13 mol��nt(NH3)��6 mol����aֵΪ________��
(2)��Ӧ�ﵽƽ��ʱ�������������Ϊ716.8 L(��״����)�����а����������Ϊ25%��ƽ��ʱ���������ʵ���Ϊ________��
(3)ԭ���������ƽ��������������ʵ���֮��(д��������ȣ���ͬ)nʼ��nƽ��______��
(4)ԭ������a��b��________��
(5)�ﵽƽ��ʱ��������У�n(N2)��n(H2)��n(NH3)��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���������������ԭ�����͵���
A. ����ɫ��NO2����ѹ����ɫ�ȱ�����dz
B. ��ѹ�ȳ�ѹ�����ںϳ�SO3�ķ�Ӧ
C. ������������ڰ��ĺϳ�
D. ��ҵ��ȡ������Na(l)+KCl(l)![]() NaCl(l)+K(g)ѡȡ���˵��¶ȣ�ʹK��������ӷ�Ӧ������з������
NaCl(l)+K(g)ѡȡ���˵��¶ȣ�ʹK��������ӷ�Ӧ������з������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ȡ0.1mol/L��NaA��NaB��������Һ��1L���ֱ�ͨ��0.02molCO2���������·�Ӧ��NaA+CO2+H2O=HA+NaHCO3��2NaB+CO2+H2O=2HB+Na2CO3����1LHA��HB����Һ�ֱ��ˮϡ�������ΪVLʱ��������ͼ���ߣ�������˵����ȷ���ǣ� ��
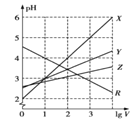
A.X��HA��Y��HB
B.������pH��NaA��Һ>NaB��Һ
C.�������£�Ũ�Ⱦ�Ϊ0.1mol/L��NaA��HA�Ļ����ҺpH>7����c(A-)>c(HA)
D.�ڵ�Ũ�ȵ�NaA��NaB�����Һ��ͨ��HCl������ʱ��c(Cl-)=c(HA)+c(HB)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
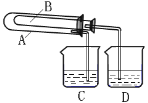
����Ŀ���ں�����ߺ�DZˮͧ�п��ù���������Ϊ����������ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ������ͼ�е�ʵ��װ�ý���ʵ�飬֤���������ƿ�����������

(1)A����ȡCO2��װ�á�д��A�з�����Ӧ�ķ���ʽ______________��
(2)��д���пո�
���� | �����Լ� | ������Լ���Ŀ�� |
B | ����NaHCO3��Һ | _________ |
C | _________ | _________ |
D | _________ | _________ |
(3)д�����������������̼��Ӧ�Ļ�ѧ����ʽ��__________��
(4)ij����С��Ϊ����֤Na2CO3��NaHCO3���ȶ��ԣ��������ͼ��ʾ��ʵ��װ�ã�����Ϊ���Թ�B��Ӧ�ŵ�������_______��C��D�����ձ��е���Һ�ֱ���______��_______��Na2CO3��ĩ�л�������NaHCO3����ȥ���ʵķ���(д����ʽ)________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10 mL 0.10molL1-1YOH��Һ���μ�0.20molL-1HX ��Һ�������Һ��pH �仯��ͼ��ʾ(�¶Ⱥ�����仯���Ѳ���)�����н��۴������
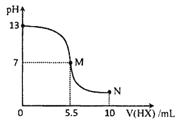
A.HXΪһԪ���ᣬYOH ΪһԪǿ��
B.M���Ӧ��Һ��ˮ�ĵ���̶ȴ���N ����Һ��ˮ�ĵ���̶�
C.N���Ӧ��Һ������Ũ�ȣ�c(HX)> c(X - ) > c(Y+ ) > c(H+ ) > c(OH-)
D.����ʱ,pH = a ��YX��Һ��ˮ�������c(OH-)=l.0��10-(14-a)molL-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʾ���ʱ仯�Ļ�ѧ������ȷ����( )
A.̼��ĵ��뷽��ʽ��H2CO3 ![]() CO32����2 H+
CO32����2 H+
B.���ᱵ�ĵ��뷽��ʽ��BaSO4 ![]() Ba2++SO42��
Ba2++SO42��
C.����ȼ�յ��Ȼ�ѧ����ʽ��H2(g)��![]() O2(g)=H2O(l)��H����285.8 kJ��mol��1
O2(g)=H2O(l)��H����285.8 kJ��mol��1
D.C����ȫȼ�յ��Ȼ�ѧ����ʽ��C(s)��![]() O2 (g)=CO(g) ��H = 110.5 kJ��mol-1
O2 (g)=CO(g) ��H = 110.5 kJ��mol-1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com